Амиксин® | Таб., покр. пленочной оболочкой, 60 мг: 6, 10, 12 или 20 шт. рег. №: ЛСР-000175/08 Дата перерегистрации: 27.07.17 Таб., покр. пленочной оболочкой, 125 мг: 6, 10, 12 или 20 шт. рег. №: ЛСР-000175/08 Дата перерегистрации: 27.07.17 | |||
Бессмертника песчаного цветки | Сырье растительное измельченное 35 г: пачки рег. | |||
Бессмертника песчаного цветки | Сырье растительное измельченное 50 г: пачки рег. №: Р N001338/02 | |||
Бессмертника песчаного цветки | Сырье растительное измельченное 50 г: пачки рег. | |||
Бессмертника песчаного цветки | Сырье растительное цельное 50 г: пачки рег. №: Р N001338/01 | |||
Бессмертника песчаного цветки | Сырье растительное цельное: пачка 30 г. рег. №: ЛП-001583 | |||
Бессмертника песчаного цветки | Сырье растительное: 50 г пачка рег. №: ЛП-002182 | |||
Бессмертника песчаного цветки | Сырье растительное: пачка 30 г. рег. №: ЛСР-007062/09 | |||
Бессмертника песчаного цветки | Сырье растительное: пачка 30 г. рег. №: 72/267/27 | |||
Бессмертника песчаного цветки | Сырье растительное: пачка 30 г. рег. №: ЛП-000536 | |||
Бессмертника песчаного цветки | Сырье растительное: пачка 50 г. рег. №: ЛП-000536 | |||
Бессмертника песчаного цветки | Сырье растительное: пачка 75 г. рег. №: ЛП-000536 | |||
Бессмертника песчаного цветки | Цветки измельченные: пачка 30 г рег. №: ЛСР-001832/08 Дата перерегистрации: 14.03.16 | |||
Вобэнзим | Таблетки кишечнорастворимые, покрытые оболочкой рег. Дата перерегистрации: 21.08.17 | |||
Галавит® | Порошок д/пригот. р-ра д/в/м введения 50 мг: фл. 3 или 5 шт. рег. №: Р N000088/02 Дата перерегистрации: 07.10.13 Порошок д/пригот. рег. №: Р N000088/02 Дата перерегистрации: 07.10.13 | |||
Галавит® | Супп. ректальные 100 мг: 5 или 10 шт. рег. №: Р N000088/03 Дата перерегистрации: 17.06.20 | |||
Галавит® | Супп. рег. №: ЛСР-002796/10 Дата перерегистрации: 26.09.13 | |||
Гепа-Мерц | Гранулы д/пригот. р-ра д/приема внутрь 3 г/1 пак.: пак. 5 г 10 или 30 шт. рег. №: П N015093/01 Дата перерегистрации: 18.03.20 | Выпускающий контроль качества: MERZ PHARMA (Германия) | ||
Гепа-Мерц | Конц. рег. №: П N015093/02 | |||
Глатион | Порошок д/приг. р-ра д/в/в и в/м введ. 0.6 г: фл. 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 шт. рег. №: ЛП-001337 Порошок д/приг. р-ра д/в/в и в/м введ. рег. №: ЛП-001337 Порошок д/приг. р-ра д/в/в и в/м введ. 1.8 г: фл. 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 шт. рег. №: ЛП-001337 Порошок д/приг. р-ра д/в/в и в/м введ. 1.2 г: фл. 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 шт. рег. №: ЛП-001337 | |||
Глутаргин | Конц. рег. №: ЛСР-000880/09 | |||
Глутаргин | Р-р д/инф. 200 мг/5 мл: амп. 5 или 10 шт. рег. №: ЛСР-000879/09 | |||
Глутаргин | Таб. рег. №: ЛСР-000881/09 | |||
Глутаргин | Таб. 750 мг: 30 или 60 шт. рег. №: ЛП-000074 | |||
Глутаргин алкоклин | Порошок д/пригот. рег. №: ЛП-000063 Дата перерегистрации: 16.08.18 | |||
Глутаргин алкоклин | Таб. 1 г: 2 или 10 шт. рег. №: ЛП-000064 Дата перерегистрации: 21.11.17 | |||
Глюкоза | Р-р д/инф. рег. №: ЛП-000730 Р-р д/инф. 10%: контейн. 250 мл или 500 мл рег. №: ЛП-000730 Р-р д/инф. 20%: контейн. 250 мл или 500 мл рег. №: ЛП-000730 Р-р д/инф. 40%: контейн. 250 мл или 500 мл рег. №: ЛП-000730 | |||
Дексаметазон-Виал | Раствор для инъекций рег. | Упаковано: ОЗОН (Россия) | ||
Дипана® | Таблетки, покрытые оболочкой рег. №: ЛС-001751 | |||
Карсил® Форте | Капсулы рег. №: ЛП-000128 Дата перерегистрации: 12.01.16 | |||
Лайфферон® | Лиофилизат д/пригот. рег. №: ЛС-001989 Лиофилизат д/пригот. р-ра д/в/м, субконъюнктивального введ. и закапывания в глаз 3 млн.МЕ: амп. 5 или 10 шт., фл. 5 шт. рег. №: ЛС-001989 Лиофилизат д/пригот. р-ра д/в/м, субконъюнктивального введ. и закапывания в глаз 5 млн.МЕ: амп. 5 или 10 шт., фл. 5 шт. рег. №: ЛС-001989 Лиофилизат д/пригот. р-ра д/в/м, субконъюнктивального введ. и закапывания в глаз 500 тыс.МЕ: амп. 5 или 10 шт., фл. 5 шт. рег. №: ЛС-001989 | |||
Лайфферон® | Р-р д/в/м, субконъюнктивального введ. рег. №: ЛСР-000091 Р-р д/в/м, субконъюнктивального введ. и закапывания в глаз 3 млн.МЕ: амп. 5 или 10 шт., фл. 5 шт. рег. №: ЛСР-000091 Р-р д/в/м, субконъюнктивального введ. и закапывания в глаз 5 млн.МЕ: амп. 5 или 10 шт., фл. 5 шт. рег. №: ЛСР-000091 Р-р д/в/м, субконъюнктивального введ. и закапывания в глаз 500 тыс.МЕ: амп. 5 или 10 шт., фл. 5 шт. рег. №: ЛСР-000091 | |||
ЛИВ. | Капли д/приема внутрь: фл. 60 мл в компл. с пипеткой-дозатором рег. №: ЛСР-009411/09 Таб.: 100 шт. рег. №: П N014783/01 | |||
Ливенциале | Раствор для в/в введения рег. Дата перерегистрации: 09.11.18 | Произведено и расфасовано: SCAN BIOTECH (Индия) | ||
Ливолайф Форте | Капсулы рег. | |||
Максар | Таблетки, покрытые пленочной оболочкой рег. №: Р N003294/01 | |||
Метионин | Таб. рег. №: ЛС-001209 | |||
Метипред | Таб. 4 мг: 30 или 100 шт. рег. №: П N015709/01 Дата перерегистрации: 14.09.20 Таб. 16 мг: 30 или 100 шт. рег. №: П N015709/01 Дата перерегистрации: 14. | Произведено и расфасовано: ORION CORPORATION (Финляндия) | ||
Орнилатекс® | Концентрат для приготовления раствора для инфузий рег. Дата перерегистрации: 15.07.15 | |||
Полифан | Порошок д/приема внутрь 1 кг: пак. рег. №: Р N001944/01 | |||
Полифан | Порошок д/приема внутрь 100 г: пак. рег. №: Р N001944/01 | |||
Полифан | Порошок д/приема внутрь 500 г: пак. рег. №: Р N001944/01 | |||
Полифепан | Гранулы д/приема внутрь 100 г: банки рег. | |||
Полифепан | Гранулы д/приема внутрь 50 г: пачки 1 или 10 шт. рег. №: Р N001047/03 | |||
Полифепан | Таб. рег. №: Р N001047/04 | |||
Полифепан® | Порошок д/приема внутрь: 10 г, 50 г, 100 г, 200 г или 250 г пак. рег. №: ЛП-005878 | |||
Преднизол | Раствор для в/в и в/м введения рег. | |||
Преднизолон | Р-р д/инъекц. 30 мг/1 мл: амп. 3, 5, 6, 10 или 20 шт. рег. №: П N014426/01-2002 | |||
Преднизолон | Таб. рег. №: ЛС-001000 | |||
Преднизолон | Таб. 5 мг: 20, 30, 50 или 60 шт. рег. №: ЛП-000773 | |||
Пробифор® | Капс. рег. №: ЛС-002558 Дата перерегистрации: 03.06.20 Порошок д/приема внутрь 500 млн.КОЕ: пак. 6, 10 или 30 шт. рег. №: Р N000090/01 Дата перерегистрации: 04.06.20 Капс. 500 млн.КОЕ: фл. 6, 10, 18 шт. рег. №: ЛС-002558 Дата перерегистрации: 03.06.20 | |||
Реаферон-ЕС | Лиоф. рег. №: Р N000642/01 Лиоф. д/пригот. р-ра д/инъекц. и местного прим. 3 млн.МЕ: амп. 5 или 10 шт., фл. 5 шт. рег. №: Р N000642/01 Лиоф. д/пригот. р-ра д/инъекц. и местного прим. 5 млн.МЕ: амп. 5 или 10 шт., фл. 5 шт. рег. №: Р N000642/01 Лиоф. д/пригот. р-ра д/инъекц. и местного прим. 500 тыс.МЕ: амп. 5 или 10 шт., фл. 5 шт. рег. №: Р N000642/01 | |||
Ремаксол® | Раствор для инфузий рег. Дата перерегистрации: 13.02.20 | |||
Тимоген® | Р-р д/в/м введения 100 мкг/1 мл: амп. 5 или 10 шт. рег. №: ЛС-002304 Дата перерегистрации: 30.10.19 | |||
Тыквеол® | Масло д/приема внутрь: фл. рег. №: Р N002321/03 Капс. 450 мг: 10, 20, 30, 50, 84, 90 или 180 шт. рег. №: Р N002321/01 Супп. ректальные 500 мг: 10 шт. рег. №: Р N002321/02 Дата перерегистрации: 28.06.19 | |||
Урсосан® форте | Капс. рег. №: П N016302/01 Дата перерегистрации: 03.03.20 Таб., покр. пленочной оболочкой, 500 мг: 10, 50 или 100 шт. рег. №: ЛП-003388 | |||
Флогэнзим | Таблетки кишечнорастворимые, покрытые пленочной оболочкой рег. №: П N012753/01 Дата перерегистрации: 22. | |||
Фосфоглив® | Капс.: 50 шт. рег. №: Р N002528/01 Дата перерегистрации: 09.01.19 | |||
Фосфоглив® | Лиофилизат д/пригот. рег. №: Р N002528/02 Дата перерегистрации: 18.05.17 | |||
Фосфоглив® Форте | Капсулы рег. №: ЛСР-008120/08 Дата перерегистрации: 10.10.17 | |||
Фосфонциале® | Капсулы рег. Дата перерегистрации: 07.07.20 | |||
Циклоферон® | Р-р д/в/в и в/м введения 125 мг/1 мл: амп. 2 мг 5 шт. рег. №: Р N001049/03 Дата перерегистрации: 09.11.18 | |||
Энтеросгель® | Паста д/приема внутрь: пак. рег. №: ЛП-N (000036)-(РГ- RU) | |||
Энтерумин | Порошок д/пригот. суспензии д/приема внутрь 5 г: пакеты 10 или 20 шт. рег. №: ЛСР-004123/09 Порошок д/пригот. суспензии д/приема внутрь 10 г: пакеты 10 или 20 шт. рег. №: ЛСР-004123/09 | |||
Эссенциале® Н | Раствор для в/в введения рег. №: П N016326/01 Дата перерегистрации: 12.12.16 | |||
Эссенциальные фосфолипиды | Р-р д/в/в введения 50 мг/1 мл: амп. рег. №: ЛП-000605 Дата перерегистрации: 19.10.16 | |||
Гепасол А | Раствор для инфузий рег. | |||
Декстроза | Р-р д/инф. 10%: бут. или фл. 100 мл рег. №: ЛП-000161 | |||
Декстроза | Р-р д/инф. рег. №: ЛП-000161 | |||
Эрбисол® | Раствор для инъекций рег. | Официальный дистрибьютор в РФ: ФК ПУЛЬС (Россия) | ||
Альгерон® | Раствор для п/к введения рег. Дата перерегистрации: 04.03.19 | |||
Альтевир® | Р-р д/инъекц. 1 млн.МЕ/1 мл: амп. 5 или 10 шт., фл. 1 или 5 шт., шприцы 1, 3 или 9 шт. рег. №: ЛС-001950 Р-р д/инъекц. 1 млн.МЕ/0.5 мл: амп. 5 или 10 шт., фл. 1 или 5 шт., шприцы 1, 3 или 9 шт. рег. №: ЛС-001950 Р-р д/инъекц. 3 млн.МЕ/1 мл: амп. 5 или 10 шт., фл. 1 или 5 шт., шприцы 1, 3 или 9 шт. рег. №: ЛС-001950 Р-р д/инъекц. 3 млн.МЕ/0.5 мл: амп. 5 или 10 шт., фл. 1 или 5 шт., шприцы 1, 3 или 9 шт. рег. №: ЛС-001950 Р-р д/инъекц. 5 млн.МЕ/0.5 мл: амп. 5 или 10 шт., фл. 1 или 5 шт., шприцы 1, 3 или 9 шт. рег. №: ЛС-001950 Р-р д/инъекц. 5 млн.МЕ/1 мл: амп. 5 или 10 шт., фл. 1 или 5 шт., шприцы 1, 3 или 9 шт. рег. №: ЛС-001950 Р-р д/инъекц. 10 млн.МЕ/0.5 мл: амп. 5 или 10 шт., фл. 1 или 5 шт., шприцы 1, 3 или 9 шт. рег. №: ЛС-001950 Р-р д/инъекц. 10 млн.МЕ/1 мл: амп. 5 или 10 шт., фл. 1 или 5 шт., шприцы 1, 3 или 9 шт. рег. №: ЛС-001950 Р-р д/инъекц. 15 млн.МЕ/0.5 мл: амп. 5 или 10 шт., фл. 1 или 5 шт., шприцы 1, 3 или 9 шт. рег. №: ЛС-001950 Р-р д/инъекц. 15 млн.МЕ/1 мл: амп. 5 или 10 шт., фл. 1 или 5 шт., шприцы 1, 3 или 9 шт. рег. №: ЛС-001950 | |||
Амиксин® | Таб. рег. №: ЛСР-000175/08 Дата перерегистрации: 27.07.17 Таб., покр. пленочной оболочкой, 125 мг: 6, 10, 12 или 20 шт. рег. №: ЛСР-000175/08 Дата перерегистрации: 27.07.17 | |||
| БАД | Артишока экстракт | Таб. рег. №: RU.77.99.11.003.Е. 011885.12. | ||
Бестим | Лиофилизат д/приготов. р-ра д/в/м введения 100 мкг: амп. 5 шт. рег. №: Р N003335/03 Дата перерегистрации: 16.12.16 | |||
Беталейкин® | Лиофилизат д/пригот. рег. №: Р N000222/01 Лиофилизат д/пригот. р-ра д/в/в и п/к введения 0.05 мкг: амп. 5 шт. рег. №: Р N000222/01 Лиофилизат д/пригот. р-ра д/в/в и п/к введения 1 мкг: амп. 5 шт. рег. №: Р N000222/01 | |||
Бициклол® | Таблетки рег. Дата перерегистрации: 08.08.17 | |||
Викейра Пак | Таблеток набор рег. №: ЛП-002965 Дата перерегистрации: 22.04.20 | Производитель (таблетки дасабувира): AbbVie Ireland NL (Ирландия) Производитель (таблетки омбитасвира+паритапревира+ритонавира): Fournier Laboratories Ireland (Ирландия) Фасовщик: AbbVie (США) Упаковщик и выпускающий контроль качества: AbbVie (США) ОРТАТ (Россия) | ||
Виферон® | Суппозитории рект. рег. №: Р N000017/01 Суппозитории рект. 3 000 000 МЕ: 10 шт. рег. №: Р N000017/01 Суппозитории рект. 150 000 МЕ: 10 шт. рег. №: Р N000017/01 Суппозитории рект. 500 000 МЕ: 10 шт. рег. №: Р N000017/01 | |||
Вобэнзим | Таблетки кишечнорастворимые, покрытые оболочкой рег. Дата перерегистрации: 21.08.17 | |||
Галавит® | Порошок д/пригот. р-ра д/в/м введения 50 мг: фл. 3 или 5 шт. рег. №: Р N000088/02 Дата перерегистрации: 07.10.13 Порошок д/пригот. рег. №: Р N000088/02 Дата перерегистрации: 07.10.13 | |||
Галавит® | Супп. ректальные 100 мг: 5 или 10 шт. рег. №: Р N000088/03 Дата перерегистрации: 17.06.20 | |||
Галавит® | Супп. рег. №: ЛСР-002796/10 Дата перерегистрации: 26.09.13 | |||
Гепа-Мерц | Гранулы д/пригот. р-ра д/приема внутрь 3 г/1 пак.: пак. 5 г 10 или 30 шт. рег. №: П N015093/01 Дата перерегистрации: 18.03.20 | Выпускающий контроль качества: MERZ PHARMA (Германия) | ||
Гепабене | Капсулы рег. | Произведено: MERCKLE (Германия) контакты: (Израиль) | ||
Гептрал® | Таб., покр. кишечнорастворимой оболочкой, 400 мг: 10 или 20 шт. рег. №: П N011968/01 Дата перерегистрации: 26.03.18 | Произведено: AbbVie (Италия) | ||
Глатион | Порошок д/приг. р-ра д/в/в и в/м введ. 0.6 г: фл. 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 шт. рег. №: ЛП-001337 Порошок д/приг. р-ра д/в/в и в/м введ. 0.3 г: фл. 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 шт. рег. №: ЛП-001337 Порошок д/приг. р-ра д/в/в и в/м введ. 1.8 г: фл. 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 шт. рег. №: ЛП-001337 Порошок д/приг. р-ра д/в/в и в/м введ. 1.2 г: фл. 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 шт. рег. №: ЛП-001337 | |||
Глутаргин | Конц. д/пригот. р-ра д/инф. 2 г/5 мл: амп. 10 или 20 шт. рег. №: ЛСР-000880/09 | |||
Глутаргин | Р-р д/инф. 200 мг/5 мл: амп. 5 или 10 шт. рег. №: ЛСР-000879/09 | |||
Глутаргин | Таб. 250 мг: 30 или 60 шт. рег. №: ЛСР-000881/09 | |||
Глутаргин | Таб. 750 мг: 30 или 60 шт. рег. №: ЛП-000074 | |||
Глутаргин алкоклин | Порошок д/пригот. р-ра д/приема внутрь 1 г: пак. 2, 5 или 10 шт. рег. №: ЛП-000063 Дата перерегистрации: 16.08.18 | |||
Глутаргин алкоклин | Таб. 1 г: 2 или 10 шт. рег. №: ЛП-000064 Дата перерегистрации: 21.11.17 | |||
Глутоксим® | Р-р д/инъекц. 10 мг/1 мл: амп. 1 мл 5 шт., амп. 2 мл 5 шт. рег. №: Р N002010/01 Дата перерегистрации: 22.04.19 Р-р д/инъекц. 30 мг/1 мл: амп. 1 мл 5 шт., амп. 2 мл 5 или 10 шт. рег. №: Р N002010/01 Дата перерегистрации: 22.04.19 | |||
Даклинза | Таб. покр. пленочной оболочкой 30 мг: 28 шт. рег. №: ЛП-003088 Таб. покр. пленочной оболочкой 60 мг: 28 шт. рег. №: ЛП-003088 | |||
Дипана® | Таблетки, покрытые оболочкой рег. №: ЛС-001751 | |||
Желчегонный сбор №3 | Сбор растительный — сырье измельченное: пакчка 50 г рег. №: ЛП-000498 | |||
Имунофан | Спрей назальный дозир. 50 мкг/1 доза: фл. 40 доз с дозирующим устройством рег. №: ЛС-002646 | |||
Имунофан | Суппозитории ректальные 100 мкг: 5 шт. рег. №: Р N000106/04 | |||
Ингарон® | Лиофилизат д/пригот. р-ра д/в/м и п/к введения 1 млн.МЕ: фл. 1, 5,10 или 20 шт. рег. №: ЛС-000924 Лиофилизат д/пригот. р-ра д/в/м и п/к введения 2 млн.МЕ: фл. 1, 5,10 или 20 шт. рег. №: ЛС-000924 Лиофилизат д/пригот. р-ра д/в/м и п/к введения 100 тыс.МЕ: фл. 1, 5,10 или 20 шт. рег. №: ЛС-000924 Лиофилизат д/пригот. р-ра д/в/м и п/к введения 500 тыс.МЕ: фл. 1, 5,10 или 20 шт. рег. №: ЛС-000924 | |||
Кукурузы столбики с рыльцами | Сырье растительное измельченное: пачки 30 г или 50 г рег. №: ЛП-000287 | |||
Кукурузы столбики с рыльцами | Сырье растительное цельное: пачки 30 г, 35 г или 40 г рег. №: ЛП-000432 | |||
Лайфферон® | Лиофилизат д/пригот. р-ра д/в/м, субконъюнктивального введ. и закапывания в глаз 1 млн.МЕ: амп. 5 или 10 шт., фл. 5 шт. рег. №: ЛС-001989 Лиофилизат д/пригот. р-ра д/в/м, субконъюнктивального введ. и закапывания в глаз 3 млн.МЕ: амп. 5 или 10 шт., фл. 5 шт. рег. №: ЛС-001989 Лиофилизат д/пригот. р-ра д/в/м, субконъюнктивального введ. и закапывания в глаз 5 млн.МЕ: амп. 5 или 10 шт., фл. 5 шт. рег. №: ЛС-001989 Лиофилизат д/пригот. р-ра д/в/м, субконъюнктивального введ. и закапывания в глаз 500 тыс.МЕ: амп. 5 или 10 шт., фл. 5 шт. рег. №: ЛС-001989 | |||
Лайфферон® | Р-р д/в/м, субконъюнктивального введ. и закапывания в глаз 1 млн.МЕ: амп. 5 или 10 шт., фл. 5 шт. рег. №: ЛСР-000091 Р-р д/в/м, субконъюнктивального введ. и закапывания в глаз 3 млн.МЕ: амп. 5 или 10 шт., фл. 5 шт. рег. №: ЛСР-000091 Р-р д/в/м, субконъюнктивального введ. и закапывания в глаз 5 млн.МЕ: амп. 5 или 10 шт., фл. 5 шт. рег. №: ЛСР-000091 Р-р д/в/м, субконъюнктивального введ. и закапывания в глаз 500 тыс.МЕ: амп. 5 или 10 шт., фл. 5 шт. рег. №: ЛСР-000091 | |||
ЛИВ. 52® | Капли д/приема внутрь: фл. 60 мл в компл. с пипеткой-дозатором рег. №: ЛСР-009411/09 Таб.: 100 шт. рег. №: П N014783/01 | |||
Ливенциале | Раствор для в/в введения рег. №: ЛП-002728 Дата перерегистрации: 09.11.18 | Произведено и расфасовано: SCAN BIOTECH (Индия) | ||
Мавирет | Таблетки, покрытые пленочной оболочкой рег. №: ЛП-004804 Дата перерегистрации: 26.09.19 | Вторичная упаковка и выпускающий контроль качества: AbbVie Deutshland (Германия) ОРТАТ (Россия) | ||
Максар | Таблетки, покрытые пленочной оболочкой рег. №: Р N003294/01 | |||
Метионин | Таб., покр. пленочной оболочкой, 250 мг: 10, 20 или 50 шт. рег. №: ЛС-001209 | |||
Метипред | Таб. 4 мг: 30 или 100 шт. рег. №: П N015709/01 Дата перерегистрации: 14.09.20 Таб. 16 мг: 30 или 100 шт. рег. №: П N015709/01 Дата перерегистрации: 14.09.20 | Произведено и расфасовано: ORION CORPORATION (Финляндия) | ||
ПегАльтевир | Лиофилизат д/пригот. р-ра д/п/к введения 50 мкг: фл. в компл. с растворителем рег. №: ЛП-002542 Лиофилизат д/пригот. р-ра д/п/к введения 80 мкг: фл. в компл. с растворителем рег. №: ЛП-002542 Лиофилизат д/пригот. р-ра д/п/к введения 100 мкг: фл. в компл. с растворителем рег. №: ЛП-002542 Лиофилизат д/пригот. р-ра д/п/к введения 120 мкг: фл. в компл. с растворителем рег. №: ЛП-002542 Лиофилизат д/пригот. р-ра д/п/к введения 150 мкг: фл. в компл. с растворителем рег. №: ЛП-002542 | |||
Пегасис® | Р-р д/п/к введения 135 мкг/0.5 мл: шприц-тюбики 1 шт. в компл. с иглой д/и стерильной рег. №: П N013704/01 Р-р д/п/к введения 135 мкг/0.5 мл: автоинжектор ПроКлик™ рег. №: П N013704/01 Р-р д/п/к введения 180 мкг/0.5 мл: автоинжектор ПроКлик™ рег. №: П N013704/01 Р-р д/п/к введения 180 мкг/0.5 мл: шприц-тюбики 1 шт. в компл. с иглой д/и стерильной рег. №: П N013704/01 | |||
Полифан | Порошок д/приема внутрь 1 кг: пак. рег. №: Р N001944/01 | |||
Полифан | Порошок д/приема внутрь 100 г: пак. рег. №: Р N001944/01 | |||
Полифан | Порошок д/приема внутрь 500 г: пак. рег. №: Р N001944/01 | |||
Полифепан | Гранулы д/приема внутрь 100 г: банки рег. №: Р N001047/03 | |||
Полифепан | Гранулы д/приема внутрь 50 г: пачки 1 или 10 шт. рег. №: Р N001047/03 | |||
Полифепан | Таб. 375 мг: 30, 50, 100 или 200 шт. рег. №: Р N001047/04 | |||
Полифепан® | Порошок д/приема внутрь: 10 г, 50 г, 100 г, 200 г или 250 г пак. рег. №: ЛП-005878 | |||
Полькортолон | Таб. 4 мг: 50 шт. рег. №: П N013540/01 | |||
Преднизолон | Таб. 5 мг: 100 шт. рег. №: ЛС-001000 | |||
Преднизолон | Таб. 5 мг: 20, 30, 50 или 60 шт. рег. №: ЛП-000773 | |||
Пробифор® | Капс. 500 млн.КОЕ: банки 6, 10, 18 или 30 шт. рег. №: ЛС-002558 Дата перерегистрации: 03.06.20 Порошок д/приема внутрь 500 млн.КОЕ: пак. 6, 10 или 30 шт. рег. №: Р N000090/01 Дата перерегистрации: 04.06.20 Капс. 500 млн.КОЕ: фл. 6, 10, 18 шт. рег. №: ЛС-002558 Дата перерегистрации: 03.06.20 | |||
Прогепар® | Таблетки, покрытые оболочкой рег. №: ЛСР-005848/08 Дата перерегистрации: 12.07.17 | |||
Реаферон-ЕС | Лиоф. д/пригот. р-ра д/инъекц. и местного прим. 1 млн.МЕ: амп. 5 или 10 шт. фл. 5 шт. рег. №: Р N000642/01 Лиоф. д/пригот. р-ра д/инъекц. и местного прим. 3 млн.МЕ: амп. 5 или 10 шт., фл. 5 шт. рег. №: Р N000642/01 Лиоф. д/пригот. р-ра д/инъекц. и местного прим. 5 млн.МЕ: амп. 5 или 10 шт., фл. 5 шт. рег. №: Р N000642/01 Лиоф. д/пригот. р-ра д/инъекц. и местного прим. 500 тыс.МЕ: амп. 5 или 10 шт., фл. 5 шт. рег. №: Р N000642/01 | |||
Револейд | Таб., покр. пленочной оболочкой, 25 мг: 28 шт. рег. №: ЛСР-010032/09 Дата перерегистрации: 29.09.15 Таб., покр. пленочной оболочкой, 50 мг: 28 шт. рег. №: ЛСР-010032/09 Дата перерегистрации: 29.09.15 | |||
Ремаксол® | Раствор для инфузий рег. №: ЛСР-009341/09 Дата перерегистрации: 13.02.20 | |||
Реосорбилакт® | Раствор для инфузий рег. №: ЛСР-003845/08 | |||
Рибавирин-Липинт® | Лиофилизат д/пригот. суспензии д/приема внутрь 500 мг: фл. 1 или 6 шт. рег. №: ЛП-000634 | |||
Рибавирин-СЗ | Капс. 200 мг: 30, 60 или 120 шт. рег. №: ЛСР-006932/10 Дата перерегистрации: 15.08.18 | |||
Ропрен® | Капли д/приема внутрь: фл. 4 г или 8 г в компл. с крышками-капельницами рег. №: ЛСР-001521/07 | Официальный дистрибьютор на территории РФ: БИОФАР (Россия) | ||
Роферон®-А | Р-р д/п/к введения 3 млн.МЕ/0.5 мл: шприц-тюбик 1 шт. рег. №: П N014755/01 Р-р д/п/к введения 4.5 млн.МЕ/0.5 мл: шприц-тюбик 1 шт. рег. №: П N014755/01 Р-р д/п/к введения 6 млн.МЕ/0.5 мл: шприц-тюбик 1 шт. рег. №: П N014755/01 Р-р д/п/к введения 9 млн.МЕ/0.5 мл: шприц-тюбик 1 шт. рег. №: П N014755/01 | |||
Сибектан® | Таблетки рег. №: Р N001213/01 | |||
Силимар® | Таблетки рег. №: ЛСР-006595/08 Дата перерегистрации: 05.06.17 | |||
Совриад® | Капсулы рег. №: ЛП-002384 | |||
Тиотриазолин® | Р-р д/в/в и в/м введения 50 мг/ 2 мл: амп. 10 шт. рег. №: ЛСР-002170/10 Р-р д/в/в и в/м введения 100 мг/4 мл: амп. 10 шт. рег. №: ЛСР-002170/10 | |||
Тиотриазолин® | Таб. 100 мг: 30 или 50 шт. рег. №: ЛСР-002165/10 | |||
Триворин | Капс. 200 мг: 12, 18, 21, 42, 60, 120, 150 или 180 шт. рег. №: ЛС-000444 Капс. 400 мг: 12, 18, 21, 42, 60, 120, 150 или 180 шт. рег. №: ЛС-000444 | Произведено: LEMERY (Мексика) контакты: (Израиль) | ||
Тыквеол® | Масло д/приема внутрь: фл.100 мл рег. №: Р N002321/03 Капс. 450 мг: 10, 20, 30, 50, 84, 90 или 180 шт. рег. №: Р N002321/01 Супп. ректальные 500 мг: 10 шт. рег. №: Р N002321/02 Дата перерегистрации: 28.06.19 | |||
Урсодез® | Капс. 250 мг: 40, 50, 60, 90, 100 или 120 шт. рег. №: ЛСР-004408/10 Дата перерегистрации: 16.04.19 | |||
Урсодез® | Капс. 500 мг: 10, 30 или 50 шт. рег. №: ЛП-003238 Дата перерегистрации: 29.04.19 | |||
Урсосан® форте | Капс. 250 мг: 10, 50, 60 или 100 шт. рег. №: П N016302/01 Дата перерегистрации: 03.03.20 Таб., покр. пленочной оболочкой, 500 мг: 10, 50 или 100 шт. рег. №: ЛП-003388 | |||
Флогэнзим | Таблетки кишечнорастворимые, покрытые пленочной оболочкой рег. №: П N012753/01 Дата перерегистрации: 22.08.17 | |||
Фосфоглив® | Капс.: 50 шт. рег. №: Р N002528/01 Дата перерегистрации: 09.01.19 | |||
Фосфоглив® | Лиофилизат д/пригот. р-ра д/в/в введения: фл. 2.5 г 5 шт. в компл. с растворителем рег. №: Р N002528/02 Дата перерегистрации: 18.05.17 | |||
Фосфоглив® Форте | Капсулы рег. №: ЛСР-008120/08 Дата перерегистрации: 10.10.17 | |||
Фосфонциале® | Капсулы рег. №: ЛСР-006426/08 Дата перерегистрации: 07.07.20 | |||
Хофитол | Р-р д/приема внутрь 20 г/100 мл: фл. 120 мл рег. №: П N013320/02 Таб., покр. оболочкой, 200 мг: 60 или 180 шт. рег. №: П N013320/01 | |||
Циклоферон® | Р-р д/в/в и в/м введения 125 мг/1 мл: амп. 2 мг 5 шт. рег. №: Р N001049/03 Дата перерегистрации: 09.11.18 | |||
Цитохром C | Лиофилизат для приготовления раствора для в/в и в/м введения рег. №: ЛСР-008117/08 Дата перерегистрации: 11.03.20 | |||
Энтеросгель® | Паста д/приема внутрь: пак. 22.5 г 2, 10 или 20 шт.; тубы 225 г 1 шт. рег. №: ЛП-N (000036)-(РГ- RU) | |||
Энтерумин | Порошок д/пригот. суспензии д/приема внутрь 5 г: пакеты 10 или 20 шт. рег. №: ЛСР-004123/09 Порошок д/пригот. суспензии д/приема внутрь 10 г: пакеты 10 или 20 шт. рег. №: ЛСР-004123/09 | |||
Эпклюза® | Таблетки, покрытые пленочной оболочкой рег. №: ЛП-005703 Дата перерегистрации: 28.11.19 | |||
Эссенциале® Н | Раствор для в/в введения рег. №: П N016326/01 Дата перерегистрации: 12.12.16 | |||
Эссенциале® форте Н | Капсулы рег. №: П N011496/01 Дата перерегистрации: 17.02.20 | |||
Эссенциальные фосфолипиды | Р-р д/в/в введения 50 мг/1 мл: амп. 5 мл 5, 10, 250 или 500 шт. рег. №: ЛП-000605 Дата перерегистрации: 19.10.16 | |||
Виктрелис | Капсулы рег. №: ЛП-002070 Дата перерегистрации: 30.06.15 | |||
Гепасол А | Раствор для инфузий рег. №: П N015495/01 | |||
Декстроза | Р-р д/инф. 10%: бут. или фл. 100 мл рег. №: ЛП-000161 | |||
Декстроза | Р-р д/инф. 5%: бут. или фл. 100 мл рег. №: ЛП-000161 | |||
Инсиво | Таблетки, покрытые пленочной оболочкой рег. №: ЛП-001931 | |||
Интераль-П | Лиофилизат д/пригот. р-ра д/инъекц. 1 млн.МЕ: амп. 5 шт. рег. №: Р N000697/01 | |||
Интераль-П | Лиофилизат д/пригот. р-ра д/инъекц. 3 млн.МЕ: амп. 5 или 10 шт. рег. №: Р N000697/01 | |||
Интераль-П | Лиофилизат д/пригот. р-ра д/инъекц. 5 млн.МЕ: амп. 5 или 10 шт. рег. №: Р N000697/01 | |||
Интераль-П | Лиофилизат д/пригот. р-ра д/инъекц. 500 тыс.МЕ: амп. 5 или 10 шт. рег. №: Р N000697/01 | |||
Реальдирон® | Лиофилизат д/пригот. р-ра д/в/м и п/к введен. 1 млн.МЕ: амп. 5 шт. рег. №: П N012808/01 | Произведено: LEMERY (Мексика) | ||
Реальдирон® | Лиофилизат д/пригот. р-ра д/в/м и п/к введен. 1 млн.МЕ: фл. 5 шт. рег. №: П N012808/01 | Произведено: LEMERY (Мексика) | ||
Реальдирон® | Лиофилизат д/пригот. р-ра д/в/м и п/к введен. 18 млн.МЕ: амп. 5 шт. рег. №: П N012808/01 | Произведено: LEMERY (Мексика) | ||
Реальдирон® | Лиофилизат д/пригот. р-ра д/в/м и п/к введен. 18 млн.МЕ: фл. 5 шт. рег. №: П N012808/01 | Произведено: LEMERY (Мексика) | ||
Реальдирон® | Лиофилизат д/пригот. р-ра д/в/м и п/к введен. 3 млн.МЕ: амп. 5 шт. рег. №: П N012808/01 | Произведено: LEMERY (Мексика) | ||
Реальдирон® | Лиофилизат д/пригот. р-ра д/в/м и п/к введен. 3 млн.МЕ: фл. 5 шт. рег. №: П N012808/01 | Произведено: LEMERY (Мексика) | ||
Реальдирон® | Лиофилизат д/пригот. р-ра д/в/м и п/к введен. 5 млн.МЕ: амп. 5 шт. рег. №: ЛСР-001492/08 | Произведено: LEMERY (Мексика) | ||
Реальдирон® | Лиофилизат д/пригот. р-ра д/в/м и п/к введен. 5 млн.МЕ: фл. 5 шт. рег. №: ЛСР-001492/08 | Произведено: LEMERY (Мексика) | ||
Реальдирон® | Лиофилизат д/пригот. р-ра д/в/м и п/к введен. 6 млн.МЕ: амп. 5 шт. рег. №: П N012808/01 | Произведено: LEMERY (Мексика) | ||
Реальдирон® | Лиофилизат д/пригот. р-ра д/в/м и п/к введен. 6 млн.МЕ: фл. 5 шт. рег. №: П N012808/01 | Произведено: LEMERY (Мексика) | ||
Реальдирон® | Лиофилизат д/пригот. р-ра д/в/м и п/к введен. 9 млн.МЕ: амп. 5 шт. рег. №: П N012808/01 | Произведено: LEMERY (Мексика) | ||
Реальдирон® | Лиофилизат д/пригот. р-ра д/в/м и п/к введен. 9 млн.МЕ: фл. 5 шт. рег. №: П N012808/01 | Произведено: LEMERY (Мексика) | ||
Сунвепра® | Капсулы мягкие рег. №: ЛП-003022 Дата перерегистрации: 09.11.18 | Фасовка, упаковка и выпускающий контроль качества: ANDERSONBRECON (США) | ||
Эрбисол® | Раствор для инъекций рег. №: ЛС-000437 | Официальный дистрибьютор в РФ: ФК ПУЛЬС (Россия) | ||
Применение фосфоглива при острых и хронических вирусных гепатитах у детей Текст научной статьи по специальности «Клиническая медицина»
Вопросы терапии
Применение фосфоглива при острых и хронических вирусных гепатитах у детей
В. ф. Учайкин, О. Б. Ковалев
ГОУ ВПО Российский государственный медицинский университет Росздрава, Москва
Фосфоглив получали более 350 больных: 236 — энтерально при острых заболеваниях печени — 2—4 недели, а при хронических — 6—12 месяцев. Инъекционную форму Фосфоглива вводили 122 больным с проявлениями печеночной недостаточности. Фосфоглив при острых гепатитах А и В у детей способствует снижению симптомов интоксикации, сокращению размеров печени, нормализации уровня билирубина и активности АлАТ, сокращает сроки пребывания больных в стационаре. Фосфоглив для внутривенных инъекций также обладает высокой эффективностью. Лечение Фос-фогливом также получали 37 больных ХГ (29 — с ХГС и 8 — с ХГВ) в комбинации с вифероном. Группу сравнения составили 104 больных (70 — ХГС и 34 — ХГВ), лечившиеся только вифероном (I группа), и 39 детей (у 27 — ХГВ, у 12 — ХГС) на базисной терапии (II группа). Полная ремиссия отмечалось в 34% случаев, неполная — в 38% и только у трети больных (28%) ремиссия отсутствовала. При ХГВ первичная ремиссия отмечена у 4 из 8 больных (50%). В I группе сравнения у больных ХГС на монотерапии вифероном первичная полная ремиссия наблюдалась у 39%, биохимическая — у 17% и отсутствие эффекта — у 44%. У больных ХГВ — 66%, 12% и 22% соответственно. Во II группе детей полной ремиссии не было. Фосфоглив хорошо переносится детьми. Побочных реакций не отмечалось. Ключевые слова: фосфоглив, рекомбинантный интерферон-альфа, острые и хронические вирусные гепатиты, терапия, дети
В настоящее время вирусные гепатиты представляют серьезную угрозу здоровью людей из-за высокого риска формирования хронического процесса с исходом в цирроз и гепатоцеллюлярную карциному. Удельный вес больных и инфицированных вирусными гепатитами остается угрожающе высоким и составляет во многих регионах страны до 10% и более. Прежде всего высок процент в группах риска: наркоманы, токсикоманы, ВИЧ-инфицированные, больные онкогемато-логическими заболеваниями, пациенты гемодиализных центров. Безусловно, решение проблемы вирусных гепатитов лежит на пути массовой вакцинопрофилактики. Но приходится констатировать, что в настоящий момент можно вести речь только о вакцинации против гепатита В, поскольку вакцин против других гепатитов (С, О, Е, С), в динамике течения которых формируются неблагоприятные исходы, нет, и создание их в ближайшей перспективе маловероятно из-за высокой изменчивости вирусов.
Все эти факторы переносят акцент борьбы с вирусными гепатитами в плоскость создания лекарственных средств, которые позволили бы, с одной стороны, достаточно эффективно лечить, а с другой стороны про-филактировать неблагоприятные исходы вирусных заболеваний печени.
Следует отметить, что для лечения заболеваний печени до настоящего времени не созданы достаточно эффективные лекарственные средства. Среди средств, применяемых для этих целей (эссенциале, гептрал, легалон, кортикостероиды, аминокислотные коктейли и т. д.) нет безусловно эффективных, во всяком случае ни один из существующих гепатотропных препаратов не отвечает принципу доказательной медицины.
Исключение, по всей видимости, составляют только рекомбинантные интерфероны. Доказано, что у больных хроническими гепатитами В и С (ХГВ и ХГС), леченных вифероном, интроном-А, рофероном-А и другими препаратами интерферона-альфа, снижается активность процесса в печени и подавляется репликация вируса [1—3]. Однако клинический эффект наблюдается не у всех больных: не более 50% при ХГВ, и около 25% при ХГС. Более того, даже в случаях до-
стигнутого эффекта после прекращения лечения высока вероятность обострения патологического процесса.
В детской практике применение парентеральных рекомбинантных интерферонов ограничено из-за частых тяжелых побочных эффектов. Низкая терапевтическая эффективность лекарственных препаратов при заболеваниях печени объясняется невозможностью их преодолевать гепатоцеллюлярные мембраны. Это выдвигает на первый план проблему конструирования лекарств по принципиально новой технологии (нанотех-нологии) с целью создания микросфер с диаметром меньше, чем диаметр каналов в липидном бислое ге-патоцитов.
Такой подход был реализован при создании нового отечественного гепатопротектора с противовирусной активностью — фосфоглива для инъекций.
Фосфоглив представляет собой комбинированный препарат, содержащий фосфатидилхолин и тринатрие-вую соль глицирризиновой кислоты. В одной капсуле препарата содержится 0,065 г фосфатидилхолина и 0,035 г тринатриевой соли глицирризиновой кислоты.
Механизм действия фосфоглива складывается из двух составляющих. Первая — аналогична действию препарата «Эссенциале» (Германия). Содержащийся в нем соевый фосфатидилхолин восстанавливает поврежденные мембраны клеток, действуя на имеющиеся в них дефекты как «мембранный клей». Вторая — аналогична действию препарата «Нео-Минофаген С» (SNMC, Япония), основу которого составляет глицир-ризиновая кислота, которая, как известно, является синергистом кортикостероидных гормонов, активирует макрофаги, обладает антиаллергическими и противовирусными свойствами, антиоксидантной и иммуномо-дулирующей активностью. Противовирусное действие глицирризиновой кислоты объясняется способностью ее модулировать иммунные свойства и индуцировать Y-интерферон [4].
В литературе достаточно широко представлена эффективность при хронических вирусных гепатитах глицир-ризиновой кислоты в виде Нео-Минофагена С (SNMC). Так, Abe Y. с соавт. [5] проводили лечение Нео-Мино-фагеном С у больных с ХГС, «не ответивших» на мо-
нотерапию интерфероном. 15 больных продолжали получать интерферон (I группа), а 13 пациентов — интерферон вместе с Нео-Минофагеном С внутривенно в течение 12 недель (II группа). Нормализация уровня АлАТ в сыворотке крови выявлена у 33,3% больных I группы и 64,3% — II группы. Исчезновение PHK-HCV определялось в 13,3 и 38,5% соответственно.
Richard N. Podell [6] наблюдал 193 больных с ХГС (у всех была выявлена гиперферментемия и проводилась пункционная биопсия печени), которые не получали интерфероны, гормональные препараты и имму-носупрессанты. Из них 84 (I группа) проводилась внутривенная терапия Нео-Минофагеном С 2—7 раз в неделю в среднем в течение 10 лет. Другие 109 больных (II группа) получали различные препараты растительного происхождения (витамин К). По окончании терапии у 36% больных первой группы сохранялся уровень печеночных ферментов в пределах нормальных величин, а во второй группе этот показатель был равен 6%. В течение 10 лет наблюдения гепатоцеллюляр-ная карцинома была выявлена у 7% больных I группы и 12% — II группы, через 15 лет — 12 и 25% соответственно (р < 0,05). Цирроз печени выявлялся через 10 лет у 12 и 20%, а через 15 лет — у 21 и 37% больных I и II групп соответственно.
Лечение фосфогливом получили более 350 больных, в том числе 236 больных принимали препарат энтерально в виде капсул по схеме: курс лечения при острых заболеваниях составил 2—4 недели, а при хронических — 6—12 месяцев. Взрослым фосфоглив назначался по 2 капсулы 3—4 раза в сутки во время еды. Детям в возрасте до 3 лет фосфоглив назначался в дозе 1/2 капсулы 3 раза в сутки, от 3 до 7 лет — 1 капсула 3 раза в сутки, старше 7 лет — 2 капсулы 3 раза в сутки.
Лечение инъекционной формой фосфоглива проводилось у 122 больных с различными видами и с различной степенью выраженности печеночной недостаточности, в том числе с острым вирусным гепатитом В (ОГВ) — 21; с хроническим гепатитом С (ХГС) — 53; с хроническими микст гепатитами В и С (ХГВ и С) — 10; с хроническим гепатитом В (ХГВ) — 3; с циррозом печени — 17, в том числе 7 больных с циррозом вирусной этиологии и 10 — с алиментарным циррозом; с гепатитом алиментарной этиологии — 6; со стеато-гепатитом — 4; с печеночной недостаточностью в качестве сопутствующего диагноза, госпитализированных по поводу других заболеваний (дерматозов и бронхолегочных обострений) — 7.
В качестве контрольных групп анализировались 80 больных — по 20 человек с ХГС и ХГВ и С и 2 группы (по 20 больных) с ОГВ.
Фосфоглив вводили по схеме: 2,5 г в 10 мл апиро-генной воды капельно 2 раза в день.
Лечение проводилось на фоне «базисной терапии», которую получали и больные контрольных групп.
После окончания внутривенного курса часть пациентов (в основном с ОГВ) получала фосфоглив в капсулах — по 2 капсулы 3 раза в день в течение 20—30 дней и 3—6 месяцев при хронической форме заболевания.
Во всех группах больных, получавших фосфоглив, наблюдалась положительная динамика клинических симптомов.
Хороший и удовлетворительный эффект от применения фосфоглива при остром гепатите В отмечался в среднем у 94% больных, а при хроническом гепатите С — в 83% случаев, при микст гепатите — у 78%.
Положительные сдвиги были отмечены и при сравнении биохимических показателей. У больных, получавших фосфоглив, уровень общего билирубина был достоверно более низким после окончания лечения по сравнению с контрольной группой — 39 ± 5,6 и 83 ± 20 мкм/л соответственно. Во всех группах больных, после окончания курса лечения зарегистрированы достоверно более низкие значения АлАТ по сравнению с контрольными группами (так, в случае ХГС — 96 ± 24,9 и 278 ± 73 ед/л соответственно), при этом при гепатите В также достоверно ниже были показатели АсАТ (95 ± 19,3 и 533 ± 195 ед/л соответственно) и гаммаглютамилт-ранспептидазы (ГГТП) (68,6 ± 6 и 98 ± 12 ед/л соответственно), а при гепатите С — уровни щелочной фосфатазы (125 ± 11 и 254 ± 30 ед/л соответственно) и ГГТП (47 ± 4 и 12 ± 19 соответственно).
У леченных фосфогливом достоверно снижалась вирусная нагрузка (рис. 1, 2).
Таким образом, у больных, леченных фосфогли-вом, положительная динамика (нормализация и улучшение биохимических показателей) была зарегистрирована в 77% случаев при гепатите В, у 74% больных с ХГС и у 78% — с микст гепатитами В и С.
Строго по протоколу исследовалась эффективность фосфоглива в клинике академика РАМП, профессора Г. И. Сторожакова [5]: 20 больных ХГС получали лечение фосфогливом изолированно, 19 — фосфогливом в комбинации с рекомбинантным ИфН-альфа внутримышечно, 20 — только рекомбинантным ИФН-альфа и 20 — лечились рекомбинантным ИФН-альфа в комбинации с рибавирином. Лечение проводилось во всех группах в течение 12 мес. фосфоглив назначался из
3 У
2,5 — у ✓
2 — у
1,5 ■ у
1 ■ у
0,5 — у
0 — у
до лечения после лечения
3 1 У
2,5- У
2 — У
1,5- У У
0,5- У
0 — У
до лечения после лечения
Рйсунок 1. Динамика РНК НСУ при лечении фосфогливом больных ХГС (в 1_д титров) (3-х месячный курс)
Рисунок 2. Динамика ДНК НВУ при лечении фосфогливом у больных ХГВ (в 1_д титров) (3-х месячный курс)
расчета 2,5 г в/в 2 раза в неделю плюс 600 мг/сутки per os, ИфН-альфа — 3 ME 3 раза в неделю.
Первичная полная ремиссия отмечена у 40% больных, леченных только фосфогливом и у 57,9% — фос-фогливом и ИфН-альфа. В остальных случаях имело место улучшение и только у 1 больного эффект отсутствовал. Принципиально важно, что у больных, леченных фосфогливом, побочные эффекты практически не встречались, тогда как среди леченных интерферо-ном-альфа гриппоподобный синдром наблюдался в 90%, лейкопения — у 45%, тромбоцитопения — у 10%, снижение веса — у 35%, тиреоидная дисфункция — у 25%, депрессия — у 30%.
У больных, леченных фосфогливом, отмечалось резкое снижение вирусной нагрузки. После окончания курса лечения РНК HCV не выявлялась у 8 из 20 больных, леченных фосфогливом (40%), у 11 из 19 леченных фосфогливом с ИфН-альфа (57,9%), у 8 из 20 получавших только ИфН-альфа (40%) и у 15 из 20 — ИфН-альфа с рибавирином (75%).
Представленные данные свидетельствуют о способности фосфоглива подавлять репликационную активность HCV и HBV за счет глицирризиновой кислоты, обладающей противовирусным действием.
Существенным признаком улучшения системы иммунитета после лечения фосфогливом явилось возрастание у большинства больных количества естественных киллеров и у-интерферона (рис. 3). У некоторых больных было установлено увеличение синтеза а-ин-терферона.
Выраженных побочных реакций на введение фос-фоглива не было. Однако у 2 больных отмечались аллергические высыпания на коже, которые купировались применением антигистаминных препаратов. У одной больной отмечалось повышение артериального давления до 150/90 мм рт. ст. на фоне лечения фос-фогливом. После окончания курса парентеральной терапии фосфогливом и переходе на энтеральную форму артериальное давление полностью нормализовалось.
Таким образом, проведенное клиническое исследование показало, что фосфоглив для внутривенных инъекций обладает высокой эффективностью при лечении заболеваний печени различной этиологии. Внутривенная форма препарата хорошо переносится больными, не дает побочных реакций и приводит к заметному улучшению их общего состояния, а также лабораторных показателей. Отмечено позитивное
$) пкг/мл
1000 750 500 250 0
.у
.У
-V
до после лечения лечения
до после лечения лечения
Рисунок 3. Влияние терапии фосфогливом на синтез гамма-интерферона (а) и активность естественных киллеров (б) у больных хроническими вирусными гепатитами
влияние препарата на репликативную активность вирусов гепатитов В и С, а также на иммунный и интерфе-роновый статусы, что позволяет рекомендовать его для использования в лечении хронических вирусных гепатитов, а возможно, в дальнейшем, и некоторых других заболеваний вирусной этиологии.
В данном сообщении мы считаем целесообразным поделиться первым опытом лечения фосфогливом острого и хронического вирусного гепатита у детей.
Проблема лечения вирусных гепатитов остается наиболее трудной в детской гепатологии, где терапия препаратами рекомбинантного альфа-интерферона часто бывает невозможна из-за высокого риска осложнений, и, кроме того, нет разрешающих документов на применение альфа-интерферона с рибавирином и другими препаратами у детей.
Материалы и методы исследования
Лечение фосфогливом получали 12 больных острым гепатитом А (ОГА) и 15 больных острым гепатитом В (ОГВ) дополнительно к базисной терапии. Группу контроля составили 14 больных с ОГА и 13 — с ОГВ. Препарат давали детям до 7 лет в дозе 1/2 табл. 3 раза в день, старше 7 лет — по 1 табл. 3 раза в день. Дети в сравниваемых группах были одного возраста, имели одинаковую форму тяжести заболевания, находились в одних и тех же условиях режима и получали одинаковую базисную терапию. Клинико-ла-бораторные показатели оценивали до лечения, на 10 и 20 дни лечения. Статистическая обработка полученных результатов проводилась с помощью критерия Стъюдента.
Под наблюдением также находилось 180 детей в возрасте от 6 мес. до 14 лет, больных хроническим гепатитом (ХГ), подтвержденным у большинства данными пункционной биопсии печени. Методом иммуно-ферментного анализа (ИфА) и полимеразной цепной реакции (ПЦР) у 73 детей был установлен ХГВ и у 107 — ХГС. Все дети находились в стадии обострения болезни.
Лечение фосфогливом получали 37 больных (29 — с ХГС и 8 — с ХГВ) в комбинации с рекомбинантным интерфероном альфа-2Ь — вифероном в свечах (основная группа).
Группу сравнения составили 104 больных (70 — ХГС и 34 — ХГВ) получавшие монотерапию вифероном (I группа), и 39 детей ( у 27 — ХГВ , у 12 — ХГС), находившихся на симптоматической базисной терапии (диета, режим, желчегонные препараты, поливитамины) (II группа).
Показанием к назначению комбинированной терапии явилась констатация хронического гепатита В или С, сопровождающегося длительным (более года) повышением активности АлАТ и АсАТ с обнаружением маркеров активной репликации вирусов гепатита В (ДНК НВУ, НВеАд) и гепатита С (РНК НСУ).
Критериями эффективности терапии были: биохимические — активность АлАТ, которая определялась ежемесячно в ходе лечения и в течение 6 мес. после окончания терапии, затем каждые 6 мес. на протяжении 36 мес.; вирусологические — РНК НСУ и ДНК НВУ — качественный и количественный методы;
Таблица 1. Динамика некоторых биохимических показателей крови у больных ОГА на фоне лечения фосфогливом (основная группа, п = 12) и на фоне базисной терапии (группа сравнения, п =14)
Биохимические показатели До лечения 10 день лечения 20 день лечения
Основная группа Группа сравнения Р Основная группа Группа сравнения Р Основная группа Группа сравнения Р
Билирубин общий (мкм/л) 53,6 ± 6,4 56,4 ± 1,6 > 0,05 18,1 ± 1,7 25,5 ± 2,1 *< 0,05 9,5 ± 0,1 20,1 ± 1,9 *< 0,05
Билирубин конъюгир. (мкм/л) 39,6 ± 5,5 40,6 ± 2,1 > 0,05 9,2 ± 1,4 14,3 ± 1,8 *< 0,05 3 ± 0,1 6,5 ± 1,1 *< 0,05
АлАТ (ед/л) 1249,7 ± 207 1623 ± 371 > 0,05 197,8 ± 21,5 265,8 ± 22 *< 0,05 43 ± 2,4 52 ± 3,1 *< 0,05
АсАт (ед/л) 646,4 ± 140 1875 ± 247 > 0,05 95,6 ± 23 80 ± 4,0 > 0,05 39 ± 1,3 43 ± 1,8 *< 0,05
Щелочная фос-фатаза (ед/л) 552 ± 27,2 507 ± 34,7 > 0,05 249 ± 23,1 276 ± 3,9 > 0,05 291 ± 4,2 243 ± 5,6 *< 0,05
Тимоловая проба (ед) 15,4 ± 1,5 15,7 ± 0,9 > 0,05 13,8 ± 1,1 17,4 ± 1,5 > 0,05 16,6 ± 2,2 14,9 ± 2,2 > 0,05
* — различие достоверно при р < 0,05 между основной и контрольными группами
гистологические — положительная динамика по данным биопсии печени с использованием индекса гистологической активности.ОНЕР». Различали первичную ремиссию — два последовательных нормальных значения уровня АлАТ в процессе лечения, ближе к концу, с интервалом не менее 2 недель, исчезновение РНК НСУ или ДНК НВУ к концу терапии; стабильную ремиссию — нормальная АлАТ, отсутствие РНК НСУ или ДНК НВУ в течение 6 мес. после окончания терапии; длительную ремиссию — нормальная АлАТ, отсутствие РНК НСУ или ДНК НВУ в течение 24 мес. после окончания терапии; прекращение ремиссии в ходе лечения («ускользание») — в течение 6 мес. терапии после нормализации АлАТ ее уровень вновь повысился (два последовательных анализа с интервалом 2 недели), и/или повторное появление РНК НСУ или ДНК НВУ в любой точке времени после ее исчезновения; отсутствие ремиссии — любая другая динамика активности АлАТ и наличие РНК НСУ или ДНК НВУ к окончанию терапии.
Фосфоглив назначался детям до 3 лет по 1/2 капсуле, от 3 до 7 лет по 1 капсуле, от 7 лет — по 1 1/2 капсуле 3 раза в день. Виферон больные получали из расчета 3 млн МЕ/м2 площади поверхности тела 3 раза в неделю. Лечение продолжалось 6 или 9 мес.
Результаты и их обсуждение
Результаты проведенных исследований при острых вирусных гепатитах представлены в табл. 1 и 2 и рис. 4—6.
У больных, леченных фосфогливом, на 10 день от начала терапии, быстрее, чем у больных в группе контроля, уменьшалась желтуха, сокращались размеры печени, в сыворотке крови снижалось содержание общего и, особенно, конъюгированного билирубина, уменьшалась активность АлАТ и, в меньшей степени АсАТ. Показатели щелочной фосфатазы и тимоловой пробы также были лучше, чем в группе контроля, однако эти различия были недостоверными.
На 20 день от начала терапии у всех детей, леченных фосфогливом, желтуха отсутствовала, тогда как в группе контроля у 7 детей из 13 с гепатитом В еще сохранялась легкая иктеричность склер. Размеры печени в эти сроки в группе больных ГА были в пределах нор-
мкмоль/л
контроль
до лечения
мкмоль/л 60-, 56
5040 30 20100
фосфоглив норма
до лечения
10 день лечения
20 день лечения
Рисунок 4. Динамика общего билирубина у детей с ОГВ, леченных фосфогливом и в группе контроля
Рисунок 5. Динамика общего билирубина у детей с ОГА, леченных фосфогливом и в группе контроля
Таблица 2. Динамика некоторых биохимических показателей крови у больных ОГВ на фоне лечения фосфогливом (основная группа, п = 15) и на фоне базисной терапии (группа сравнения, п = 13)
Биохимические показатели До лечения 10 день лечения 20 день лечения
Основная группа Группа сравнения р Основная группа Группа сравнения р Основная группа Группа сравнения р
Билирубин общий (мкм/л) 90,6 ± 6,5 91,6 ± 3,3 > 0,05 44,2 ± 3,1 53,3 ± 2,5 *< 0,05 14,3 ± 3,2 22,4 ± 1,8 *< 0,05
Билирубин конъю-гир. (мкм/л) 70 ± 5,8 72,3 ± 1,5 > 0,05 29,2 ± 2,3 22,3 ± 1,9 *< 0,05 4,0 ± 0,3 1,8 ± 1,7 *< 0,05
АлАТ (ед/л) 1484,6 ± 48,4 1510 ± 41,5 > 0,05 674 ± 112,8 1074 ± 79,4 *< 0,05 64,6 ± 5,2 81,6 ± 3,3 *< 0,05
АсАт (ед/л) 817,2 ± 138,7 975 ± 93,7 > 0,05 685,8 ± 155 150,2 ± 23 > 0,05 46 ± 1,3 50,2 ± 2,3 > 0,05
Щелочная фос-фатаза (ед/л) 394,4 ± 9,2 325 ± 8,2 > 0,05 272,4 ± 14,3 293 ± 14,0 > 0,05 303 ± 16,4 293 ± 145,0 > 0,05
Тимоловая проба (ед) 12,4 ± 0,7 18,2 ± 1,5 > 0,05 11,6 ± 13 10,9 ± 0,8 > 0,05 8,5 ± 2,6 9,1 ± 1,7 > 0,05
* — различие достоверно при р < 0,05 между основной и контрольной группами
мы у 10 из 12 леченных фосфогливом и у 9 из 14 — в группе контроля. А у больных ГВ у 8 из 15 и у 4 из 13 соответственно.
В сыворотке крови на 20 день лечения фосфогливом у всех детей с ГА и с ГВ наступила нормализация показателей общего и конъюгированного билирубина, тогда как в группе контроля эти величины еще не достигли нормальных значений. То же можно сказать и в отношении активности АлАТ и АсАТ. Однако цифровые показатели у леченных фосфогливом и контрольной группы различались не столь существенно, но все же у детей с ГВ в группе контроля активность АлАТ сохранялась повышенной по сравнению с нормальными величинами в 2—2,5 раза, тогда как в группе леченных фосфогливом она была в пределах нормальных значений (р < 0,05). Различия остальных показателей биохимических проб печени (АсАТ, тимоловая проба, щелочная фосфатаза) были статистически недостоверными.
Дети, получавшие фосфоглив, выписывались из стационара в среднем на 4—6 дней раньше, чем дети контрольных групп.
Таким образом, применение фосфоглива в комплексной терапии при острых гепатитах А и В способствует более быстрому улучшению общего состояния, снижению симптомов интоксикации, сокращению размеров печени, нормализации уровня билирубина и ак-
тивности АлАТ. Лечение фосфогливом сокращает сроки пребывания больных в стационаре.
фосфоглив хорошо переносится детьми. Побочных реакций не отмечалось.
Наши исследования позволяют рекомендовать назначение отечественного гепатопротектора «фосфоглив» при острых вирусных гепатитах у детей по схеме: по 1 таблетке 3 раза в день детям с 3 до 7 лет и по 2 таблетке 3 раза в день детям старше 7 лет в течение 15—20 дней.
При хроническом гепатите С после окончания 6-месячного курса лечения фосфогливом с вифероном состояние полной ремиссии отмечалось в 34% случаев, неполной ремиссии еще в 38% и только у трети (28%) больных не наблюдали сколько-нибудь существенного влияния лечения на репликацию вируса и активность патологического процесса (рис. 7).
При ХГВ первичная ремиссия отмечена у 4 из 8 больных (50%), вышедших в стабильную и длительную ремиссию. У 2 детей отмечалась неполная ремиссия, сохранившаяся в дальнейшем.
В I группе сравнения у больных ХГС на монотерапии вифероном первичная полная ремиссия наблюдалась у 39%, биохимическая — у 17% и отсутствие эффекта — у 44%. При хроническом гепатите В у больных, получавших монотерапию вифероном, — соответственно у 66, 12 и 22%.
ЕД/л 1800 -1 1600 -1400 -1200 -1000 -800 -600 -400 -200 -0 —
1510
контроль .1074
до лечения
10 день лечения
20 день лечения
Рисунок 6. Динамика активности АлАТ у детей с ОГВ, леченных фосфогливом и в группе контроля
Виферон + фосфоглив (п = 29)
Виферон (п = 70)
□ — неполная ремиссия; □ ремиссии
полная ремиссия; ■ — отсутствие
Рисунок 7. Эффективность применения (по консенсусу «Еиго-Иер») фосфоглива (в капсулах) в комбинации с вифероном в течение 6 мес. у больных ХГС
Во II группе детей, не получавших противовирусное лечение, ни в одном случае не отмечалось полной ремиссии (неполная биохимическая или серологическая ремиссия отмечалась у 5 из 27 больных ХГВ и у 3 из 12 больных ХГС).
Важно отметить, что большинство детей, включенных в группу комбинированной терапии, были рефрактерными на монотерапии вифероном.
Побочных эффектов не наблюдалось ни в одном случае лечения фосфогливом.
Выводы
1. Проведенное клиническое исследование показало высокую эффективность препарата «фосфоглив» у больных острыми А, В, хроническими В, С и микст В и С гепатитами, а также хроническими диффузными заболеваниями печени, обусловленными метаболическими нарушениями (гиперлипидемия, алкогольное поражение печени).
2. фосфоглив — удачная комбинация фосфатидилхо-лина и глицирризиновой кислоты, обладающая гепатопро-тективной и выраженной противовирусной активностью.
3. фосфоглив существенно улучшает синтетическую функцию печени и снижает клинико-лаборатор-ные проявления печеночной недостаточности различной (особенно алиментарной) этиологии.
4. Открытое сравнительное исследование препарата «фосфоглив» и базисной терапии показало, что по клиническим и биохимическим показателям фосфоглив является более эффективным, чем общепринятая базисная терапия, и сопоставимым с интерферонотерапией.
5. Отмечается достоверное влияние фосфоглива на репликтивную активность HBV и HCV. Новый отечественный препарат «фосфоглив» обладает хорошей пе-
реносимостью, побочные реакции в виде аллергической сыпи встречаются лишь у единичных больных.
6. Фосфоглив является препаратом выбора при лечении больных с ХГС, особенно у пациентов с высоким риском развития значимых побочных явлений терапии ИфН-альфа или в группе больных, где традиционное противовирусное лечение гепатита С противопоказано.
7. Результаты клинических контролируемых испытаний позволяют рекомендовать фосфоглив для лечения острых и хронических вирусных и диффузных заболеваний печени. Курс лечения: по 2,5 г 2 раза в неделю в/в плюс 600 мг/сутки в виде капсул при острых вирусных и других гепатитах — не менее 1—3 мес., при хронических гепатитах и диффузных заболеваниях печени — не менее 6—12 мес.
Литература:
1. Учайкин В. ф. Вирусные гепатиты у детей: от А до TTV / В. ф. Учайкин, Н. И. Нисевич, Т. В. Чередниченко. — М., 2003. — 431 с.
2. Учайкин В. ф. Комбинированная терапия хронических гепатитов В и С у детей / В. ф. Учайки н, Т. В. Чередниченко,
B. В. Малиновская // Педиатрия. — 2001. — Спец. вып. —
C. 58—61.
3. Байкова И. Е. Клинко-морфологическая динамика хронического вирусного гепатита С на фоне различных вариантов этиопа-тогенетического лечения: Автор. дисс. … к. м. н. — 2003.
4. Effects of glycyrrhizin on immune-mediated cytotoxicity / М. Yoshikawa et. al. // J. Gastroenterol. Hepatol. — 1997. — 12(3). — P. 243—248.
5. Effectivenes of interferon, glycyrrhizin combination therapy in patients with chronic hepatitis С / Y. Abe, T. Ueda, T. Kato, Y. Kohli // Nippon Rinsho. — 1994. — 52(7). — P. 1817— 1822.
6. Richard N. Podell. Licorice Root May Deter Liver Cancer // Article info. Health and Nutrition. — Breakthroughs 09/98.
Клиническая эффективность препарата «Нурофен для Детей» при ОРВИ со стенозируюшим ларинготрахеитом
Ф. С. Харламова, Т. П. Легкова, О. В. Кладова, Е. В. Демина, В. Ф. Учайкин
ГОУ ВПО РГМУ Росздрава, Москва Морозовская детская клиническая больница, Москва
У 50 детей в возрасте от 6 мес. до 12 лет, страдающих ОРВИ со стенозирующим ларинготрахеитом проводилась сравнительная оценка эффективности препаратов «Нурофена для Детей» и «Детского Панадола». Проводилась комбинированная терапия (симптоматическая, антигистаминная, противовирусная и/или антибактериальная). Эффективность лечения оценивалась в баллах в зависимости от сроков исчезновения интоксикации и лихорадки, выраженных воспалительных явлений со стороны дыхательных путей, ротоглотки и среднего уха).
Результаты исследования свидетельствуют о более выраженном и быстром, в сравнении с Детским Панадолом, жаропонижающем, обезболивающем и противовоспалительном действии Нурофена для Детей при ОРВИ, сопровождающимся стенозом гортани, острым средним отитом и обструктивным бронхитом. Нурофен для Детей рекомендован для широкого использования в педиатрической практике при заболеваниях, отягощенных аллергопатологией.
Ключевые слова: Нурофен для Детей, Детский Панадол, стенозирующий ларинготрахеит, отит, лихорадка, интоксикация
Синдром лихорадки является ведущим клиническим признаком всех инфекционных заболеваний. С теоретической точки зрения повышение температуры тела можно считать защитной реакцией, направлен-
ной на элиминацию инфекционного патогена. Однако на практике такое объяснение не всегда бывает корректным. Нередко у детей на высоте температурной реакции возникают нежелательные проявления в виде
ФОСФОГЛИВ УРСО инструкция по применению, цена, аналоги, показания, совместимость, отзывы
пр-т Героев, д.26 (1)
пр-т Ленина, д.67 (1)
пр-т. Бусыгина, д.19 (1)
пр-т. Бусыгина, д.45А (1)
пр-т. Гагарина, д.107 (1)
пр-т. Гагарина, д.184 (1)
пр-т. Гагарина, д.222 (1)
пр-т. Гагарина, д.84 (1)
пр-т. Кораблестроителей, д.22 (1)
пр-т. Кораблестроителей, д.25 (1)
пр-т. Ленина, д.16 (1)
пр-т. Ленина, д.28А (1)
пр-т. Ленина, д.41 (1)
пр-т. Ленина, д.77 (1)
пр-т. Октября, д.25 (1)
ул. Адмирала Макарова, д.3, корп.2 (1)
ул. Академика Сахарова, д.109 (1)
ул. Базарная, д.8 (1)
ул. Баранова, д.9 (1)
ул. Бекетова, д.18 (1)
ул. Бекетова, д.66 (1)
ул. Белинского, д.118/29 (1)
ул. Белинского, д.38 (1)
ул. Белинского, д.87 (1)
ул. Березовская, д.111 (1)
ул. Богородского, д.5, корп.1 (1)
ул. Большая Покровская, д.29 (1)
ул. Большая Покровская, д.63 (1)
ул. Бориса Панина, д.4 (1)
ул. Буревестника, д.16 (1)
ул. Васенко, д.3 (1)
ул. Веденяпина, д.10 (1)
ул. Верхне-Печерская, д. 14, корп. 1 (1)
ул. Верхне-Печерская, д.4, к.1 (1)
ул. Верхне-Печерская, д.5 (1)
ул. Военных Комиссаров, д.1 (1)
ул. Генерала Ивлиева, д.39 (1)
ул. Героя Прыгунова, д. 10 (1)
ул. Горная, д.11 (1)
ул. Движенцев, д.14 (1)
ул. Дьяконова, д.20 (1)
ул. Есенина, д.41 (1)
ул. Ефремова, д.16 (1)
ул. Зайцева, д.17 (1)
ул. Иванова Василия, д.14, к.1 (1)
ул. Касьянова, д.1 (1)
ул. Коминтерна, д. 4/2 (1)
ул. Коминтерна, д.160 (1)
ул. Коминтерна, д.172 (1)
ул. Краснодонцев, д.1 (1)
ул. Краснодонцев, д.9 (1)
ул. Краснозвездная, д.31 (1)
ул. Культуры, д.13 (1)
ул. Культуры, д.14 (1)
ул. Культуры, д.3 (1)
ул. Львовская, д.3 (1)
ул. Маршала Рокоссовского, д.4 (1)
ул. Маршала Рокоссовского, д.8А (1)
ул. Мончегорская, д.15а (1)
ул. Мончегорская, д.7А (1)
ул. Ногина, д.9 (1)
ул. Октябрьской революции, д.42 (1)
ул. Переходникова, д. 29 (1)
ул. Полтавская, д.16 (1)
ул. Родионова, д.189/24 (1)
ул. Родионова, д.195 (1)
ул. Родионова, д.5 (1)
ул. Светлоярская, д.24 (1)
ул. Светлоярская, д.32 (1)
ул. Сергея Есенина, д.32 (1)
ул. Телеграфная, д.3 (1)
ул. Тонкинская, д.7А (1)
ул. Фруктовая, д.5, корп.1 (1)
ул. Щербинки I, д.11 (1)
ул. Южное шоссе, д.28, корп.1 (1)
ул.Коминтерна, д. 168 (1)
ш. Казанское, д.10, корп.3 (1)
ш. Казанское, д.5 (1)
ш. Московское, д.126 (1)
ш. Московское, д.9 (1)
РазвернутьСвернуть
Фосфоглив ампулы раствор 2,5г n5 флакон, инструкция по применению
Полное название: Фосфоглив ампулы раствор 2,5г n5 флакон
Артикул товара: M9RWJX
Цена: 1027,6
- Форма выпуска:
раствор для инъекций - Упаковка:
5 флаконов по 2,5г - Дозировка:
500мг/200мг
Описание:
Форма выпуска
Лиофилизат для приготовления раствора для в/в введения
Состав
1 флакон содержит: Фосфолипида — 500 мг, глицирата — 200 мг
Упаковка
5 фл.
Фармакологическое действие
Фосфоглив — оригинальный гепатопротективный препарат на основе фосфатидилхолина (фосфолипид) растительного происхождения (из семян сои) и тринатриевой соли глицирризиновой кислоты из корня солодки.
Фосфоглив разработан в ИБМХ РАМН, как усовершенствованный аналог выпускаемого фирмой Nattermann Internetional GmBH, Germany препарата Эссенциале, используемого для лечения заболеваний печени.
Фосфолипиды являются основным структурным компонентом всех клеточных мембран. При препоральном введении в организм фосфолипиды воостанавливают целостность мембран клеток, в первую очередь печени — гепатоцитов.
Глицирризиновая кислота обладают широким спектром биологической активности, противовоспалительными свойствами, применяются для лечения заболеваний печени токсического и вирусного происхождения, в том числе и гепатита С. За счет детергентного действия обеспечивает эмульгирование фасфатидилхолина в кишечнике.
Сочетание этих двух компонентов делает фосфоглив особенно эффективным при лечении печени.
Показания
Применяют для лечения хронических заболеваний печени (гепатитов, гепатозов различной этиологии), цирроз печени, интоксикации, радиационный синдром, псориаз.
Противопоказания
Гиперчувствительность к компонентам препарата.
Способ применения и дозы
Инъекционный раствор вводят внутривенно предварительно растворив 2,5г (1 флакон) сухого лиофилизированного порошка в 10 мл апирогенной воды (воды для инъекций).
При острой форме заболевания препарат вводят 1 или 2 раза в день в течение 10-30 дней, при хронической форме 1 раз через день или 3 раза в неделю в течении 6 — 12 месяцев. После окончания внутривенного курса терапия может быть продолжена Фосфогливом в капсулах — по 2 капсулы 3 раза в день в течение 30 дней при острой и 6 -12 месяцев при хронической форме заболевания.
Побочные действия
При повышенной индивидуальной чувствительности возможно появление кожной сыпи, которая исчезает после отмены препарата.
Лекарственное взаимодействие
Содержимое флакона нельзя смешивать с другими растворами. Запрещается использовать для разведения препарата физиологический раствор или раствор глюкозы.
Условия хранения
В сухом, защищенном от света месте, при температуре не выше 20 °C
форма выпуска и когда назначается
Фармацевтическое средство Фосфоглив относится к гепатопротекторам. С помощью него лечат печень и кожные заболевания.
Содержание:
Что входит в состав лекарства
Действующими веществами капсулированной формы являются:
Дополнительные компоненты:
-
коллоидный безводный диоксид кремния -
микрокристаллическая целлюлоза -
тальк -
карбонат кальция -
стеарат кальция
Активно действующими компонентами лиофилизата для изготовления раствора для внутривенного введения так же является:
Форма выпуска
Производитель выпускает медикамент в двух формах:
1. Капсулы. Медикамент имеет оранжевый корпус и черную крышку. Внутри капсулы имеется желтоватый порошок. От препарата исходит едва уловимый специфический аромат.
Капсулы по 10 штук содержатся в блистерах, которые по 5 штук упаковываются в небольшие коробки из картона
2. Лиофизилат, предназначенный для внутривенного введения является светло-желтой либо белой массой. Производитель упаковывает препарат в 2, 5 г флаконы, которые по 5 или 10 штук кладутся в пачки из картона
Фармакодинамика
Фосфолипиды, которые являются активно действующими компонентами гепатопротектора, способствуют восстановлению поврежденных клеток печени. Они действуют на клеточную стенку, остальные элементы гепатоцидов, нормализуют липидный и белковый обмен в этих клетках.
Кислота глицирризиновая угнетающее воздействует на вирусы, стимулирует выработку интерферонов. Кроме того вещество славится мембраностабилизирующей и антиоксидантной активностью. Такое влияние распространяется не только на печень, медикамент хорошо подходит для терапии кожных патологий.
После перорального приема, происходит всасывание капсул. Максимальная концентрация лекарства в кровотоке может достигнуть через 6-24 часа. Препарат выводится с желчью и мочой.
Фармакокинетика
В случае внутривенного введения лекарственного средства, оно сразу попадает в кровь, соответственно максимальная концентрация будет достигнута быстрее. Действие на организм и выведение остаётся таким же, как при приеме Фосфоглива внутрь.
Когда назначается Фосфоглив
Капсулы Фосфоглив назначаются врачом при:
-
жировой дегенерации печени (гепатоз) -
циррозе печени -
различных видах отравления -
заболевании кожных покровов (нейродермит, экзема, псориаз) -
острые, хронические формы гепатита -
поражениях печени, вследствие злоупотребления спиртным, медикаментами
Противопоказания
Фармацевтическое средство запрещено принимать в следующих случаях:
-
грудное вскармливание -
беременность, все три триместра -
детский возраст, младше 12 лет -
антифосфолипидный синдром -
гиперчувствительность компонентам препарата
С особой осторожностью лекарственный препарат назначается пациентам, которые страдают от повышенного давления.
Побочные эффекты
Негативные проявления после употребления Фосфоглива встречаются довольно редко, обычно препарат хорошо переносится.
Какие нежелательные эффекты могут проявиться:
-
высыпания на кожном покрое -
отечность на периферических частях тела -
повышение артериального давления -
заложенность носа -
кашель -
конъюнктивит -
метеоризм -
отрыжка -
тошнота
Инструкция по применению
Внутривенное введение фармацевтического средства можно проводить пациентам старше 12 лет.
При приготовлении инъекционного раствора, медицинский сотрудник должен смешать содержимое ампулы с 10 мл воды, все необходимо хорошо перемешать.
Препарат необходимо вводить в дозировке 10 мл, внутривенную инъекцию проводят два раза в день.
Уколы делают недолго, чаще всего пациента
переводят на капсулированную форму лекарства.
Капсулы Фосфоглива можно назначать пациентам старше 12 лет.
Медикамент необходимо употреблять по 1 либо 2 капсулы 4 раза в сутки. Прием фармацевтического средства должен осуществляться во время употребления пищи. Капсулы Фосфоглива необходимо запивать водой. Лечебный курс может длиться до 6 месяцев.
Передозировка
Случаи передозировки не зарегистрированы. Однако стоит учесть, что среди компонентов есть кислота глицирризиновая. После попадания в организм в увеличенных дозах, он часто оказывает псевдокортикостероидный эффект. При этом увеличивается концентрация минералокортикидов, глюкокортикоидов в крови. В связи в организме увеличивается концентрация натрия и уменьшается количество калия. При этом человек может мучиться от повышения артериального давления и отеков.
Взаимодействие
Активно действующее вещество Фосфоглива усиливает воздействие кортикостероидных гормонов.
Условия продажи
Фосфоглив нельзя приобрести без рецепта, выписанного лечащим доктором.
Условия хранения
Фармацевтическое средство требует хранения, как медикаменты, входящие в группу Б. Лекарство необходимо защищать от воздействия солнечного света. Требуемая температура максимум 20градусов.
Срок годности Фосфоглива
Лекарственные капсулы можно хранить не более 3 лет, ампулы годны в течение 2 лет.
Особые указания
Врачи должны с осторожностью прописывать Фосфоглив больным, которым поставлен диагноз гипертензия. Если прием медикамента, стал причиной повышения показателей давления, рекомендуется отказаться от дальнейшего лечения, обратиться за медицинской помощью.
Раствор, приготовленный для в/в запрещено смешивать с другими медикаментами.
Фосфоглив и алкоголь
Стоит иметь в виду, что лекарство и этанол оказывают на работы печени противоположные влияния. Спиртное мешает регенерации клеток органа, его употребление в большом объеме, делает лечение практически бессмысленным.
Однако одноразовый прием спиртного в период лечения, не должен отрицательно сказаться на здоровье человека. Здесь имеется в виду небольшая доза алкогольных напитков.
Аналогичные препараты
Фосфоглив имеет следующие аналоги:
Фосфоглив при сахарном диабете: механизм действия
Широкое применение нашел «Фосфоглив» при сахарном диабете. Этот лекарственный препарат эффективно лечит заболевания печени, которые зачастую являются осложнением сахарного диабета. «Фосфоглив» представляет собой гепатопротектор, обладающий способностью купировать воспалительные процессы и уничтожать вирусные агенты. Использовать при сахарном диабете гепатопротекторное средство необходимо по назначению врача, строго придерживаясь назначенных им дозировок.
Состав и форма выпуска
Производится фармацевтический препарат, основное предназначение которого лечить патологии печени, в виде капсул, помещенных в блистеры по 10 штук. Можно приобрести «Фосфоглив» и в форме порошка, из которого готовится раствор для в/в введения. «Фосфоглив» состоит и следующих активнодействующих и вспомогательных веществ:
- фосфолипиды и натрия глицирризинат в качестве активных компонентов таблеток и раствора;
- МКЦ;
- аэросил;
- тальк;
- углекислый кальций;
- пищевой эмульгатор Е572;
- мальтоза (в качестве дополнительного вещества в составе порошка).
Вернуться к оглавлению
Механизм действия
Терапевтический эффект лекарственного средства «Фосфоглив» достигается благодаря его составу, а точнее, активным компонентам, которые способны нормализовать липидный и белковый обмен, оказывая при этом положительное воздействие на функционирование самой крупной железы у человека. «Фосфоглив» является уникальным препаратом, ведь содержащиеся в нем фосфолипиды, изготовленные химическим путем, имеют строение идентичное натуральному. Кроме этого, обладает фармпрепарат еще одной не менее важной способностью — он снимает воспалительные процессы, снижая тем самым болезненную симптоматику и предупреждая развитие атрофических процессов.
Вернуться к оглавлению
Когда назначается?
С помощью «Фосфоглива» можно вылечить различные патологические состояния. В таблице описаны случаи, когда целесообразно использовать конкретную лекарственную форму медпрепарата:
| Вид лекарства | Показания |
|---|---|
| Капсулы | Гепатоз |
| Псориаз | |
| Вирусные гепатиты острого и хронического характера в комплексном лечении | |
| Поражение печени токсическими, алкогольными и лекарственными веществами | |
| Цирроз печени | |
| Порошок для приготовления раствора | Жировая дистрофия печени, в частности, при сахарном диабете |
| Острая лучевая болезнь | |
| Псориаз | |
| Отравление организма химическими, пищевыми веществами | |
| Цирроз печени | |
| Острый и хронический гепатит |
Вернуться к оглавлению
Инструкция по применению и дозировка
В инструкции написано, что принимать нужно по две капсулы трижды в день.
Медицинское средство «Фосфоглив» принимают во время приема пищи, не разжевывая и запивая небольшим объемом жидкости. Необходимую дозировку подбирает квалифицированный врач, основываясь на результатах диагностического обследования. В аннотации к препарату указана общая дозировка, которая применяется для всех категорий больных и составляет она 2 таблетки трижды в сутки. Лечение в среднем длится 3 месяца.
Если для терапии заболеваний печени, которые зачастую возникают при сахарном диабете, больному назначали «Фосфоглив» в виде порошка, то потребуется развести порошкообразную консистенцию в воде из соотношения: 1 флакончик лекарства на 10 мл инъекционной воды. Готовый раствор вводят 1—2 раза в сутки на протяжении 10—30 дней, если было выявлено острое течение недуга. Больным с хронической формой печеночных заболеваний делают по 1-му уколу трижды в неделю на протяжении 6—12-ти месяцев.
Вернуться к оглавлению
Противопоказания
Не рекомендуется использовать «Фосфоглив» лицам с индивидуальной непереносимостью какого-либо компонента из состава препарата. Помимо этого, ограничением к приему гепатопротектора выступают:
- период вынашивания ребенка;
- грудное вскармливание;
- детский возраст до 12-ти лет;
- антифосфолипидный синдром;
- повышенное кровяное давление.
Вернуться к оглавлению
Негативные реакции «Фосфоглива» при сахарном диабете
В большинстве случае «Фосфоглив» переносится пациентами хорошо и не провоцирует побочных явлений. Однако изредка медпрепарат может вызвать такие нежелательные эффекты:
Иногда прием препарата сопровождается кашлем.
- кашель;
- высыпания на покровах кожи;
- заложенность носа;
- конъюнктивит;
- увеличение артериального давления;
- дискомфорт в области живота;
- подташнивание, отрыжка и скопление в животе газов.
Наблюдая перечисленную побочную симптоматику, необходимо прекратить прием «Фосфоглива» и обратиться к доктору.
Вернуться к оглавлению
Заменители
Если для лечения печеночных заболеваний, возникших при сахарном диабете, нет возможности использовать «Фосфоглив», медиками назначается аналогичное по фармацевтическому действию медицинское средство. Заменить описываемое лекарство могут:
- «Фосфатидилхолин»;
- «Липостабил»;
- «Эссливер форте»;
- «Лифолин форте»;
- «Гепафор»;
- «Дипана»;
- «Гепатосан»;
- «Карсил»;
- «Глутаргин»;
- «Максар»;
- «Прогепар»;
- «Силимар»;
- «Силибинин»;
- «Тыквеол»;
- «Метрол ГП»;
- «Холенол»;
- «Ропрен».
Вернуться к оглавлению
Условия продажи и хранения
Продается «Фосфоглив» в аптеке, и купить его можно без рецепта от врача. Фармацевтическое средство хранят в недоступном для маленьких деток месте. Вас беспокоит вопрос о том, как подобрать хороший игровой дом, чтобы не столкнуться с неприятностями? Здесь https://elenarou.com/samye-luchshie-kazino/ вы можете ознакомиться со всей необходимой информацией. Узнать о самых лучших казино, ознакомиться с их преимуществами и перспективами. Выбирайте для себя более подходящий вариант и регистрируйтесь. Приятное времяпровождение будет вам гарантировано. Важно, чтобы в помещении, где сберегается медикамент, температура на столбике термометра не поднималась выше 25-ти градусов Цельсия, а на упаковку не проникали солнечные и световые лучи. При соблюдении перечисленных условий срок годности составит 36 месяцев и по истечении этого периода использовать фармпрепарат категорически противопоказано.
Особенности абсорбции глицирризиновой кислоты в лекарственной форме Фосфоглив
Ипатова О.М., Фосфоглив: механизм действия и применение в практике . М .: Институт биомедицинской химии, 2005.
Google Scholar
Als, M. и Hosseinzaden, H., Phytother. Res. , 2008, т. 22. С. 709–724.
Артикул
Google Scholar
Бюлер Х., Першель Ф.Х., Фитцнер Р. и Хирхольцен К., Стероиды , 1994, т. 59, нет. 2. С. 131–135.
Артикул
CAS
Google Scholar
Плоегер, Б., Менсинга, Т., Сипс, А., Сейнен, В., и Меуленбельт, Дж., Обзоры метаболизма лекарств , 2001, том. 33, нет. 2. С. 125–147.
Артикул
CAS
Google Scholar
Такеда, С., Ishthara, K., Wakui, Y., Amagaya, S., Maruno, M., Akao, T., and Kobashi, K., J. Pharm. Pharmacol. , 1996, т. 48, вып. 9. С. 902–905.
Артикул
CAS
Google Scholar
Акао, Т., Хаяси, Т., Кобаши, К., Канаока, М., Като, Х., Кобаяси, М., и Такеда, С., J. Pharm. Pharmacol. , 1994, т. 46, нет. 2. С. 135–137.
Артикул
CAS
Google Scholar
Кантелли-Форти, Г., Маффеи, Ф., Хрелия, П., Бугамелли, Ф., Бернарди, М., Д’Интино, П., и Маранези, М., Environ. Здоровье Persp. , 1994, т. 102, вып. 9. С. 65–68.
Артикул
CAS
Google Scholar
Сасаки, К., Йонэбаяси, С., Йошида, М., Симидзу, К., Аотсука, Т., и Такаяма, К., Int. J. Pharmaceutics , 2003, т. 265. С. 95–102.
Артикул
CAS
Google Scholar
Lin, Z.J., Qiu, S.-X., Wufuer, A., and Shum, L., J. Chromatogr. В , 2005, т. 814. С. 201–207.
Артикул
CAS
Google Scholar
Игнатов Д.В., Прокофьев Ю.И., Ипатова О.М., Тимофеев В.П., Медведева Н.В., Мишарин А.Ю., Биоорган. Хим. , 2003, т. 29, нет. 4. С. 429–433.
CAS
Google Scholar
Кога К., Кавасима С., Шибата Н., Такада К. и Мураками М., Biol. Pharm. Бык. , 2003, т. 26, вып. 9. С. 1299–1305.
Артикул
CAS
Google Scholar
Чжоу, Л., Ян, Дж., Чжан, X.Y., Лю, X.Q. и Ван, Г.Дж., Яо Сюэ Сюэ Бао , 2008, т. 43, нет. 1. С. 71–75.
CAS
Google Scholar
Фосфоглив гепатопротектор усиленная формула фосфолипиды + глицирризин (50 капсул)
Описание
Активные вещества:
фосфатидилхолин (эссенциальные фосфолипиды) — 65 мг;
натрия глицирризинат — 35 мг.
Принимать по две капсулы 3 раза в день.
https://www.phosphogliv.ru
Фосфоглив:
- Доказанное действие на причины повреждения печени
- Восстановление клеток печени
- Благоприятный профиль безопасности
- Доступная стоимость курса терапии
- Широкий спектр применения
- Оптимальный состав активных ингредиентов.
Фосфоглив помогает на всех стадиях поражения печени!
— Жировая болезнь печени (гепатоз)
— Воспаление клеток печени
— Замена клеток печени рубцовой тканью
— Профилактика цирроза
Показания к применению:
- вирусный гепатит (острый и хронический)
- жировая дистрофия печени (гепатоз)
- другие поражения печени (наркотические, алкогольные, токсические)
- цирроз печени
- интоксикация
- псориаз
- нейродермит
- экзема
Для профилактики:
Стресс, Плохая экология, Недоедание, Малоподвижный образ жизни.
Для восстановления печени:
Переедание, прием алкоголя, лекарства.
Фосфатидилхолин (действующее вещество фосфолипидов) является основным структурным элементом клеточных и внутриклеточных мембран, способен восстанавливать их структуру и функцию в случае повреждения, обладая цитопротекторным действием. Он нормализует белковый и липидный обмен, предотвращает потерю ферментов и других активных веществ гепатоцитами, восстанавливает детоксицирующую функцию печени, тормозит образование соединительной ткани, снижая риск фиброза и цирроза печени.
Глицирризиновая кислота — основной активный компонент корня солодки, который успешно применяется в медицине более 3000 лет.
Глицирризиновая кислота обладает противовоспалительным действием, подавляет размножение вирусов в печени и других органах, стимулируя выработку интерферонов, увеличивая фагоцитоз и повышая активность естественных клеток-киллеров. Обладает гепатопротекторным действием за счет антиоксидантной и мембраностабилизирующей активности. Он потенцирует действие эндогенных глюкокортикостероидов, оказывая противовоспалительное и противоаллергическое действие при неинфекционных поражениях печени.
Рецепт не требуется.
Принимать внутрь, во время еды, не разжевывая, запивая небольшим количеством жидкости.
Рекомендуемая схема приема для взрослых и детей старше 12 лет — по 2 капсулы 3 раза в сутки. Срок использования может составлять до 6 месяцев, в среднем — 3 месяца.
1 капсула:
Активные вещества:
-Фосфолипиды (основной компонент фосфатидилхолина) — 65 мг,
-Глицирризинат натрия — 35 мг.
Вспомогательные вещества:
микрокристаллическая целлюлоза — 141,2 мг, карбонат кальция — 204,7 мг, стеарат кальция — 0,9 мг, тальк — 7,7 мг, диоксид кремния коллоидный (аэросил) — 5,5 мг, твердые желатиновые капсулы — 96,0 мг [случай: краситель закатный закат желтый (E110) — 1,0%, диоксид титана (E171) — 1,0%, желатин — до 100,0%; колпачок: диоксид титана (Е171) — 0,2%, краситель оксид железа черный (Е172) — 3,5%, желатин — до 100,0%].
Твердые желатиновые капсулы.
Корпус капсулы — оранжевый, крышка — черная.
Содержимое капсулы представляет собой гранулированный порошок от белого со слегка желтоватым оттенком до светло-желтого цвета со слабым специфическим запахом.
Повышенная чувствительность к глицирризиновой кислоте, фосфатидилхолину или другим компонентам препарата.
Антифосфолипидный синдром.
Беременность (данных об эффективности и безопасности недостаточно).
Период грудного вскармливания (данных об эффективности и безопасности недостаточно).
Детский возраст до 12 лет (данных об эффективности и безопасности недостаточно).
С осторожностью: у пациентов с портальной гипертензией, у пациентов с артериальной гипертензией.
При наличии данных заболеваний перед приемом препарата следует проконсультироваться с врачом.
Производство Россия.
Производитель: Фармстандарт (PHS JSC)
Это оригинальный продукт. Поставляется в оригинальной упаковке.
Присылаю товар, выпущенный для распространения в России, поэтому текст и надпись на русском языке.
Абсолютно новое состояние, не использовалось, не вскрывалось.
Срок годности : 3 года.
Даты изготовления и срок годности, указанные на упаковке, указаны в европейском формате: ДД / ММ / ГГ.
Дата производства : 12/2019 или новее.
Хранение: хранить в сухом месте при температуре не выше 25 ° C.
Я отправляю товары зарегистрированным экономом Авиапочтой (с номером отслеживания).
Обычно отправка товаров занимает от 2 до 4 дней (после оплаты).
Возможность на 200 миллиардов долларов США: глобальный лекарственный препарат с наночастицами
Дублин, 20 апреля 2018 г. (ГЛОБАЛЬНАЯ ИНФОРМАЦИЯ) — В предложение ResearchAndMarkets.com добавлен отчет «Глобальный рынок доставки лекарств с наночастицами, дозировка, цены и клинические перспективы на 2024 год».
Доставка лекарств играет важную роль в определении терапевтического результата лечения. Ограничения традиционной системы доставки лекарств, такие как низкая биодоступность терапевтических средств, плохое соблюдение пациентом режима лечения и колебания концентрации, привели к острой необходимости в разработке нового, лучшего и безопасного метода доставки с улучшенным терапевтическим результатом и безопасностью.
Понимание рыночных тенденций показывает, что способность наночастиц значительно улучшать терапевтический результат побудила фармацевтические компании разработать составы с наночастицами популярных препаратов, таких как Megace ES (повышенная стабильность), Estrasorb (эмульсия для местного применения эстрадиола) и Triglide. (Нанокристаллический состав Tricor). Составы с наночастицами популярных терапевтических средств против рака, таких как доксорубицин и таксол, также были хорошо приняты в терапевтическом сегменте рака из-за более длительного периода полураспада и снижения побочных эффектов.
Развитие нанотехнологий привело к появлению на рынке многих типов наночастиц. Нанокристаллы и липосомы в настоящее время являются наиболее популярными наночастицами, за ними следуют мицеллы и дендримеры. В настоящее время разрабатываются и продаются лекарственные формы на основе нанокристаллов, липосом и мицелл, что, несомненно, увеличит размер рынка в будущем.
Географический анализ метода доставки лекарств с помощью наночастиц прогнозирует растущее доминирование США, занимающих более 40% мирового рынка, за которыми следует Европа.Однако ожидается, что в течение прогнозируемого периода размер рынка в Азиатско-Тихоокеанском регионе и Латинской Америке увеличится из-за множества факторов роста, поддерживающих анализ, таких как увеличение количества пациентов и растущий интерес ключевых игроков, таких как Johnson & Johnson и Novartis, к регион.
Исследование оценивает глобальный рынок лекарств с наночастицами в размере более 200 миллиардов долларов США к 2024 году при среднегодовом темпе роста 10%. Факторы, способствующие росту, такие как увеличение глобальной распространенности различных клинических показаний, таких как рак, диабет и ревматоидный артрит, неизбежно будут способствовать росту рынка, в котором онкология является доминирующим сегментом.Ожидается, что растущий спрос на эффективные методы лечения для растущего числа пациентов также поможет сегменту сохранить доминирующее положение в прогнозируемом периоде отчета.
Рынок доставки наночастиц лекарств, однако, сталкивается с некоторыми серьезными проблемами, которые, как ожидается, будут препятствовать его дальнейшему росту. Высокий спрос на инвестиции, научные и технические ограничения и перенаселенность поставщиков и маркетинговые проблемы, такие как непомерно высокие цены на терапевтические препараты, ограниченное проникновение на рынок и низкая осведомленность, являются препятствиями, о которых необходимо позаботиться, чтобы повысить потенциал сегмента доставки лекарств на основе наночастиц.
В этом отчете об исследовании глобального рынка доставки лекарств с использованием наночастиц содержится углубленный анализ рынка с особым акцентом на размер глобального рынка, текущие рыночные тенденции, динамику и другие факторы, которые могут повлиять на рынок. Сравнительный анализ цен, дозировок и затрат на терапию оригинальных препаратов с составами наночастиц анализирует многообещающий потенциал доставки лекарств на основе наночастиц, что в конечном итоге доказывает их превосходство. Анализ исследования основан на обширных исследованиях как из первичных, так и из вторичных источников, выделяя рыночные возможности на региональном уровне и обеспечивая оптимистичный прогноз будущего глобального рынка доставки лекарств с использованием наночастиц.
Основные моменты отчета:
- Рынок наночастиц: 200 миллиардов долларов США Возможности к 2024 году
- Глобальный трубопровод для лекарств с наночастицами: 231 лекарство
- Лекарства, входящие в фазу испытаний II и выше: 33 препарата
- Наркотики, продаваемые на рынке Лекарства
- Дозировка, цена и патентный анализ ключевых лекарств
- Предстоящие методы доставки лекарств с наночастицами
- Глобальный клинический трубопровод с наночастицами по компаниям, показаниям и фазам
Основные темы:
1.Наночастицы — революционный метод доставки лекарств
1.1 Пролог к целевой доставке лекарств с помощью наночастиц
1.2 Доставка лекарств с помощью наночастиц — повышение эффективности терапии с помощью нанотехнологий
2. Потребность в доставке лекарств с помощью наночастиц
2.1 Ограничения традиционных методов доставки лекарств
Растущий спрос на более эффективные методы адресной доставки лекарств в онкологическом сегменте
3. Превосходство доставки лекарств на основе наночастиц над традиционной доставкой лекарств
3.1 Лучший терапевтический результат, чем традиционные методы доставки лекарств
3.2 Роль наночастиц в лучшей диагностике рака
4. Важность доставки наночастиц в терапию рака
4.1 Широкое применение наночастиц в терапии рака
4.2 Механизмы интернализации наночастиц при раке Клетки для визуализации и терапии
5. Существующие методы доставки лекарств с наночастицами
5.1 Нанокристаллы
5.2 Липосомы
5.3 Дендримеры
5.4 Доставка лекарств на основе мицелл
6. Предстоящие методы доставки лекарств с наночастицами
6.1 Полимерные наночастицы
6.2 Наночастицы на основе металлов (золото, оксид железа)
6.3 Фуллерены и углеродные нанотрубки
6.4 Доставка квантовых точек
. Обзор мирового рынка лекарств с наночастицами
7.1 Текущий сценарий рынка
7.2 Обзор глобального клинического трубопровода лекарств с наночастицами
8. Анализ цен и дозировки коммерчески доступных терапевтических средств с наночастицами
8.1 Липосомальный доксорубицин
8.1.1 Доступность, цена и механизм действия
8.1.2 Дозировка при различных клинических показаниях
8.1.3 Липосомальный доксорубицин (наночастицы) против традиционного доксорубицина — сравнительный анализ
8.2 Амфотерицин
8.2.1 Доступность, цена & Механизм действия
8.2.2 Дозировка по показаниям
8.2.3 Сравнительный анализ — Обычные составы наночастиц амфотерицина B v / s
8.3 Паклитаксел (таксол, онксал)
8.3.1 Доступность, цена и механизм действия
8.3.2 Анализ дозировки при различных типах рака
8.3.3 Паклитаксел против Abraxane (липосомальный)
8.4 Сиролимус (Rapamune)
8.4.1 Доступность, цена и механизм действия
8.4.2 Rapamune — анализ дозировки
8.5 Исправить (Aprepitant Nanocrystal)
8.5.1 Доступность и цена
8.5.2 Анализ дозировки
8.6 Megace ES (Повышенная стабильность)
8.6.1 Доступность, цена и механизм действия
8.6.2 Сравнительный анализ дозировки — Megace против Megace ES
8,7 Эмульсия для местного применения эстрадиола (Estrasorb)
8.8 Другие терапевтические составы с наночастицами
8.8.1 Feraheme
8.8.2 Триглид — нанокристаллическая версия Tricor
9. Доставка лекарств с наночастицами — тенденции рынка и анализ распределения патентов
9.1 Статус подачи заявок на патенты в области доставки лекарств с наночастицами
9.2 Распространение патентов Тип наноматериала
9.3 Распространение патентов по стимулам
9.4 Распространение патентов по способам введения и формам доставки лекарств
10. Движущие факторы рынка доставки наночастиц лекарств
10.1 Растущая распространенность заболеваний и потребность в лучших терапевтических средствах
10.2 Лучшая надежность и безопасность по сравнению с традиционными терапевтическими средствами
10.3 Прогресс в исследованиях и разработках
10.4 Перспективные инвестиции и рыночный потенциал
10.5 Быстрое развитие инновационных и передовых технологий
11. Сложные аспекты сегмента доставки наночастиц
11.1 Дорогая техника и продукты с наночастицами
11.2 Научно-технические ограничения, связанные с доставкой наночастиц
11.3 Региональные ограничения и низкий уровень проникновения на рынок
11.4 Доминирование сегмента доставки обычных лекарств
12. Прогноз на будущее и анализ рынка глобального рынка доставки лекарств с наночастицами
13. Глобальный клинический трубопровод с наночастицами по компаниям, показаниям и фазам
13,1 Неизвестно
13,2 Исследования
13,3 Доклинические
13,4 Клинические
13,5 Фаза-I
13,6 Фаза-I / II
13,7 Фаза-II
13,8 Фаза-II / III
13.9 Фаза III
13.10 Предварительная регистрация
13.11 Зарегистрировано
14. Клинические данные о продаваемых на рынке лекарственных препаратах с наночастицами по компаниям и показаниям
14.1 Рилпивирин (эдурант)
14.2 Паклитаксел, связанный с альбумином (Abraxane, CoraxaneLEX10 и Coroxane®)
14,4 Ферумокситол (Feraheme & Rienso)
14,5 Липосомальный паклитаксел — Sun Pharma Advanced Research Company
14,6 Фенофибрат (Lipanthyl & TriCor)
14,7 Доксорубицин липосомальный (Caelyx & Doxil)
14.8 Винкристин липосомальный (Marqibo)
14,9 Фенофибрат (триглид)
14,10 Rexin-G
14,11 Эстрадиол для местного применения (Estrasorb)
14,12 Glycyrrhiza / Phosphatidylcholine (Phosphogliv) 15103 14,13 Пейзаж (Phosphogliv) BioScience
15.2 Access Pharmaceuticals
15.3 Alnylam Pharmaceuticals
15,4 Amgen
15,5 Arrowhead Research
15,6 BIND Therapeutics
15,7 Cadila Healthcare
15,8 Celegen Corporation
15.9 Celsion Corporation
15.10 Genzyme Corporation
15.11 Merck
15.12 NanoCarrier
15.13 Nippon Kayaku
15.14 Nanobiotix
15.15 Novavax
15.16 Pfizer
15.17 Roche
15.18 Samyang
15.19 Sanofi 9a10 Pharmps Подробнее об этом отчете : //www.researchandmarkets.com/research/qhb34f/us_200_billion? w = 12
ПРАЙМ PubMed | [Гемореологическая и клиническая эффективность нового фосфолипидного гепатопротекторного препарата Фосфоглив у больных псориатическим артритом]
Цитата
Ипатова О.М., и другие. «[Гемореологическая и клиническая эффективность нового фосфолипидного гепатопротекторного препарата Фосфоглив у пациентов с псориатическим артритом]». Биомедицинская Химия, т. 49, нет. 5, 2003, стр. 484-90.
Ипатова О.М., Насонов Е.Л., Коротаева Т.В. и др. Гемореологическая и клиническая эффективность нового фосфолипидного гепатопротекторного препарата Фосфоглив у больных псориатическим артритом. Биомед Хим . 2003; 49 (5): 484-90.
Ипатова О.М., Насонов Э.Л., Коротаева, Т. В., Фирсов, Н. Н., Ивкина, О. А., Торховская, Т. И., Арчаков, А. И. (2003). Гемореологическая и клиническая эффективность нового фосфолипидного гепатопротекторного препарата Фосфоглив у больных псориатическим артритом. Биомедицинская Химия , 49 (5), 484-90.
Ипатова О.М., и др. Гемореологическая и клиническая эффективность нового фосфолипидного гепатопротекторного препарата Фосфоглив у больных псориатическим артритом. Биомед Хим. 2003 сентябрь-октябрь; 49 (5): 484-90.PubMed PMID: 16119102.
TY — JOUR
Т1 — [Гемореологическая и клиническая эффективность нового фосфолипидного гепатопротекторного препарата Фосфоглив у больных псориатическим артритом].
АУ — Ипатова О М,
А.Ю. — Насонов Э.Л.,
АУ — Коротаева Т.В.,
АС — Фирсова, Н Н,
AU — Ивкина, О А,
AU — Торховская, Т I,
AU — Арчаков А Я,
PY — 2005/8/27 / pubmed
PY — 2005/10/12 / medline
PY — 2005/8/27 / entrez
СП — 484
EP — 90
JF — Биомедицинская химия
JO — Биомед Хим
ВЛ — 49
ИС — 5
N2 — Новый фосфолипидный препарат «Посфоглив» ранее показал хорошие результаты при лечении заболеваний печени.Механизм его действия заключается в неспецифической репарации биомембран. В настоящем исследовании он использовался для лечения пациентов с псориатическим артритом, сопровождающимся серьезными нарушениями реологии крови. Группа больных принимала Фосфоглив 3 месяца по 0,6 г в сутки. После лечения наблюдалось значительное снижение агрегации эритроцитов. Изменений общей вязкости крови не было. После проведенного лечения клиническое состояние пациентов заметно улучшилось. Одновременное снижение уровня С-реактивного белка в крови свидетельствует об ослаблении воспаления.Механизм этих эффектов может включать прямое влияние фосфолипида на мембраны эритроцитов и / или косвенное влияние через улучшение функции печени. Результаты показывают, что включение Фосфоглива в терапию улучшило состояние пациентов с псориатическим артритом. Результаты настоящего исследования также указывают на принципиальную возможность расширения клинического применения этого препарата. Его положительные эффекты основаны на мембранно-репаративных свойствах полиненасыщенного фосфатидилхолина в сочетании с противовоспалительным и иммуномодулирующим действием его второго компонента, глицирризиновой кислоты.СН — 2310-6972
UR — https://www.unboundmedicine.com/medline/citation/16119102/%5bhemorheological_and_clinical_efficiency_of_a_new_phospholipid_hepatoprotective_drug_phosphogliv_in_patients_with_psoriatic_arthritis%5d_
L2 — http://www.diseaseinfosearch.org/result/592
БД — ПРЕМЬЕР
DP — Unbound Medicine
ER —
Phospholiv — Уникальный тоник для печени и стимулятор роста, लिवर टॉनिक — Vetneeds Labs, Bengaluru
О компании
Год основания 1994
Юридический статус Фирмы Физическое лицо — Собственник
Характер бизнеса Производитель
Количество сотрудников от 11 до 25 человек
Годовой оборот2-5 крор
Участник IndiaMART с марта 2010 г.
GST29AVXPS8326D1ZS
Код импорта и экспорта (IEC) 07140 *****
Основанная в 1994, Vetneeds Group является одним из самых известных производителей и Trader из ветеринарных товаров . Наш широкий ассортимент продукции включает ветеринарный болюс, КОРМОВУЮ ДОБАВКУ ДЛЯ ВЕТЕРИНАРИИ и порошок антибиотика широкого спектра действия для ветеринарии и птицеводства.Они широко признаны уважаемыми покупателями за их высокую пищевую ценность, гигиеническую обработку, точный состав, рентабельность, более длительный срок хранения и безопасность. Наши товары обрабатываются в соответствии со стандартами и нормами Управления по санитарному надзору за качеством пищевых продуктов и медикаментов. Изготовленный с использованием сырья высшего качества, весь наш ассортимент олицетворяет их долговечность, качество, прочность и многое другое. Используя наш клиентоориентированный подход, мы предоставляем ветеринарные товары по доступным ценам нашей огромной клиентской базе в различных отраслях промышленности.
Наша организация создала хорошо обслуживаемую инфраструктуру, которая поддерживается необходимыми удобствами. Для оптимизации всех наших бизнес-операций мы разделили нашу инфраструктуру на разные отделы. Каждый отдел оснащен новейшим оборудованием и передовыми технологиями, которыми эффективно управляют наши квалифицированные и опытные специалисты. Это позволяет нам удовлетворять особые и оптовые потребности клиентов в течение указанного периода времени.Кроме того, мы также разработали надежную и вместительную складскую единицу. Это устройство установлено со всеми основными удобствами, необходимыми для безопасного хранения предлагаемых нами продуктов.
Профилактика лекарственного поражения печени у пациентов с туберкулезом легких и хроническим гепатитом С
Резюме
Справочная информация: Хронический гепатит С (ХГС) у больных туберкулезом легких (ТБ) является основным фактором риска лекарственного поражения печени (ЛПП) во время противотуберкулезной терапии (АТТ), причина отмены эффективных противотуберкулезных препаратов и прогрессирующего поражения печени.Комбинация эссенциальных фосфолипидов и глицирризина (Фосфоглив) доказала свою эффективность в симптоматическом лечении пациентов с ХГС. Его роль в профилактике ЛПП во время АТТ у пациентов с туберкулезом и ХГС не изучена.
Цель — оценить эффективность эссенциальных фосфолипидов / глицирризина для профилактики ЛПП у пациентов с ХГС и туберкулезом легких.
Методы: В проспективное когортное исследование были включены 55 больных туберкулезом легких с хроническим гепатитом С, 45 мужчин и 10 женщин в возрасте от 23 до 74 лет (медиана 38 лет).Отмечена активная репликация вируса с исходным уровнем трансаминаз 1,5-2,5 ULN. Пациенты первой группы (n = 27) получали эссенциальные фосфолипиды / глицирризин (Фосфоглив) по 300 мг ежедневно с начала АТТ; контрольная группа (n = 28) получала АТТ без фосфоглива. Оценивалась частота любого повышения трансаминаз более чем на 3 ULN и DILI с необходимостью отмены противотуберкулезных препаратов.
Результаты: среди пациентов первой группы было меньше случаев повышения трансаминаз более чем на 3 ULN: 6/27 (22.2%) против 14/28 (50%) в контрольной группе, p = 0,03. Клинически значимые ЛПП, требующие отмены АТТ, наблюдались у 3/27 пациентов против 10/28 пациентов в контрольной группе (p = 0,03).
Заключение. Комплекс эссенциальных фосфолипидов и глицирризина эффективен для профилактики поражения печени и обеспечения непрекращающейся АТТ у больных туберкулезом с ХГС.
Сноски
Цитируйте эту статью как: European Respiratory Journal 2019; 54: Дополнение. 63, PA2024.
Это тезисы Международного конгресса ERS. Полнотекстовая версия недоступна. Дополнительные материалы, сопровождающие этот тезис, могут быть доступны на сайте www.ers-education.org (только для членов ERS).
- Авторские права © авторы 2019
Глобальный рынок доставки лекарств с наночастицами, дозировка, цены и клинические перспективы развития 2024
«Глобальный рынок доставки наночастиц, дозировка, цены и клинические перспективы на 2024 год» Основные моменты отчета:
- Рынок наночастиц: возможности на 200 миллиардов долларов к 2024 году
- Глобальный трубопровод для лекарств с наночастицами: 231 лекарство
- Препараты, включенные в исследования фазы II и выше: 33 препарата
- Продаваемые препараты с наночастицами: 13 препаратов
- Дозировка, цена и патентный анализ основных лекарственных средств
- Предстоящие методы доставки лекарств с наночастицами
- Глобальный клинический трубопровод для лекарственных препаратов с наночастицами по компаниям, показаниям и фазам
Доставка лекарств играет важную роль в определении терапевтического результата лечения.Ограничения традиционной системы доставки лекарств, такие как низкая биодоступность терапевтических средств, плохое соблюдение пациентом режима лечения и колебания концентрации, привели к острой необходимости в разработке нового, лучшего и безопасного метода доставки с улучшенным терапевтическим результатом и безопасностью.
Практика доставки лекарств резко изменилась за последние несколько десятилетий, и в будущем ожидаются существенные изменения. Новый метод, который явно выделяется, — это использование нанотехнологии в доставке лекарств, в которой используются специально разработанные наночастицы для более эффективной и точной доставки лекарств с дополнительными преимуществами, такими как более длительная доставка в кровоток, более длительный период полураспада, лучшая биодоступность, улучшенная фармакокинетика и уменьшенная побочная активность эффекты.
Кроме того, наночастицы также обладают способностью переносить молекулы лекарств через гематоэнцефалический барьер, что может быть использовано для разработки революционных терапевтических средств для лечения таких клинических состояний, как болезнь Паркинсона, болезнь Альцгеймера, шизофрения и депрессия. Это также вселило надежду на такое сложное заболевание, как опухоль головного мозга, которое в настоящее время невозможно лечить обычными методами доставки лекарств.
Анализ рыночных тенденций показывает, что способность наночастиц значительно улучшать терапевтический результат побудила фармацевтические компании разработать составы в виде наночастиц таких популярных лекарств, как Megace ES (повышенная стабильность), Estrasorb (эмульсия эстрадиола для местного применения) и Triglide (нанокристалл). формулировка Трикора).Составы с наночастицами популярных терапевтических средств против рака, таких как доксорубицин и таксол, также были хорошо приняты в терапевтическом сегменте рака из-за более длительного периода полураспада и снижения побочных эффектов.
Развитие нанотехнологий привело к появлению на рынке многих типов наночастиц. Нанокристаллы и липосомы в настоящее время являются наиболее популярными наночастицами, за ними следуют мицеллы и дендримеры. В настоящее время разрабатываются и продаются лекарственные формы на основе нанокристаллов, липосом и мицелл, что, несомненно, увеличит размер рынка в будущем.
Географический анализ метода доставки лекарств с помощью наночастиц прогнозирует растущее доминирование США, занимающих более 40% мирового рынка, за которыми следует Европа. Однако ожидается, что в течение прогнозируемого периода размер рынка в Азиатско-Тихоокеанском регионе и Латинской Америке увеличится из-за множества факторов роста, поддерживающих анализ, таких как увеличение количества пациентов и растущий интерес ключевых игроков, таких как Johnson & Johnson и Novartis, к регион.
KuicK Research оценивает, что к 2024 году мировой рынок лекарств с использованием наночастиц достигнет более 200 миллиардов долларов при среднегодовом темпе роста 10%.Факторы, способствующие росту, такие как увеличение глобальной распространенности различных клинических показаний, таких как рак, диабет и ревматоидный артрит, неизбежно будут способствовать росту рынка, в котором онкология является доминирующим сегментом. Ожидается, что растущий спрос на эффективные методы лечения для растущего числа пациентов также поможет сегменту сохранить доминирующее положение в прогнозируемом периоде отчета.
Рынок доставки наночастиц лекарств, однако, сталкивается с некоторыми серьезными проблемами, которые, как ожидается, будут препятствовать его дальнейшему росту.Высокий спрос на инвестиции, научные и технические ограничения и перенаселенность поставщиков и маркетинговые проблемы, такие как непомерно высокие цены на терапевтические препараты, ограниченное проникновение на рынок и низкая осведомленность, являются препятствиями, о которых необходимо позаботиться, чтобы повысить потенциал сегмента доставки лекарств на основе наночастиц.
В отчете KuicK Research о глобальном рынке доставки лекарств с использованием наночастиц содержится углубленный анализ рынка с особым акцентом на размере глобального рынка, текущих рыночных тенденциях, динамике и других факторах, которые могут оказать влияние на рынок.Сравнительный анализ цен, дозировок и затрат на терапию оригинальных препаратов с составами наночастиц анализирует многообещающий потенциал доставки лекарств на основе наночастиц, что в конечном итоге доказывает их превосходство.
 №: Р N003558/01
№: Р N003558/01 №: Р N000471/01
№: Р N000471/01


 №: П N011530/01
№: П N011530/01 р-ра д/в/м введения 100 мг: фл. 3 или 5 шт.
р-ра д/в/м введения 100 мг: фл. 3 или 5 шт. ректальные 50 мг: 5 или 10 шт.
ректальные 50 мг: 5 или 10 шт. д/пригот. р-ра д/инф. 5 г/10 мл: амп. 10 шт.
д/пригот. р-ра д/инф. 5 г/10 мл: амп. 10 шт. 0.3 г: фл. 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 шт.
0.3 г: фл. 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 шт. д/пригот. р-ра д/инф. 2 г/5 мл: амп. 10 или 20 шт.
д/пригот. р-ра д/инф. 2 г/5 мл: амп. 10 или 20 шт. 250 мг: 30 или 60 шт.
250 мг: 30 или 60 шт. р-ра д/приема внутрь 1 г: пак. 2, 5 или 10 шт.
р-ра д/приема внутрь 1 г: пак. 2, 5 или 10 шт. 5%: контейн. 250 мл или 500 мл
5%: контейн. 250 мл или 500 мл №: ЛСР-006923/10
№: ЛСР-006923/10 11.11
11.11 р-ра д/в/м, субконъюнктивального введ. и закапывания в глаз 1 млн.МЕ: амп. 5 или 10 шт., фл. 5 шт.
р-ра д/в/м, субконъюнктивального введ. и закапывания в глаз 1 млн.МЕ: амп. 5 или 10 шт., фл. 5 шт. и закапывания в глаз 1 млн.МЕ: амп. 5 или 10 шт., фл. 5 шт.
и закапывания в глаз 1 млн.МЕ: амп. 5 или 10 шт., фл. 5 шт. 52®
52® №: ЛП-002728
№: ЛП-002728 №: ЛП-000068
№: ЛП-000068 , покр. пленочной оболочкой, 250 мг: 10, 20 или 50 шт.
, покр. пленочной оболочкой, 250 мг: 10, 20 или 50 шт. 09.20
09.20 №: ЛП-002691
№: ЛП-002691
 №: Р N001047/03
№: Р N001047/03 375 мг: 30, 50, 100 или 200 шт.
375 мг: 30, 50, 100 или 200 шт. №: П N013091/01
№: П N013091/01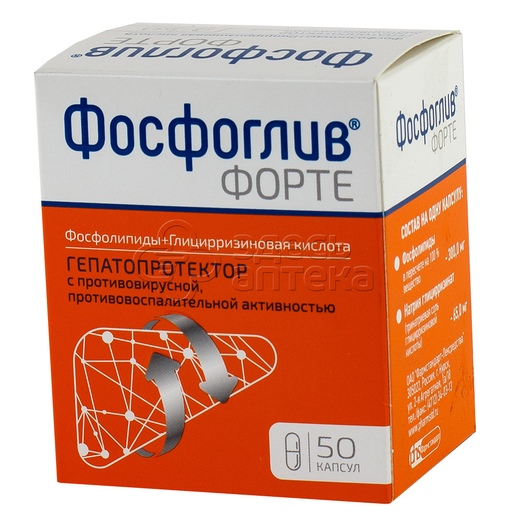 5 мг: 100 шт.
5 мг: 100 шт. 500 млн.КОЕ: банки 6, 10, 18 или 30 шт.
500 млн.КОЕ: банки 6, 10, 18 или 30 шт.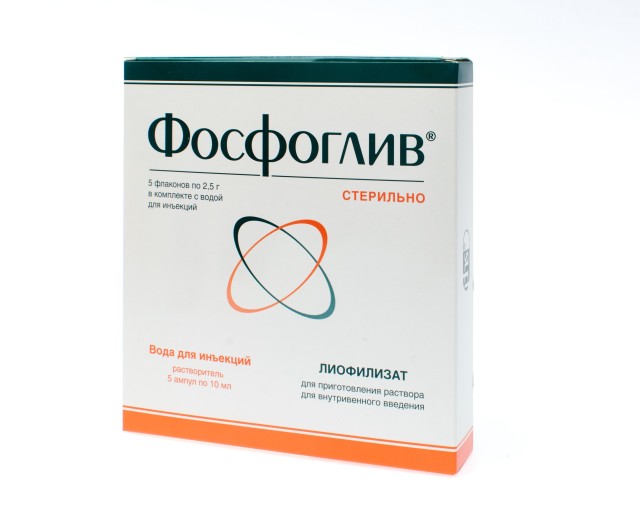 д/пригот. р-ра д/инъекц. и местного прим. 1 млн.МЕ: амп. 5 или 10 шт. фл. 5 шт.
д/пригот. р-ра д/инъекц. и местного прим. 1 млн.МЕ: амп. 5 или 10 шт. фл. 5 шт. №: ЛСР-009341/09
№: ЛСР-009341/09 100 мл
100 мл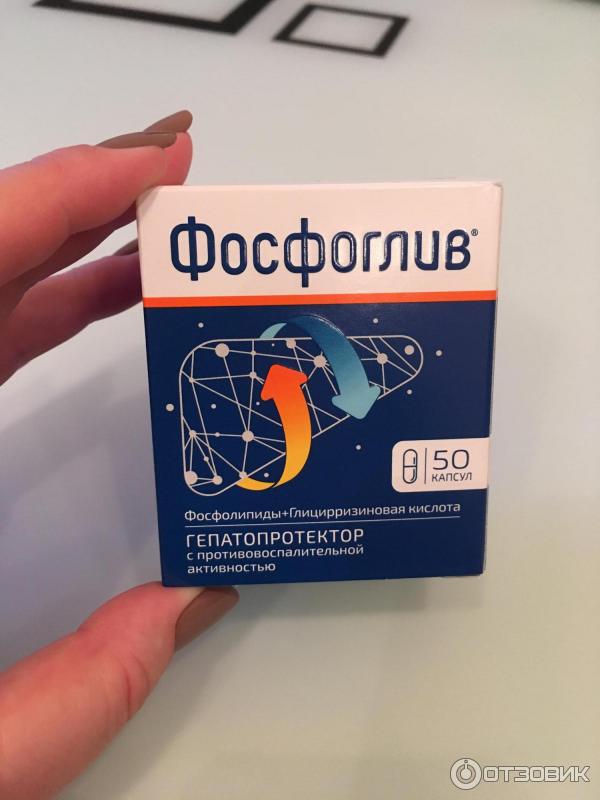 250 мг: 10, 50, 60 или 100 шт.
250 мг: 10, 50, 60 или 100 шт. 08.17
08.17 р-ра д/в/в введения: фл. 2.5 г 5 шт. в компл. с растворителем
р-ра д/в/в введения: фл. 2.5 г 5 шт. в компл. с растворителем №: ЛСР-006426/08
№: ЛСР-006426/08 22.5 г 2, 10 или 20 шт.; тубы 225 г 1 шт.
22.5 г 2, 10 или 20 шт.; тубы 225 г 1 шт.
 5 мл 5, 10, 250 или 500 шт.
5 мл 5, 10, 250 или 500 шт. №: П N015495/01
№: П N015495/01 5%: бут. или фл. 100 мл
5%: бут. или фл. 100 мл №: ЛС-000437
№: ЛС-000437 №: ЛП-002017
№: ЛП-002017
 08.06
08.06 , покр. пленочной оболочкой, 60 мг: 6, 10, 12 или 20 шт.
, покр. пленочной оболочкой, 60 мг: 6, 10, 12 или 20 шт. 14
14 р-ра д/в/в и п/к введения 0.5 мкг: амп. 5 шт.
р-ра д/в/в и п/к введения 0.5 мкг: амп. 5 шт. №: ЛП-003144
№: ЛП-003144 1 000 000 МЕ: 10 шт.
1 000 000 МЕ: 10 шт. №: П N011530/01
№: П N011530/01 р-ра д/в/м введения 100 мг: фл. 3 или 5 шт.
р-ра д/в/м введения 100 мг: фл. 3 или 5 шт. ректальные 50 мг: 5 или 10 шт.
ректальные 50 мг: 5 или 10 шт. №: П N012369/01
№: П N012369/01