Вакцинация против клещевого энцефалита в вопросах и ответах
Для профилактики клещевого энцефалита к использованию в России разрешены следующие вакцины:
Вакцина клещевого энцефалита культуральная очищенная концентрированная инактивированная сухая (производство РФ).
ЭнцеВир (EnceVir) (производство РФ).
ФСМЕ-Иммун Инжект/Джуниор (FSME-Immun Inject/Junior) (производство Австрия).
Энцепур Взрослый и Энцепур Детский (производство Германия).
О вакцинации в вопросах и ответах
В.: Зачем нужна вакцинация против клещевого энцефалита, и в чём разница между привитым и непривитым человеком?
О.: Прививка нужна для того, чтобы обучить иммунную систему определять вирус и бороться с ним. В процессе вакцинации появляются антитела (иммуноглобулины), в случае встречи их с вирусом они его уничтожат.
В.: Кому показана вакцинация? Где ее пройти?
О.: Вакцинация показана клинически здоровым людям (детям с 12 месяцев), проживающим на эндемичной по клещевому энцефалиту территории или пребывающим на ней, после осмотра терапевтом (педиатром). Терапевт (педиатр) также проинформирует вас о том, где можно провести вакцинацию.
Вакцинироваться можно только в учреждениях, имеющих лицензию на этот вид деятельности. Введение вакцины, которая хранилась неправильно (без соблюдения «холодовой цепи») бесполезно, а иногда опасно.
В.: Является ли профилактический осмотр терапевта неотъемлемой частью вакцинации против клещевого энцефалита?
О.: Да, осмотр терапевта крайне желателен. Осмотр должен проходить в день вакцинации, без справки от терапевта в большинстве случаев в прививке отказывают.
В.: Через какое время после перенесенной болезни можно ставить прививку?
О.: Согласно инструкции вакцинацию можно проводить не ранее, чем через 2 недели после выздоровления — импортной вакциной, и не ранее, чем через 1 месяц — отечественной.
В.: У меня хроническое заболевание, возможно ли мне поставить прививку против клещевого энцефалита?
О. : Перечень противопоказаний указан в инструкции к каждой вакцине (инструкции см. ниже). У импортных вакцин противопоказаний меньше, чем у российских. В каждом случае заболевания, не содержащегося в перечне противопоказаний, вакцинация проводится по разрешению врача, исходя из состояния здоровья вакцинируемого и риска заражения клещевым энцефалитом.
: Перечень противопоказаний указан в инструкции к каждой вакцине (инструкции см. ниже). У импортных вакцин противопоказаний меньше, чем у российских. В каждом случае заболевания, не содержащегося в перечне противопоказаний, вакцинация проводится по разрешению врача, исходя из состояния здоровья вакцинируемого и риска заражения клещевым энцефалитом.
Вакцина клещевого энцефалита культуральная очищенная концентрированная инактивированная сухая (производство РФ).
ЭнцеВир (EnceVir) (производство РФ).
ФСМЕ-Иммун Инжект/Джуниор (FSME-Immun Inject/Junior) (производство Австрия).
Энцепур Взрослый, Энцепур Детский (производство Германия).
В.: В чем разница между вакцинами?
О.: Все вакцины для профилактики клещевого энцефалита взаимозаменяемы. Западноевропейские штаммы вируса клещевого энцефалита, из которых готовятся импортные вакцины, и восточноевропейские штаммы, используемые в отечественном производстве, близки по антигенной структуре. Сходство в структуре ключевых антигенов составляет 85%. В связи с этим иммунизация вакциной, приготовленной из одного вирусного штамма, создает стойкий иммунитет против заражения любым вирусом клещевого энцефалита. Эффективность зарубежных вакцин в России подтверждена, в том числе исследованиями с использованием российских диагностических тест-систем. У импортных вакцин меньше перечень противопоказаний и частота побочных реакций, они лучше переносятся.
В.: Лучшее время для вакцинации?
О.: Вакцинироваться против клещевого энцефалита можно круглый год, но планировать вакцинацию нужно таким образом, чтобы с момента второй прививки прошло не менее 2 недель до возможной встречи с клещом. Если вы только планируете начать вакцинацию, то для достижения иммунитета вам потребуется минимум 21-28 дней — при экстренной схеме вакцинации, при стандартной — минимум 45 дней.
В.: Мне была сделана прививка против клещевого энцефалита, но название вакцины я не помню. Что делать? Какую ставить вакцину?
О. : Все вакцины против клещевого энцефалита взаимозаменяемы.
: Все вакцины против клещевого энцефалита взаимозаменяемы.
В.: Я привит от клеща, значит ли это, что теперь они мне совсем не страшны?
О.: Нет! Прививок от клещей не существует! Существует лишь прививка от клещевого энцефалита, она способна защитить человека не менее, чем в 95% случаев но лишь от клещевого энцефалита, а не от всех болезней, переносимых клещами. Поэтому не стоит пренебрегать элементарными правилами профилактики укусов клещей и лишний раз подвергать себя опасности их укусов.
В.: Я поставил только одну прививку (или еще не прошло 2 недель с момента второй), но меня укусил клещ. Что делать?
О.: Одна прививка не может защитить от клещевого энцефалита, поэтому вам необходимо поступить, как непривитому человеку.
В.: На основе каких анализов можно судить о наличии иммунитета к клещевому энцефалиту?
О.: Можно сдать кровь на антитела IgG к клещевому энцефалиту. При титрах 1:200 — 1:400 принято считать, что у пациента создан минимальный протективный уровень специфических антител. При титрах 1:100 или отрицательном результате считается, что иммунитет к клещевому энцефалиту отсутствует.
Схема вакцинации клещевого энцефалита
В.: Как правильно пройти вакцинацию? Какую выбрать схему вакцинации?
О.: В первую очередь нужно следовать рекомендациям вашего врача и указаниям инструкции к выбранной вами вакцине.
Стандартная схема вакцинации клещевого энцефалита состоит из 3 доз, которые вводятся по схеме 0-1(3)-9(12) месяцев — для импортных, и 0-1(7)-(12) — для отечественных вакцин; ревакцинация проводится каждые 3 года.
Для формирования иммунитета большинству прививаемых достаточно 2 прививок с интервалом в 1 мес. Стойкий иммунитет к клещевому энцефалиту появляется через две недели после введения второй дозы, независимо от вида вакцины и выбранной схемы.
Однако для выработки полноценного и длительного (не менее 3 лет) иммунитета необходимо сделать третью прививку через год после второй.
Экстренная схема вакцинации клещевого энцефалита
Для большинства вакцин разработана экстренная схема вакцинации (см. инструкцию). Целью применения экстренной схемы является быстрое достижение защитного эффекта, в случаях, когда сроки стандартной вакцинации были упущены.
инструкцию). Целью применения экстренной схемы является быстрое достижение защитного эффекта, в случаях, когда сроки стандартной вакцинации были упущены.
Быстрее всего иммунитет к клещевому энцефалиту появится при экстренной вакцинации Энцепуром — через 21 день. При экстренной вакцинации ФСМЕ-ИММУН или Энцевиром — через 28 дней.
Вакцина, введенная по экстренной схеме, создает такой же стойкий иммунитет, как и при стандартной схеме вакцинации.
Вакцинация способна реально защитить около 95% привитых. В случаях возникновения заболевания у привитых людей оно протекает легче и с меньшими последствиями. Однако следует помнить, что вакцинация против клещевого энцефалита не исключает всех остальных мер профилактики укусов клещей (репелленты, надлежащая экипировка), поскольку клещи переносят не только клещевой энцефалит, но и другие инфекции, от которых нельзя защититься вакцинацией.
Ревакцинация
После стандартного первичного курса из 3-х прививок стойкий иммунитет сохраняется как минимум 3 года.
Ревакцинация против клещевого энцефалита проводится каждые 3 года после третьей прививки.
Ревакцинация осуществляется путем однократного введения стандартной дозы вакцины.
В случае, когда была пропущена одна ревакцинация (1 раз в 3 года), весь курс заново не проводится, делается лишь одна прививка-ревакцинация. Если было пропущено 2 плановых ревакцинации, курс прививок против клещевого энцефалита проводится заново.
Согласно профессиональной технике безопасности для выезжающих на полевые работы в эндемичные регионы с целью сохранения высокого уровня антител ревакцинация проводится ежегодно.
Побочные реакции на вакцинацию
В.: Насколько часто встречаются аллергические реакции на вакцину, и как они проявляются?
К местным побочным реакциям относятся покраснение, уплотнение, болезненность, отек в месте введения вакцины. Также к местным реакциям относят крапивницу (аллергическая сыпь, напоминающая таковую при ожоге крапивы), увеличение близлежащих от места укола лимфоузлов. Обычные местные реакции отмечаются у 5% прививаемых. Длительность таких реакций может достигать 5 дней.
Обычные местные реакции отмечаются у 5% прививаемых. Длительность таких реакций может достигать 5 дней.
К общим поствакцинальным реакциям относят охватывающую значительные участки тела сыпь, повышение температуры тела, беспокойство, нарушения сна и аппетита, головную боль, головокружение, кратковременную потерю сознания, цианоз (посинение кожи и слизистых), похолодание конечностей. Частота температурных реакций (более 37,5°С) на российские вакцины не превышает 7%.
Для российских вакцин существует рекомендация о наблюдении за привитыми в течение 1 часа в связи с риском развития аллергических реакций.
Импортные вакцины переносятся лучше, частота побочных реакций у них меньше.
В.: После прививки второй день держится температура 37,5 °С, болит голова и ломота во всем теле.
Можно ли принять аспирин или обезболивающее?
О.: Такое случается. Подобное состояние может наблюдаться в течении нескольких дней, однако не всегда плохое самочувствие связано с вакцинацией… Обратитесь к врачу. В случае, если причина вашего недомогания действительно в прививке, то можно принять аспирин или обезболивающее.
В.: Первую прививку перенес очень тяжело, болел 3 дня. При следующих прививках состояние будет таким же?
О.: Обычно вторая и последующие прививки переносятся легче, но риск возникновения побочных реакций присутствует.
Нарушение сроков вакцинации
В.: Два года назад поставил одну прививку, вторую и последующие ставить не стал. В этом году решил продолжить вакцинацию. Проходить полный курс сначала?
О.: Да. В случае, если в указанные сроки не была поставлена вторая прививка (см. инструкцию) после первой, то необходимо пройти полный курс вакцинации.
В.: Была поставлена первая прививка против клещевого энцефалита. Вторую прививку врач рекомендовал поставить через месяц, но я не пришел, так как серьезно болел. На сегодняшний день (прошло 3 месяца после первой прививки) я поправился. Можно ли поставить вторую прививку сейчас?
О. : Производителями вакцин разработаны схемы вакцинации, именно они многократно опробованы и оптимальны для получения наилучшего иммунитета, и этих сроков стоит придерживаться.
: Производителями вакцин разработаны схемы вакцинации, именно они многократно опробованы и оптимальны для получения наилучшего иммунитета, и этих сроков стоит придерживаться.
В инструкции к вакцине указывается не конкретный день следующей вакцинации, а интервал времени.
Для второй прививки согласно инструкции он составляет 1-7 месяцев — для отечественных вакцин, 1-3 месяца — для импортных.
Третья прививка — через 9-12 месяцев после второй.
Но в случае необходимости эти сроки можно незначительно изменять (1-2 месяца).
В.: Прошел первичную вакцинацию (3 прививки, как указано в инструкции), нужно было пройти ревакцинацию через 3 года после последней прививки, но этого я не сделал (забыл). Как быть? Проходить весь курс вакцинации сначала?
О.: Если после полного первичного курса вакцинации прошло от 3 до 5 лет, то достаточно однократной ревакцинации. Если прошло 6 лет и более, то вакцинация против клещевого энцефалита проводится заново.
Взаимодействие
В.: Возможно ли совмещать с другими прививками прививку против клещевого энцефалита?
О.: Допускается одновременное введение вакцины против клещевого энцефалита и введение других инактивированных (кроме антирабических) вакцин отдельными шприцами в разные участки тела. Но по возможности этого делать не стоит, постарайтесь повременить со следующей прививкой не менее 1 месяца.
В.: На завтра назначена вакцинация от клещевого энцефалита. Сегодня сделали Манту, можно завтра поставить прививку или повременить. Если ждать, то сколько?
О.: Проба Манту не должны проводиться одновременно с какими бы то ни было прививками — увеличивается риск ложноположительных реакций.
Сразу после оценки результатов пробы, прививки могут проводиться без ограничений.
В.: Мне поставили укол иммуноглобулина против клещевого энцефалита. Через какое время можно поставит прививку?
О.: После введения иммуноглобулина против клещевого энцефалита необходимо соблюдение интервала не менее 4-х недель перед прививкой, в противном случае уровень специфических антител может быть снижен.
В.: Можно ли привитому человеку поставить иммуноглобулин после укуса? Какие негативные последствия могут быть?
О.: Иммуноглобулин получают из крови привитых доноров. Привитому человеку нет смысла ставить иммуноглобулин. Именно поэтому в европейских странах с высоким процентом вакцинированного населения полностью прекращен выпуск иммуноглобулина против клещевого энцефалита.
Существует мнение, что чужеродные антитела могут привести к сбою собственной иммунной системы. Но отрицательное влияние иммуноглобулина на развитие клещевого энцефалита у привитых людей не доказано. Однако точно известно о достаточно частых негативных реакциях в ответ на введение здоровым людям иммуноглобулина – вплоть до анафилактического шока.
В.: Сколь дней после прививки против клещевого энцефалита нельзя употреблять алкоголь?
О.: На развитии иммунитета прием алкоголя не скажется. В меру употреблять можно. Большие же дозы алкоголя могут ослабить иммунную систему и увеличить риск возникновения побочных реакций на прививку.
Вакцина против клещевого энцефалита и беременность
В.: Через неделю после прививки против клещевого энцефалита узнала, что беременна. Что делать? Как это отразится на ребенке? Сохранять беременность или нет?
О.: Особого повода для беспокойства нет. Отрицательное влияние прививок не доказано. Хотя намеренно ставить прививку, зная о беременности, не стоит (за исключением случаев, когда польза от вакцинации заметно выше возможного вреда), так как ее влияние пока недостаточно изучено, именно поэтому в противопоказаниях некоторых вакцин и значится беременность.
В.: Через какое время после прививки можно начинать планировать ребенка?
О.: Доказанных фактов влияния вакцинации против клещевого энцефалита на плод и сперму нет, но в противопоказаниях к вакцинам значится беременность. Лучше подождать 1 месяц.
Вакцина против клещевого энцефалита и период лактации
В.: Я — кормящая мать, ребенку 5 месяцев. Когда можно пройти вакцинацию?
Когда можно пройти вакцинацию?
О.: В вашем случае лучше выбрать импортную вакцину (Энцепур, FSME-Immun Inject), обязательно проконультироваться с педиатром и терапевтом. Вакцина назначается кормящим женщинам с осторожностью, после тщательной оценки возможного риска и пользы. Если риск пострадать от укуса клеща невелик, то лучше подождать достижения ребенком 1 года.
Вакцинация детей
В.: Какая вакцина будет оптимальной для ребенка в возрасте 1 года? Можно ли прививаться или лучше подождать до 3-х лет?
О.: Несмотря на то, что выпускаются вакцины для детей (FSME-Immun Junior, Энцепур Детский) и их применение разрешено с 1 года, решение о вакцинации должен с осторожностью принимать врач-педиатр, после тщательной оценки возможного риска и пользы. Если риск пострадать от укуса клеща невелик, то лучше подождать достижения ребенком возраста 2-3 лет.
Вакцина против клещевого энцефалита и животные
В.: Можно ли поставить прививку против клещевого энцефалита собаке (кошке)?
О.: Вакцинация животных не проводится! Влияние вируса клещевого энцефалита на собак и кошек пока мало изучено. Есть сведения о том, что они тоже восприимчивы к вирусу, однако случаи заражения крайне редки. Для собак главную опасность представляют другие заболевания передаваемые клещами: пироплазмоз, боррелиоз, бабезиоз.
Клещевой энцефалит — «Семейная клиника №1», г. Южно-Сахалинск
КЛЕЩЕВОЙ ЭНЦЕФАЛИТ. ПОЧЕМУ ВАЖНА ВАКЦИНАЦИЯ?
Живя в городе, мы не задумываемся о над тем, как страшен может быть укус клеща. Кровососущее, является переносчиком опасной инфекции, которая поражает спинной и головной мозг.
Энцефалит вызывает лихорадочные состояния, судороги, рвоту, нарушает координацию движений. Обычный выезд на природу, для не привитого человека, может закончиться плачевно. Ведь отличить обычного клеща от энцефалитного, могут только специалисты в лаборатории.
ПРИЗНАКИ ЗАБОЛЕВАНИЯ ЭНЦЕФАЛИТОМ
После укуса клещом, нужно обязательно обратиться в больницу для поверки членистоногого на наличие инфекции. Инкубационный период развития патологии составляет от 7 до 14 дней. В редких случаях бывает острая реакция. Симптомы заболевания схожи с гриппом: слабость, озноб, боли в мышцах, повышенная температура и даже рвота. Кожа может покраснеть, а сосуды в глазах начинают лопаться. Развитие болезни зависит от формы клещевого энцефалита (очаговой, лихорадочно или менингеальной).
Инкубационный период развития патологии составляет от 7 до 14 дней. В редких случаях бывает острая реакция. Симптомы заболевания схожи с гриппом: слабость, озноб, боли в мышцах, повышенная температура и даже рвота. Кожа может покраснеть, а сосуды в глазах начинают лопаться. Развитие болезни зависит от формы клещевого энцефалита (очаговой, лихорадочно или менингеальной).
КОГДА ЛУЧШЕ ПРИВИВАТЬСЯ ОТ КЛЕЩЕВОГО ЭНЦЕФАЛИТА?
Вакцинация против клещевого энцефалита входит в Национальный календарь прививок по эпидемиологическим показаниям.
Оптимальным временем для вакцинации является февраль или март. Привиться лучше за 44 дня до выезда на природу или дачу. Клещи просыпаются весной, когда температура устанавливается в районе 3 градусов тепла. Активными они становятся уже при +10 °C.
Вакцинация подразумевает три этапа введения препарата.
1. Первая ставится в определенное вами время (напоминаем, что желательно сделать её в феврале или марте. До наступления теплого периода).
2. Через 1 месяц ставится вторая доза препарата.
3. Последняя вакцинация производится через 9-12 месяцев от первой прививки.
Пожизненного иммунитета против энцефалита нет. Поэтому ревакцинация необходима спустя три года.
Так же, есть и экстренная вакцинация. Когда пациента вводится две дозы препарата с промежутком в 2-3 недели. Третья прививка рекомендована через 1 год.
О СОСТАВЕ ВАКЦИНЫ
В составе вакцины против клещевого энцефалита находится штамм арбовируса. Выращивают его на куриных белках и инактивируют (дословно – убивают) формалином.
Препарат не содержит консервантов. Хранится при низких температурах. Есть два варианта дозировки:
— Для взрослых. Ампулы по 0,5 мл.
— Для детей от 1 года до 16 лет. Ампула по 0,25мл.
КОМУ НУЖНО ПРИВИВАТЬСЯ ОТ КЛЕЩЕВОГО ЭНЦЕФАЛИТА?
От укуса клеща не застрахован никто. Поэтому мы рекомендуем привиться всем, кто проживает на эндемичной территории распространения болезни. Не зависимо от того, как часто вы бываете природе. Прививка от клещевого энцефалита разрешена детям от 1 года.
Не зависимо от того, как часто вы бываете природе. Прививка от клещевого энцефалита разрешена детям от 1 года.
ПРОТИВОПОКАЗАНИЯ ДЛЯ ВАКЦИНАЦИИ
Как и у любой вакцины, у прививки от клещевого энцефалита есть свои противопоказания.
— Недавно перенесенные операции или болезни.
— Аллергическая реакция на поставленную ранее вакцину.
— Непереносимость куриного белка.
— Беременность и кормление грудью.
— Острые заболевания в период вакцинации.
Перед вакцинацией обязательна консультация у врача. Именно он принимает решение о вакцинации, основываясь на ваших показателях здоровья.
КАКИЕ БЫВАЮТ ПОБОЧНЫЕ ЭФФЕКТЫ ОТ ПРИВИВКИ?
Помимо противопоказаний, важно знать, что вакцина от клещевого энцефалита может вызвать побочные эффекты. Впрочем, как и любая другая вакцина. Это могут быть:
— Покраснения в месте введения препарата, небольшая припухлость, зуд.
— Слабость или тошнота.
— Головная боль.
— Повышение температуры.
— Увеличение лимфоузлов.
После того, как вам ввели вакцину, следует быть под наблюдением специалиста первые 30 минут. При ухудшении состояния обратиться к врачу, который ставил прививку.
В НАШЕЙ КЛИНИКЕ ВЫ МОЖЕТЕ ПРИВИТЬСЯ СЛЕДУЮЩИМИ ВАКЦИНАМИ:
1. Клещ-Э-Вак (для детей и для взрослых)
2. Энцевир (для взрослых)
Сделать прививку можно по адресу г. Южно-Сахалинск, ул. Емельянова, 21а (см. на карте).
ЗАПИСАТЬСЯ НА ВАКЦИНАЦИЮ МОЖЕТЕ:
— по номеру телефона 240-250, 220-600
— заказать обратный звонок
— написать нам WhatsApp
Прививка от клещевого энцефалита для детей и взрослых в клинике МедиАрт в ЗАО Москвы
Вакцинация от клещевого энцефалита
Клещевой энцефалит (весенне-летний клещевой менингоэнцефалит) – природно-очаговая вирусная инфекция, характеризующаяся лихорадкой, интоксикацией и поражением серого вещества головного мозга (энцефалит) и/или оболочек головного и спинного мозга (менингит и менингоэнцефалит).
Заболевание может привести к стойким неврологическим и психиатрическим осложнениям и даже к смерти больного.
Носителями вируса по статистике являются шесть клещей из ста (при этом заболеть от заражённой особи могут от 2 до 6% укушенных людей).
К сожалению, в Москве и Московской области проблема заболеваний клещевым энцефалитом с каждым годом становится все более актуальной. Причина этому — отсутствие вакцинации и позднее обращение за медицинской помощью, а также не серьезное отношение к укусам клещей со стороны людей.
За последние 3 года в медицинские учреждения города Москвы обратилось более 48000 человек с жалобами на присасывание клещей, из них более 9000 дети до 17 лет.
Роспотребнадзор в 2017 году провел работы по сбору и исследованию клещей на территории лесного массива между Рублевским шоссе, ул. Крылатская, ул. Осенняя, МКАД и ЦБК (ул. Маршала Тимошенко).
За август- сентябрь 2017 года с растительности было собрано 227 клещей. Вирус клещевого энцефалита был обнаружен в 5 клещах. Также в октябре 2017 года в лесном массиве вдоль ул. Осенняя были проведены отловы мелких млекопитающих. Было отловлено 44 зверька, из них в тканях мозга 2 рыжих полевок был обнаружен вирус клещевого энцефалита.
Исследование указывает на возможность заражения клещевым энцефалитом даже при укусах клещей на прогулке в лесо-парковых зонах Москвы.
Специального (специфического) лечения от вирусного клещевого энцефалита не существует! Защититься от клещевого энцефалита позволяет вакцинация.
Вакцинация от клещевого энцефалита
Вакцина является надежным, проверенным средством и практически исключает заражение, но все это происходит только при правильной и своевременной вакцинации. Вакцина вводится в несколько этапов и начинает действовать не сразу.
При вакцинации от клещевого энцефалита пациент практически на 100% защищён от этой болезни, но если все же укус произойдет, то вытащенного клеща все равно стоит сдать на проверку, так как клещи переносят и другие болезни.
Плановая вакцинация от клещевого энцефалита состоит из нескольких этапов:
-
Делается первый укол (первичное введение препарата) -
Через 2-4 недели делается второй укол (повторное введение препарата)
Иммунитет от клещевого энцефалита начинает действовать через 2 недели после второго укола (повторного введения препарата)
Для поддержания иммунитета следует повторить укол весной следующего года. Далее укол необходимо делать 1 раз в 3 года.
Плановая вакцинация имеет ряд достоинств:
-
Препарат может вводиться детям от 1 года (для взрослых ограничений по возрасту нет) -
Небольшой (0,25 мл у детей и 0,5 мл у взрослых) объем вводимого препарата -
Хорошая переносимость (в первые 3 суток возможны незначительные местные реакции – покраснение и болезненность, температура поднимается крайне редко) препарата -
Высокая эффективность: правильно выполненный курс вакцинации надежно защищает от вирусного клещевого энцефалита
Из недостатков плановой вакцинации стоит назвать время выработки антител. Вакцина начинает действовать (в организме вырабатываются антитела) через две недели после повторного введения препарата. Т.е. организм становится защищен от энцефалита через 1-1,5 месяца после первого введения препарата. Поэтому плановую вакцинацию делать начинают заранее с февраля.
В сети клиник для детей и взрослых МедиАрт пациентам пришедшим на плановую вакцинацию вводится препарат «Клещ-Э-Вак ». Препарат показал свою надежность и зарекомендовал с самой лучшей стороны.
Данный препарат можно вводить, даже если до этого вы использовали другую вакцину. Единственное условие (кроме врачебных показаний) – это временной интервал между последней прививкой (любой) и введением вакцины должен быть не менее 1 месяца.
Единственное условие (кроме врачебных показаний) – это временной интервал между последней прививкой (любой) и введением вакцины должен быть не менее 1 месяца.
Противопоказания при плановой вакцинации от клещевого энцефалита:
-
острые заболевания или обострение хронических заболеваний, -
непереносимость компонентов препарата.
Делать плановую вакцинацию или довериться воли случая – выбор за вами. Но учитывайте, часто так бывает, что вы отвечаете не только за себя, но и за членов своей семьи – детей, родителей.
Стоит ли рисковать их жизнями или лучше сделать несколько уколов и не бояться ходить по паркам, лесам и приусадебным участкам — выбор за вами.
Если вы захотите проконсультироваться в этом вопросе со специалистом, позвоните нам по телефону 8 (495) 2-876-000 и запишитесь на консультацию врача.
Прививка от клещевого энцефалита детям, цены в Москве в клинике ИММА
Записаться на прием
Клещевой энцефалит – заболевание, вызываемое вирусами и поражающее спинной, головной мозг и его оболочки, периферические нервы и нервные корешки. Энцефалит может привести к необратимым неврологическим и психологическим осложнениям, а порой и к летальному исходу. Носителями вируса являются иксодовые клещи, пик максимальной численности и активности которых приходится на май, июнь и конец августа, сентябрь, октябрь. Заразиться можно не только при укусе клеща, но и при попытке извлечь впившееся насекомое, после употребления непастеризованного молока от животного.
Защита от энцефалита
Специфического лечения от клещевого энцефалита нет. С целью профилактики необходимо проводить само- и взаимоосмотры (во время и после прогулки на природе), носить головной убор, высокую обувь, одежду светлых тонов, закрывающую все тело. Можно использовать репеллентные или акарицидные препараты, отпугивающие или уничтожающие клещей. На коляску с малышом желательно надевать москитную сетку для защиты от клеща. Молоко от домашних коров и коз обязательно нужно кипятить.
Можно использовать репеллентные или акарицидные препараты, отпугивающие или уничтожающие клещей. На коляску с малышом желательно надевать москитную сетку для защиты от клеща. Молоко от домашних коров и коз обязательно нужно кипятить.
Наиболее надежной мерой профилактики является вакцинация. Прививку от клещевого энцефалита делают весной или осенью. Вакцинация особенно актуальна пациентам, проживающим в лесных районах России, Украины, Казахстана, Белоруссии, Киргизии, Прибалтики. Вакцинация рекомендуется не только жителям эндемичных регионов (мест обитания иксодовых клещей и распространения клещевого энцефалита), но и тем, кто собирается уехать на Урал, Дальний Восток, в Сибирь, Калининградскую область.
Прививки от клещевого энцефалита выполняются при достижении ребенком 1 года. Их можно совмещать с инъекциями по графику вакцинации детей. Об активной иммунизации ребенка следует позаботиться заранее, за 1 месяц до сезона активности клещей. Инъекция выполняется трижды в дельтовидную мышцу плеча. Эффект вакцинации сохраняется на 3 года, далее следует проводить ревакцинацию от энцефалита через каждые 3–5 лет.
Важное о вакцинации против клещевого энцефалита!
Зачем нужна вакцинация?
Прививка от клещевого энцефалита (как и любая другая) нужна для того, чтобы обучить иммунную систему определять вирус и бороться с ним. В процессе вакцинации появляются АТ (иммуноглобулины), в случае встречи их с вирусом они его уничтожат.
Кому показана вакцинация? Где ее пройти?
Вакцинация показана клинически здоровым людям (детям с 12 мес.), Вакцинироваться можно только в ЛУ, имеющих лицензию на этот вид деятельности. Введение вакцины, которая хранилась неправильно (без соблюдения «холодовой цепи») бесполезно, а иногда опасно.
Является ли профилактический осмотр терапевта неотъемлемой частью вакцинации против клещевого энцефалита?
Да, осмотр терапевта крайне желателен. Осмотр должен проходить в день вакцинации, без справки от терапевта в большинстве случаев в прививке отказывают.
Через какое время после перенесенной болезни можно ставить прививку?
Согласно инструкции вакцинацию можно проводить не ранее, чем через 2 недели после выздоровления — импортной вакциной, и не ранее, чем через 1 месяц — отечественной.
Можно ли ставить прививку против клещевого энцефалита при наличии хронического заболевания?
Перечень противопоказаний указан в инструкции к каждой вакцине. У импортных вакцин противопоказаний меньше, чем у российских. В каждом случае заболевания, не содержащегося в перечне противопоказаний, вакцинация проводится по разрешению врача, исходя из состояния здоровья вакцинируемого и риска заражения клещевым энцефалитом.
В чем разница между вакцинами?
Виды вакцин:
1) Вакцина клещевого энцефалита культуральная очищенная концентрированная инактивированная сухая (производство РФ).
2) ЭнцеВир (EnceVir) (производство РФ).
3) ФСМЕ-Иммун Инжект/Джуниор (FSME-Immun Inject/Junior) (производство Австрия).
4) Энцепур Взрослый, Энцепур Детский (производство Германия).
Все вакцины для профилактики клещевого энцефалита взаимозаменяемы. Сходство в структуре ключевых антигенов вакцин составляет 85%. Эффективность зарубежных вакцин в России подтверждена. У импортных вакцин меньше перечень противопоказаний и частота побочных реакций, они лучше переносятся.
Лучшее время для вакцинации?
Вакцинироваться против клещевого энцефалита можно круглый год, но планировать вакцинацию нужно таким образом, чтобы с момента второй прививки прошло не менее 2 недель до возможной встречи с клещом. Если вы только планируете начать вакцинацию, то для достижения иммунитета вам потребуется минимум 21-28 дней — при экстренной схеме вакцинации, при стандартной — минимум 45 дней.
Если привит от клеща, значит ли это, что теперь они человеку совсем не страшны?
Нет! Прививок от клещей не существует! Существует лишь прививка от клещевого энцефалита, она способна защитить человека не менее, чем в 95% случаев но лишь от клещевого энцефалита, а не от всех болезней, переносимых клещами. Поэтому не стоит пренебрегать элементарными правилами профилактики укусов клещей и лишний раз подвергать себя опасности их укусов.
Поэтому не стоит пренебрегать элементарными правилами профилактики укусов клещей и лишний раз подвергать себя опасности их укусов.
Если поставили только одну прививку (или еще не прошло 2 недель с момента второй), но укусил клещ. Что делать?
Одна прививка не может защитить от клещевого энцефалита, поэтому необходимо поступать, как непривитому человеку.
Как правильно пройти вакцинацию? Какую выбрать схему вакцинации?
Стандартная схема вакцинации клещевого энцефалита состоит из 3 доз, которые вводятся по схеме 0-1(3)-9(12) месяцев — для импортных, и 0-1(7)-(12) — для отечественных вакцин; ревакцинация проводится каждые 3 года.
Для формирования иммунитета большинству прививаемых достаточно двух прививок с интервалом в 1 мес. Стойкий иммунитет к клещевому энцефалиту появляется через две недели после введения второй дозы, независимо от вида вакцины и выбранной схемы.
Однако для выработки полноценного и длительного (не менее 3 лет) иммунитета необходимо сделать третью прививку через год после второй.
Экстренная схема вакцинации клещевого энцефалита
Целью применения экстренной схемы является быстрое достижение защитного эффекта, в случаях, когда сроки стандартной вакцинации были упущены.
Быстрее всего иммунитет к клещевому энцефалиту появится при экстренной вакцинации Энцепуром — через 21 день. При экстренной вакцинации ФСМЕ-ИММУН или Энцевиром — через 28 дней.
Вакцина, введенная по экстренной схеме, создает такой же стойкий иммунитет, как и при стандартной схеме вакцинации.
Вакцинация способна реально защитить около 95% привитых. В случаях возникновения заболевания у привитых людей оно протекает легче и с меньшими последствиями. Однако следует помнить, что вакцинация против клещевого энцефалита не исключает всех остальных мер профилактики укусов клещей (репелленты, надлежащая экипировка), поскольку клещи переносят не только клещевой энцефалит, но и другие инфекции, от которых нельзя защититься вакцинацией.
Ревакцинация
После стандартного первичного курса из 3-х прививок стойкий иммунитет сохраняется как минимум 3 года.
Ревакцинация против клещевого энцефалита проводится каждые 3 года после третьей прививки и осуществляется путем однократного введения стандартной дозы вакцины.
В случае, когда была пропущена одна ревакцинация (1 раз в 3 года), весь курс заново не проводится, делается лишь одна прививка-ревакцинация. Если было пропущено 2 плановых ревакцинации, курс прививок против клещевого энцефалита проводится заново.
Нарушение сроков вакцинации
В случае, если в указанные сроки не была поставлена вторая прививка после первой, то необходимо пройти полный курс вакцинации.
Для второй прививки согласно инструкции он составляет 1-7 месяцев — для отечественных вакцин, 1-3 месяца — для импортных.
Третья прививка — через 9-12 месяцев после второй.
Но в случае необходимости эти сроки можно незначительно изменять (1-2 месяца).
Если после полного первичного курса вакцинации прошло от 3 до 5 лет, то достаточно однократной ревакцинации. Если прошло 6 лет и более, то вакцинация против клещевого энцефалита проводится заново.
Профилактика клещевого вирусного энцефалита — ДЗМ
Весеннее пробуждение природы сопровождается подъёмом биологической активности животных, птиц и членистоногих, которые являются источниками либо переносчиками различных инфекционных заболеваний. Риск заражения человека отдельными инфекционными болезнями при тесном контакте с природой многократно увеличивается.
Одной из больших опасностей для москвичей за городом являются клещи – переносчики целого ряда инфекционных заболеваний, в том числе самого опасного из них — клещевого вирусного энцефалита (КВЭ). Клещевой вирусный энцефалит – это острое вирусное инфекционное заболевание, характеризующееся лихорадкой, интоксикацией, поражением вещества и оболочек головного и спинного мозга. Исход заболевания зависит от объёма поражения центральной нервной системы. В 25-30% случаев заболевание заканчивается смертью больного. Также возможно развитие серьезных осложнений (параличей, эписиндрома, снижения интеллекта), приводящих к инвалидизации человека.
Исход заболевания зависит от объёма поражения центральной нервной системы. В 25-30% случаев заболевание заканчивается смертью больного. Также возможно развитие серьезных осложнений (параличей, эписиндрома, снижения интеллекта), приводящих к инвалидизации человека.
Где можно заразиться клещевым вирусным энцефалитом?
Ареал обитания клещей – переносчиков клещевого вирусного энцефалита – достаточно широк и захватывает многие административные территории Российской Федерации. За природными территориями, населёнными клещами, ведётся плановое наблюдение с исследованием клещей на наличие вируса клещевого энцефалита. Отдельные территории являются благополучными по КВЭ, в других – при исследовании клещей регулярно выделяется вирус клещевого энцефалита. Территории, где обитают клещи, заражённые вирусом, определены как эндемичные.
С перечнем территорий нашей страны, эндемичных по клещевому вирусному энцефалиту, можно ознакомиться на сайте Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека: https://rospotrebnadzor.ru/deyatelnost/epidemiological-surveillance/?ELEMENT_ID=13603
Эндемичные районы Московской области по клещевому энцефалиту -Дмитровский и Талдомский.
Начало активности клещей совпадает с появлением в лесу первых проталин, поэтому уже в апреле возможны первые укусы. С каждым днём количество активных клещей увеличивается, достигая пика в мае, и остается высокой до середины или конца июня. Поэтому наиболее опасны выезды на природу в майские праздники.
К заражению КВЭ восприимчивы все люди, независимо от возраста и пола.
Как можно защититься от клещевого энцефалита?
Наиболее эффективным средством защиты от клещевого вирусного энцефалита является вакцинация. Всем лицам, планирующим выезд в эндемичные по клещевому энцефалиту территории, необходимо заранее сделать профилактические прививки против клещевого энцефалита.
Вакцинация проводится двукратно с минимальным интервалом между первой и второй прививками 1 месяц и ревакцинацией через год. Последующие ревакцинации проводятся каждые 3 года. Для выработки иммунитета требуется не менее двух недель, поэтому завершить прививочный курс (две прививки) против клещевого энцефалита необходимо за 2 недели до выезда в неблагополучную территорию.
Последующие ревакцинации проводятся каждые 3 года. Для выработки иммунитета требуется не менее двух недель, поэтому завершить прививочный курс (две прививки) против клещевого энцефалита необходимо за 2 недели до выезда в неблагополучную территорию.
Где и когда можно получить профилактические прививки против КВЭ?
Вакцинация осуществляется бесплатно в медицинских организациях по месту прикрепления.
Вакцинация проводится круглогодично, без календарных ограничений, т.е. если летом вы планируете поездку в эндемичный район, то уже зимой можно пройти вакцинацию против клещевого энцефалита в поликлинике по месту прикрепления.
Прививаются:
Лица, проживающие на эндемичных по клещевому вирусному энцефалиту территориях; лица, выезжающие на эндемичные по клещевому вирусному энцефалиту территории, а также прибывшие на эти территории лица, выполняющие следующие работы:
— сельскохозяйственные, гидромелиоративные, строительные, по выемке и перемещению грунта, заготовительные, промысловые, геологические, изыскательские, экспедиционные, дератизационные и дезинсекционные;
— по лесозаготовке, расчистке и благоустройству леса, зон оздоровления и отдыха населения.
Лица, работающие с живыми культурами возбудителя клещевого энцефалита.
Приказ Минздрава от 21032014 125н.pdf
Позаботьтесь о своём здоровье заранее!
Что делать и куда обращаться, если произошло присасывание клеща?
Не следует самостоятельно удалять клеща, необходимо немедленно обратиться в ближайший травматологический пункт. Там вам окажут квалифицированную медицинскую помощь и решат вопрос о необходимости проведения экстренной серопрофилактики (введение иммуноглобулина против клещевого энцефалита).
Экстренная серопрофилактика КВЭ проводится в случае присасывания клеща на эндемичной территории лицам:
— не привитым против КВЭ или получившим неполный курс вакцинации;
— привитым в случае повышенного риска заражения (выявлено инфицирование присосавшегося клеща, многократные укусы или одновременное присасывание нескольких клещей).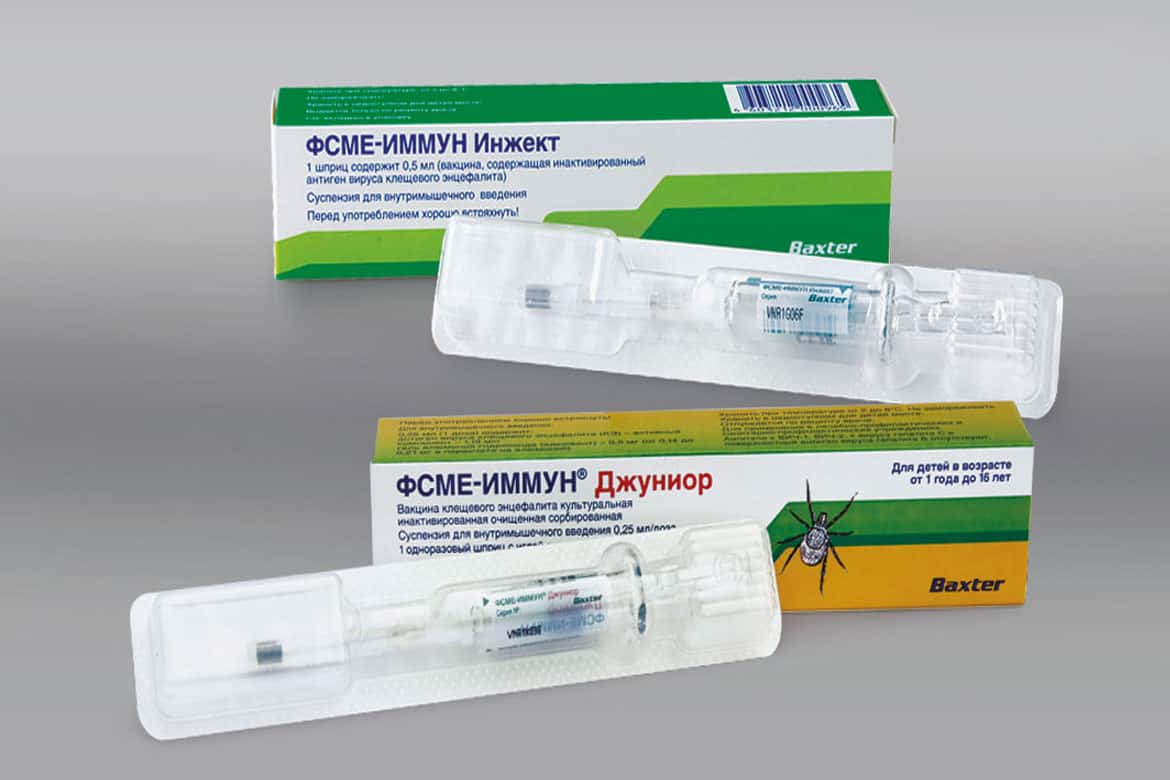
Введение иммуноглобулина необходимо провести как можно раньше, но не позднее 4-го дня (96 часов) после присасывания клеща.
В каких медицинских организациях Москвы проводится экстренная серопрофилактика клещевого энцефалита?
Экстренная серопрофилактика клещевого энцефалита в Москве проводится круглосуточно:
- взрослым — на базе Городского консультативного кабинета по вакцинно-сывороточной профилактике клещевого вирусного энцефалита в ГБУЗ «Инфекционная клиническая больница № 2 ДЗМ» по адресу: г. Москва, 8-я ул. Соколиной горы, д. 15, тел. 8(495)366-84-68, 8(49)365-01-47, 8(495)365-19-28
- детям — на базе ГБУЗ «Детская клиническая больница № 13
им. Н. Ф. Филатова ДЗМ» по адресу: г. Москва, ул. Садовая-Кудринская, д. 15, тел.: 8(499)254-34-30.
Получить дополнительную информацию, а также проконсультироваться по вопросам клещевого вирусного энцефалита и укусам клещей можно в Городском консультативном кабинете по вакцинно-сывороточной профилактике клещевого вирусного энцефалита ГБУЗ «Инфекционная клиническая больница № 2 ДЗМ» по адресу: г. Москва, 8-я ул. Соколиной горы, д. 15, тел.: 8 (495) 366-84-68,
8(495)365-59-47.
Если нет возможности сразу обратиться в травматологический пункт для удаления присосавшегося клеща, и вы самостоятельно смогли его удалить, сохраните его и доставьте в лабораторию для исследования. Это важно сделать, так как при укусе клещом кроме клещевого энцефалита можно заразиться клещевым боррелиозом. Вакцины для профилактики клещевого боррелиоза не существует. Если от присосавшегося клеща выделен возбудитель боррелиоза, то необходимо обратиться к врачу для дальнейшего назначения лечения.
Вакцинация против клещевого энцефалита | Медицинский центр «Сердолик»
Не нужно напоминать, что мы живем в регионе, эндемичном по клещевому энцефалиту. Клещевой энцефалит – природноочаговое вирусное заболевание, которое передается через укус иксодовых клещей, которые распространены в лесных и таежных зонах.
Проявляется клещевой энцефалит в виде поражения центральной нервной системы (энцефалит, менингит, менингоэнцефалит). Летальный исход наступает в 25-30% случаев. У перенесших это заболевание длительно (до 1-2х лет, а иногда и пожизненно) сохраняются выраженные органические изменения центральной нервной системы (судорожные синдромы, атрофии мышц и др.).
Не секрет, что заболеваемость клещевым энцефалитом наносит огромный ущерб здоровью населения и экономике страны. На сегодняшний день наиболее эффективным средством защиты от вируса является сезонная вакцинация. Современные высококачественные вакцины стимулируют выработку антител, что обеспечивает надежную защиту от вируса клещевого энцефалита для лиц, проживающих на эндемичных по клещевому энцефалиту территориях, а также выезжающих на эти территории в весенне-летний период. В настоящее время в России зарегистрировано несколько вакцин от клещевого энцефалита, в т.ч FSME (производство «Бакстер» Австрия), Энцепур (производство «Новартис», Германия), Энцевир (производство Россия).
Вакцины представляют собой высокоочищенные суспензии инактивированного вируса, полученного на клетках куриного эмбриона. Используется у взрослых и детей, начиная с первого года жизни.
Первичный курс вакцинации (для взрослых и детей)
Вакцинация | Схема А | Схема В | |
Первая прививка | 1 доза | 0 день | 0 день |
Вторая прививка | 1 доза | Через 1-3 месяца | Через 14 дней |
Третья прививка | 1 доза | Через 9-12 месяцев после второй прививки | Через 9-12 месяцев |
Обычно вакцинация проводится до начала сезона активности клещей. Первую и вторую прививку предпочтительно проводить в зимние или весенние месяцы (схема А). Допускается проведение вакцинации в летнее время. Если первая вакцинация проводится в летние месяцы, то рекомендуется вторую прививку делать через две недели после первой прививки по схеме быстрой (экстренной) иммунизации (схема В). Третья прививка завершает полный курс вакцинации в соответствии с выбранной схемой. Экстренная схема предназначена для максимально быстрой выработки иммунитета, если сроки стандартной вакцинации были упущены.
Первую и вторую прививку предпочтительно проводить в зимние или весенние месяцы (схема А). Допускается проведение вакцинации в летнее время. Если первая вакцинация проводится в летние месяцы, то рекомендуется вторую прививку делать через две недели после первой прививки по схеме быстрой (экстренной) иммунизации (схема В). Третья прививка завершает полный курс вакцинации в соответствии с выбранной схемой. Экстренная схема предназначена для максимально быстрой выработки иммунитета, если сроки стандартной вакцинации были упущены.
Ревакцинация (для взрослых и детей):
После курса первичной вакцинации, проведенного согласно одной из двух схем, ревакцинация проводится через каждые 3 года в виде одной дозы вакцины
Уровень иммунной защиты превышает 90% после второй прививки и 97% – после третьей. Опыт применения данных вакцин показывает, что защитный эффект, полученный в результате такой иммунизации (3 дозы), сохраняется не менее 3-х лет.
После второй вакцинации (через месяц после постановки) в нашей клинике Вы можете сдать кровь на антитела IgG к клещевому энцефалиту. При титрах 1:200 — 1:400 принято считать, что у пациента создан минимальный защитный уровень специфических антител. При титрах 1:100 или отрицательном результате считается, что иммунитет к клещевому энцефалиту отсутствует.
ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. НЕОБХОДИМО ПРОКОНСУЛЬТИРОВАТЬСЯ СО СПЕЦИАЛИСТОМ!
Следует ли делать детям прививку от болезни Лайма?
18 января 2000 г. (Бостон) — Вакцина, разработанная для защиты людей от клещевой болезни Лайма, может быть столь же эффективной и хорошо переносимой у детей, как и у подростков и взрослых. Но даже если вакцина будет одобрена FDA для детей младше 15 лет, должен ли ее получить каждый ребенок? Скорее всего, нет, говорят ведущие педиатры, опрошенные WebMD.
«Я думаю, что это решать отдельным пациентам и врачам, но это не огромная беда человечества — мы не предотвращаем смертельную болезнь, такую как полиомиелит», — говорит Юджин Д. Шапиро, доктор медицины, профессор педиатрии и эпидемиологии Медицинской школы Йельского университета в Нью-Хейвене, штат Коннектикут, в интервью WebMD.
Шапиро, доктор медицины, профессор педиатрии и эпидемиологии Медицинской школы Йельского университета в Нью-Хейвене, штат Коннектикут, в интервью WebMD.
Старый каштан о том, что унция профилактики стоит фунта лечения, безусловно, относится к болезни Лайма, которая, по данным CDC, составляет более 95% всех болезней, передаваемых насекомыми или животными в США. хотя недавно одобренная вакцина (LYMErix) предлагает достаточно хорошую защиту от заражения организмом, вызывающим болезнь Лайма , , лучшая защита — в первую очередь избегать укусов, говорят члены консультативной группы Американской академии педиатрии (AAP). в январском номере «Педиатрия».
Продолжение
Болезнь Лайма — названная так потому, что некоторые из самых ранних выявленных случаев произошли в районе Старого Лайма, штат Коннектикут, — может возникнуть, когда человека укусил обыкновенный оленьий клещ, зараженный штопором. Формованная бактерия называется Borrelia burgdorferi . Заражение обычно начинается с красной сыпи, которая распространяется вокруг места укуса, как мишень. При раннем обнаружении инфекция легко поддается лечению антибиотиками, но если ее не лечить или неправильно диагностировать, она может вызвать мышечную боль и головные боли, лихорадку, болезненный отек и воспаление крупных суставов (артрит Лайма).В запущенных случаях инфекции могут вызывать симптомы инвалидности в сердце и головном мозге.
Большинство случаев болезни Лайма в США сосредоточено в Новой Англии, штатах средней Атлантики и в верховьях реки Миссисипи. Клещи-олени, как правило, предпочитают лесные районы, высокие травы, болота и пляжи. Но даже в тех регионах, где это заболевание распространено, общий риск заражения после укуса оленьего клеща по-прежнему составляет 1 из 50, по оценкам исследователей.
Продолжение
Группа AAP рекомендует людям принимать разумные меры против инфекции, такие как избегать зараженных клещами участков, использовать защитную одежду (брюки, заправленные в носки, рубашки с длинными рукавами) и использовать репеллент от насекомых, содержащий химический ДЭТА ( n, n-диэтил-м-толуамид) на коже. Другой тип репеллента, предназначенный только для нанесения на одежду и содержащий химический перметрин, также оказался высокоэффективным.
Другой тип репеллента, предназначенный только для нанесения на одежду и содержащий химический перметрин, также оказался высокоэффективным.
Группа выступает против рутинного использования антибиотиков у людей, укушенных клещом, но не имевших положительного диагноза болезни Лайма, заявляя, что такая практика «имеет непроверенную ценность и связана с потенциальными рисками и затратами».
В рекомендациях AAP также говорится, что вакцинация против болезни Лайма может быть рассмотрена для подростков в возрасте 15 лет и старше, которые живут, работают или играют в районах с высоким или умеренным риском, или тех, кто остается в таких местах во время весеннего пикового сезона передачи инфекции. и чья деятельность приводит к частому или продолжительному воздействию (т.е. садовые и газонные работы, расчесывание пляжей, катание на лодках и т.д.).
Продолжение
А как насчет детей от 5 до 15 лет? В исследовании 250 детей, о которых сообщалось в Pediatrics в ноябре 1999 года, Генри М. Федер, доктор медицинских наук, и другие обнаружили, что вакцина , по-видимому, хорошо переносится и вырабатывает высокий уровень антител к бактериям у 99% детей. кто получил вакцину. Наличие антител предполагает, что иммунная система детей была настроена на борьбу с болезнью Лайма.
«Предварительное впечатление от вакцины таково, что побочные эффекты у детей, во всяком случае, не больше, чем у взрослых, и, вероятно, меньше, а иммунный ответ по крайней мере такой же, но, вероятно, лучше», — говорит Федер, профессор педиатрия в Детском медицинском центре Коннектикута и профессор семейной медицины в Центре здоровья Университета Коннектикута в Фармингтоне в интервью WebMD.
Федер говорит, что, поскольку вакцина «не идеальна» для защиты пациентов от инфекции, «очень важно, чтобы все, что люди пытаются сделать, чтобы избежать болезни Лайма, они продолжали делать.Я думаю, что это одна из вещей, которая беспокоит некоторых врачей по поводу вакцины Лайма — идея о том, что «О, теперь, когда у меня была вакцина, мне не нужно быть осторожным [в отношении воздействия клещей]» ».
Продолжение
Шапиро сообщает WebMD, что он согласен с рекомендациями комиссии по дальнейшему изучению рисков и преимуществ вакцины у детей. необходимость вакцинации в качестве рутинной процедуры », — говорит он.«Группа экспертов рекомендует использовать его для людей с высоким риском, но большинство детей не подвержены высокому риску, и в целом это легко поддающееся лечению заболевание, поэтому нет реальной необходимости в иммунизации».
Среди проблем, вызывающих озабоченность по поводу вакцины, отмечает Шапиро, требуются многократные дозы (три инъекции за столько же месяцев), частые сообщения о боли и отеках в месте инъекции, а также большое количество ложноположительных тестов на антитела у пациентов, которые получили вакцину.Ложноположительные результаты исследования антител могут заставить врачей ошибочно полагать, что у пациента болезнь Лайма, и упускать из виду другие возможные причины симптомов пациента.
Продолжение
«Обычно я никому не рекомендую [вакцину], — говорит Шапиро.
КЭ, или «клещевая вакцина» — Инфекционные болезни и вакцинация
Вакцина обеспечивает защиту от клещевого энцефалита (КЭ).
Болезни, предупреждаемые с помощью вакцин
На этой странице
Кому вводится вакцина против клещевого энцефалита?
Национальная программа вакцинации предлагает бесплатную вакцинацию лицам в возрасте от 3 лет и старше, проживающим в муниципалитете Финляндии и имеющим постоянный дом или дом для отдыха в
- южных районах Кеми
- Simo
- Архипелаг Котка
- Район Саммонлахти в Лаппеенранте
- Остров Прейскари недалеко от Раахе
- Парайнен
- Район архипелага Лохьяньярви
- Кустави
- Район Луома в Киркконумми
- В некоторых частях архипелага Сипоо
природа в течение как минимум 4 недель летом нуждается в вакцине.
Лица, постоянно проживающие на Аландских островах, также имеют право на бесплатную вакцинацию.
Карта, показывающая заболеваемость клещевым энцефалитом и рекомендации по вакцинации по местности
Человек, который ранее не был вакцинирован, имеет право на получение трех бесплатных доз.
Человек, чья серия первичной вакцинации не была завершена, также получает бесплатные ревакцинации в рамках национальной программы.
Вакцину можно вводить как постоянным жителям, так и другим лицам, имеющим право на бесплатную вакцинацию, на Аландских островах, в Парайнене, Симо, Кеми, Котке, Лаппеенранте, Раахи, Лохья или Кустави.
Бустеры для тех, кто получил серию из трех доз, в настоящее время не включены в национальную программу вакцинации.
Вакцина против клещей не защитит вас от клещей
Вакцина против клещевого энцефалита часто называется вакцинацией против клещей. Следует помнить, что вакцина не защитит вас от клещей и не остановит их прикрепление к вашей коже.
Наиболее частым заболеванием, передаваемым клещами, является боррелиоз, против которого нет вакцины.
Вот почему вам следует защищаться от укусов клещей, даже если вы прошли вакцинацию.Инструкция по защите от клещей.
Какая вакцина используется и что в ней содержится?
- Вакцины TicoVac или Encepur для взрослых и TicoVac Junior или Encepur Children для детей используются в национальной программе вакцинации.
- Хотя состав вакцин для взрослых и детей схож, объем вакцины для детей составляет лишь половину дозы для взрослых.
- Вакцины не содержат живых патогенов и поэтому не могут вызывать клещевой энцефалит.
- Действующее вещество содержит целые инактивированные вирусы клещевого энцефалита, культивируемые в примордиальных зародышевых клетках курицы.
- Адъювант представляет собой соединение алюминия.
- Вакцины не содержат консервантов.
- Не содержат значительных объемов яичного белка (овальбумина).
Дозировка и график
Тиковак и Тиковак Юниор
- Вакцина Тиковак Юниор применяется для детей в возрасте от 1 до 15 лет.
 Разовая доза составляет 0,25 мл.
Разовая доза составляет 0,25 мл. - Ticovac используется для лиц в возрасте 16 лет и старше. Разовая доза составляет 0,5 мл.
- Серия первичной вакцинации состоит из трех доз. Вторая доза вводится через 1-3 месяца после первой. Третья доза вводится через 5-12 месяцев после второй.
- Если защита необходима срочно, вторую дозу можно вводить уже через две недели после первой. В этом случае также вводят третью дозу через 5-12 месяцев после второй дозы.
- После начала вакцинация при необходимости может быть продолжена другой вакциной против клещевого энцефалита.
Encepur и Encepur Children
- Вакцина Encepur Children применяется для детей в возрасте от 1 до 11 лет. Разовая доза составляет 0,25 мл.
- Энцепур используется для лиц в возрасте от 12 лет и старше. Разовая доза составляет 0,5 мл.
- Серия первичной вакцинации состоит из трех доз. Вторая доза вводится через 1-3 месяца после первой.Третья доза вводится через 9-12 месяцев после второй дозы.
- Если защита необходима более срочно, вторую дозу можно вводить уже через две недели после первой. В этом случае также вводят третью дозу через 9–12 месяцев после второй дозы.
- Если необходима немедленная защита, можно использовать ускоренный график вакцинации Encepur. В этом случае первые три дозы вводятся на 0, 7 и 21 дни, а первая ревакцинация — уже через 12-18 месяцев после третьей дозы.
- После начала вакцинация при необходимости может быть продолжена другой вакциной против клещевого энцефалита.
Бустерные дозы
Рекомендуется введение первой бустерной дозы через три года. Впоследствии бустеры вводятся следующим образом, если воздействие вируса клещевого энцефалита продолжается:
- тем, кто получил ревакцинацию в возрасте до 50 лет, следующая бустерная доза вводится через 10 лет
- тем, кто получил ревакцинацию в возрасте от 50 до 60, ревакцинации назначаются каждые 5 лет
- тем, кто получил ревакцинацию в возрасте старше 60 лет, следующие бустерные дозы вводятся каждые 3 года
- людям с ослабленной иммунной системой в результате лечения или болезни, ревакцинальная доза должна быть вводится каждые 3 года.

Например: 53-летний мужчина, получивший последнюю бустерную дозу в возрасте 48 лет, получает следующую бустерную дозу в возрасте 58 лет. к обоим продуктам, Ticovac и Encepur, и отличаются от инструкций, приведенных в сводке характеристик продукта.
Какие противопоказания и меры предосторожности связаны с вакциной?
Вакцину нельзя вводить детям в возрасте до 1 года.
Вакцину нельзя вводить человеку, у которого была подтвержденная анафилактическая реакция после предыдущей дозы вакцины против клещевого энцефалита или вакцины, содержащей аналогичные компоненты.
Аллергия на яйца не является противопоказанием для вакцинации . Если вакцинация считается необходимой, вы также можете сделать ее человеку, у которого яйца или продукты, содержащие яйца, вызвали анафилактическую реакцию. Противопоказания и меры предосторожности THL и производителя при назначении людям с аллергией на яйца в этом отношении различаются.
Отложите вакцинацию, если у человека поднялась температура.
Каковы преимущества вакцины против клещевого энцефалита?
Вакцина предотвращает около девяти из десяти случаев КЭ.
Помимо острого заболевания, вакцина может также предотвратить долгосрочные неврологические проблемы, включая нарушения памяти и концентрации внимания, которые затрагивают прибл. каждый третий пациент, у которого развивается заболевание с симптомами нервной системы.
Каковы возможные побочные эффекты вакцины против клещевого энцефалита?
Обычные побочные эффекты включают местные симптомы в месте инъекции, включая покраснение, жар, боль и отек.
У реципиента вакцины могут быть преходящие генерализованные симптомы, включая головные боли, тошноту и усталость. Некоторые испытывают ломоту в конечностях и увеличение лимфатических узлов.
Лихорадка — частый симптом, особенно у маленьких детей, который в основном возникает после первой дозы.
Кожные симптомы или реакции гиперчувствительности возникают редко.
Вакцина применяется уже давно, и за это время были введены десятки миллионов доз.
Неврологические симптомы, возникающие в период после вакцинации, крайне редки: они затронули ок. один на миллион получателей.
Связь между вакциной и изолированными инфекциями центральной или периферической нервной системы, о которых сообщалось после вакцинации, нельзя полностью исключить.
Местные и генерализованные симптомы обычно начинаются в течение нескольких дней после введения и продолжаются в течение нескольких дней. Их можно лечить с помощью жаропонижающих и обезболивающих.
Местные и генерализованные симптомы не являются противопоказанием для дальнейших вакцинаций.
История вакцины против клещевого энцефалита в национальной программе вакцинации
вакцины против клещевого энцефалита были начаты как часть национальной программы вакцинации на Аландских островах в 2006 году.
Парайнен и Симо были добавлены в программу в 2017 году и были частью Кеми и Лаппеенранта, а также архипелаг Котка и остров Прейскари в 2018 году. Программа вакцинации была начата в ограниченном районе Лохья в 2019 году, а в 2020 году этот район был расширен.Весной 2021 года вакцинация стала доступна в некоторых частях Киркконумми и в некоторых частях архипелага Сипоо.
Рекомендации и отчеты
Следует ли расширить программу иммунизации против клещевого энцефалита?
Отчет рабочей группы по иммунизации против клещевого энцефалита
Вакцина против клещевого энцефалита | Mehiläinen
Вы можете записаться на прием для вакцинации против клещевого энцефалита через Интернет или позвонив в нашу службу поддержки клиентов. В большинстве мест вакцинация также проводится без предварительной записи.Пожалуйста, уточните, предоставляет ли в вашем предпочтительном месте услуги вакцинации, позвонив в нашу службу поддержки клиентов.
Запишитесь на прививку от клещевого энцефалита!
Посмотреть стоимость вакцинации
Вакцинация защищает от клещевого энцефалита, но не от болезни Лайма
Вакцинация против клещевого энцефалита (КЭ) может предотвратить заражение вирусным энцефалитом, переносимым клещами. Вакцина предотвращает примерно девять из десяти случаев инфицирования клещевым энцефалитом.Вакцина необходима, в частности, тем, кто проводит недели или месяцы в местах распространения болезни и проводит много времени на открытом воздухе. Вакцину можно вводить младенцам старше 12 месяцев, хотя дети младше 7 лет редко заболевают этой болезнью, а если и заболевают, то симптомы обычно слабо выражены. Однако этот вопрос малоизвестен, и даже у маленьких детей диагностировали тяжелые случаи лихорадки мозга, вызванной вирусом клещевого энцефалита.
Вакцина предотвращает примерно девять из десяти случаев инфицирования клещевым энцефалитом.Вакцина необходима, в частности, тем, кто проводит недели или месяцы в местах распространения болезни и проводит много времени на открытом воздухе. Вакцину можно вводить младенцам старше 12 месяцев, хотя дети младше 7 лет редко заболевают этой болезнью, а если и заболевают, то симптомы обычно слабо выражены. Однако этот вопрос малоизвестен, и даже у маленьких детей диагностировали тяжелые случаи лихорадки мозга, вызванной вирусом клещевого энцефалита.
Вакцина не защищает от других клещевых заболеваний или самих клещей и не препятствует их прикреплению к коже.Прикрепление клещей можно предотвратить с помощью защитной одежды и средства от насекомых, которое действует на клещей. Если, несмотря на вакцинацию, у вас укус клеща и на пораженном участке появляется увеличивающееся покраснение, возможно, вы заразились болезнью Лайма. Вам следует немедленно обратиться за медицинской помощью.
Проведение вакцинации против клещевого энцефалита
Базовая иммунизация взрослых и детей включает три внутримышечные инъекции. Первые две инъекции следует делать в зимние месяцы до начала сезона клещей с интервалами от 1 до 3 месяцев, а третью инъекцию следует делать в течение следующего зимнего сезона.Полный иммунитет достигается через две недели после приема второй дозы.
Программы ускоренной вакцинации также могут применяться для обеспечения иммунитета, если вакцинация начинается позже, чем заражение.
После основного иммунитета, обеспечиваемого тремя дозами, первая бустерная доза обычно вводится через три года, а следующие дозы — каждые десять лет людям в возрасте до 50 лет. Бустерная доза вводится 50–60-летним каждые пять лет и 60-летним каждые три года.
Для получения дополнительной информации, пожалуйста, свяжитесь с нашей службой поддержки клиентов по телефону +358 (0) 10 414 00 (0,084 € / мин). Служба поддержки клиентов Mehiläinen открыта для частных клиентов каждый день с 6:00 до 22:00.
Кому нельзя делать прививку от клещевого энцефалита?
Серьезная аллергия на яйца или тяжелая аллергическая реакция на предыдущую вакцинацию против клещевого энцефалита могут быть противопоказаниями к вакцинации, если реакция имеет анафилактический характер. Как правило, вакцинировать можно тем, у кого аллергия на яйца.
Варианты вакцинации против клещевого энцефалита
Доступны два вакцинных продукта с вариантами вакцины, которые также подходят для детей.
Побочные эффекты вакцинации против клещевого энцефалита
Объем побочного действия соответствует таковому у других вакцин. Побочные эффекты могут включать тошноту, головную боль, усталость, временные местные симптомы, иногда боль в конечностях и отек лимфатических узлов. Лихорадка является частым симптомом, особенно у маленьких детей, и в основном возникает после первой инъекции вакцины.
Подробнее (на финском):
• 7 фактов об укусах клещей
• Укусы клещей
• Боррелиоз (болезнь Лайма)
• Укусы и укусы насекомых — что делать при зуде?
Специалисты
См. Всех других специалистов
Рекомендации ACIP по противопоказаниям для иммунизации
Общие рекомендации по передовой практике иммунизации: Рекомендации Консультативного комитета по практике иммунизации (ACIP)
Версия для печати pdf icon [18 страниц]
Обновления
Основные изменения в руководстве по передовой практике в этом разделе включают: 1) усиление определения «меры предосторожности» с целью включения любого состояния, которое может сбивать с толку диагностическую точность, и 2) рекомендацию вакцинации во время госпитализации, если у пациента нет острого состояния средней или тяжелой степени. больной.
Общие принципы
Установлены национальные стандарты для практики вакцинации детей, которые включают описание действующих противопоказаний и мер предосторожности к вакцинации ( 2 ). Лица, которые вводят вакцины, должны проверять пациентов на противопоказания и меры предосторожности для вакцинации перед введением каждой дозы вакцины (Таблица 4-1). Скринингу способствует постоянное использование скрининговых анкет, которые можно получить в некоторых государственных программах вакцинации и из других источников (например, из других источников).g., внешний значок Коалиции действий по иммунизации).
Скринингу способствует постоянное использование скрининговых анкет, которые можно получить в некоторых государственных программах вакцинации и из других источников (например, из других источников).g., внешний значок Коалиции действий по иммунизации).
Противопоказания
Противопоказания (состояния реципиента, повышающие риск серьезных побочных реакций) к вакцинации — это условия, при которых вакцины не следует вводить. Поскольку большинство противопоказаний являются временными, вакцинацию часто можно проводить позже, когда состояние, приводящее к противопоказанию, больше не существует. Вакцину нельзя вводить при наличии противопоказаний; например, вакцину MMR не следует вводить лицам с тяжелым иммунодефицитом ( 1 ).Однако некоторые состояния обычно ошибочно воспринимаются как противопоказания (т. Е. Не являются вескими причинами для отсрочки вакцинации).
Лица с тяжелым иммунодефицитом, как правило, не должны получать живые вакцины ( 3 ). Из-за теоретического риска для плода беременные женщины, как правило, не должны получать живые ослабленные вирусные вакцины ( 4 ). Лица, у которых возникла энцефалопатия в течение 7 дней после введения предыдущей дозы вакцины, содержащей коклюш, не связанной с другой идентифицируемой причиной, не должны получать дополнительные дозы вакцины, содержащей коклюш ( 4, 5 ).Заболевание тяжелого комбинированного иммунодефицита (ТКИД) и инвагинация в анамнезе являются противопоказаниями к получению ротавирусных вакцин ( 6 ).
Меры предосторожности
Мера предосторожности — это состояние реципиента, которое может повысить риск серьезной побочной реакции, вызвать диагностическую путаницу или поставить под угрозу способность вакцины вырабатывать иммунитет (например, введение противокоревой вакцины человеку с пассивным иммунитетом к кори. от переливания крови, проведенного до 7 месяцев назад) ( 7 ).Человек может испытать более тяжелую реакцию на вакцину, чем можно было бы ожидать в противном случае; однако риск этого меньше, чем риск, ожидаемый при наличии противопоказаний. Как правило, вакцинацию следует отложить, если соблюдаются меры предосторожности. Однако вакцинация может быть показана при наличии меры предосторожности, если польза от защиты от вакцины превышает риск побочной реакции.
Как правило, вакцинацию следует отложить, если соблюдаются меры предосторожности. Однако вакцинация может быть показана при наличии меры предосторожности, если польза от защиты от вакцины превышает риск побочной реакции.
Наличие умеренного или тяжелого острого заболевания с лихорадкой или без нее является мерой предосторожности при введении всех вакцин (Таблица 4-1).Решение о проведении вакцинации или отсрочке вакцинации из-за текущего или недавнего острого заболевания зависит от тяжести симптомов и этиологии состояния. Безопасность и эффективность вакцинации лиц с легкими заболеваниями подтверждены документально ( 8-11 ). Людям с умеренным или тяжелым острым заболеванием следует отложить вакцинацию. Эта мера предосторожности позволяет избежать диагностической путаницы между проявлениями основного заболевания и возможными побочными эффектами вакцинации или наложения побочных эффектов вакцины на основное заболевание.После проверки на противопоказания лицам с умеренным или тяжелым острым заболеванием следует вакцинировать, как только состояние острого заболевания улучшится. Исследования показывают, что отказ от вакцинации детей с легкими заболеваниями может затруднить вакцинацию ( 12–14 ). Среди лиц, соблюдение которых не может быть обеспечено, использование каждой возможности для введения соответствующих вакцин имеет решающее значение.
Госпитализацию следует использовать как возможность для проведения рекомендованной вакцинации.В медицинских учреждениях соблюдаются стандарты предложения вакцины против гриппа госпитализированным пациентам, поэтому провайдеры заинтересованы в вакцинации этих пациентов в какой-то момент во время госпитализации ( 15 ). Точно так же пациенты, поступающие на плановые процедуры, не будут серьезно болеть в течение всего периода их госпитализации. Большинство исследований, изучающих влияние хирургического вмешательства или анестезии на иммунную систему, были наблюдательными, включали только младенцев и детей, были небольшими и непрямыми, поскольку в них не рассматривалось конкретно иммунное влияние на реакцию на вакцинацию ( 16- 35 ). Они не предоставляют убедительных доказательств того, что недавняя анестезия или операция значительно влияют на реакцию на вакцины. Текущая, недавняя или предстоящая анестезия / операция / госпитализация не является противопоказанием к вакцинации, но определенные факторы могут побудить поставщика принять во внимание текущую, недавнюю или предстоящую анестезию / операцию / госпитализацию в качестве меры предосторожности ( 16-35 ). Следует приложить усилия, чтобы обеспечить введение вакцины во время госпитализации или при выписке. Пациентам, которые на протяжении всего периода госпитализации считаются больными средней или тяжелой формой заболевания, вакцинация должна проводиться при первой возможности (т.е. во время немедленного последующего наблюдения после госпитализации, включая посещения на дому или в офисе), когда клинические симптомы пациента улучшились.
Они не предоставляют убедительных доказательств того, что недавняя анестезия или операция значительно влияют на реакцию на вакцины. Текущая, недавняя или предстоящая анестезия / операция / госпитализация не является противопоказанием к вакцинации, но определенные факторы могут побудить поставщика принять во внимание текущую, недавнюю или предстоящую анестезию / операцию / госпитализацию в качестве меры предосторожности ( 16-35 ). Следует приложить усилия, чтобы обеспечить введение вакцины во время госпитализации или при выписке. Пациентам, которые на протяжении всего периода госпитализации считаются больными средней или тяжелой формой заболевания, вакцинация должна проводиться при первой возможности (т.е. во время немедленного последующего наблюдения после госпитализации, включая посещения на дому или в офисе), когда клинические симптомы пациента улучшились.
Личная или семейная история судорог является мерой предосторожности при вакцинации MMRV; это связано с тем, что недавнее исследование выявило повышенный риск фебрильных судорог у детей в возрасте 12–23 месяцев, получающих MMRV, по сравнению с вакциной MMR и вакциной против ветряной оспы ( 36 ).
Ни противопоказаний, ни мер предосторожности
Клиницисты или другие медицинские работники могут ошибочно воспринимать определенные условия или обстоятельства как действительные противопоказания или меры предосторожности к вакцинации, если они фактически не препятствуют вакцинации ( 2 ) (Таблица 4-2).Эти неправильные представления приводят к упущенным возможностям введения рекомендованных вакцин ( 37 ).
Регулярные медицинские осмотры и процедуры (например, измерение температуры) не являются предварительным условием для вакцинации людей, которые выглядят здоровыми. Поставщик должен спросить родителя или опекуна, если ребенок болен. Если у ребенка заболевание средней или тяжелой степени тяжести, вакцинацию следует отложить.
ТАБЛИЦА 4-1. Противопоказания и меры предосторожности
(a) к широко используемым вакцинам
| Вакцина | Цитата | Противопоказания | Меры предосторожности |
|---|---|---|---|
| DT, Td | ( 4 ) | Тяжелая аллергическая реакция (e. g., анафилаксия) после предыдущей дозы или компонента вакцины g., анафилаксия) после предыдущей дозы или компонента вакцины | GBS <6 недель после предыдущей дозы вакцины, содержащей столбнячный анатоксин История реакций гиперчувствительности типа Артюс после предыдущей дозы вакцины, содержащей дифтерийный анатоксин или столбнячный анатоксин; отложить вакцинацию до истечения 10 лет с момента последней вакцины, содержащей столбнячный анатоксин Умеренное или тяжелое острое заболевание с лихорадкой или без нее |
| DTaP | ( 38 ) | Тяжелая аллергическая реакция (e.g., анафилаксия) после предыдущей дозы или компонента вакцины Энцефалопатия (например, кома, снижение уровня сознания, продолжительные припадки), не связанная с другой идентифицируемой причиной, в течение 7 дней после введения предыдущей дозы АКДС или АКДС | Прогрессирующее неврологическое расстройство, включая детские спазмы, неконтролируемую эпилепсию, прогрессирующую энцефалопатию; отложить АКДС до выяснения и стабилизации неврологического статуса GBS <6 недель после предыдущей дозы вакцины, содержащей столбнячный анатоксин История реакций гиперчувствительности типа Артюс после предыдущей дозы вакцины, содержащей дифтерийный анатоксин или столбнячный анатоксин; отложить вакцинацию до истечения как минимум 10 лет с момента последней вакцины, содержащей столбнячный анатоксин Умеренное или тяжелое острое заболевание с лихорадкой или без нее |
| Гепатит А | ( 39 ) | Тяжелая аллергическая реакция (e.g., анафилаксия) после предыдущей дозы или компонента вакцины | Умеренное или тяжелое острое заболевание с лихорадкой или без нее |
| Гепатит B | ( 40 ) | Тяжелая аллергическая реакция (например, анафилаксия) после предыдущей дозы или компонента вакцины Повышенная чувствительность к дрожжам | Умеренное или тяжелое острое заболевание с лихорадкой или без нее |
| Hib | ( 41 ) | Тяжелая аллергическая реакция (e. g., анафилаксия) после предыдущей дозы или компонента вакцины g., анафилаксия) после предыдущей дозы или компонента вакциныВозраст <6 недель | Умеренное или тяжелое острое заболевание с лихорадкой или без нее |
| ВПЧ (б) | ( 42 ) | Тяжелая аллергическая реакция (например, анафилаксия) после предыдущей дозы или на компонент вакцины, включая дрожжи | Умеренное или тяжелое острое заболевание с лихорадкой или без нее |
| IIV | ( 43 ) | Тяжелая аллергическая реакция (e.g., анафилаксия) после предыдущей дозы вакцины против гриппа или компонента вакцины. | GBS <6 недель после предыдущей дозы вакцины против гриппа Умеренное или тяжелое острое заболевание с лихорадкой или без нее Аллергия на яйца, кроме крапивницы, например ангионевротический отек, респираторный дистресс, головокружение, рецидивирующая рвота; или необходим адреналин или другое неотложное медицинское вмешательство (IIV можно вводить в стационарных или амбулаторных условиях и под наблюдением врача, который может распознать и справиться с тяжелыми аллергическими состояниями). |
| ИПВ | ( 44 ) | Тяжелая аллергическая реакция (например, анафилаксия) после предыдущей дозы или компонента вакцины | Беременность Умеренное или тяжелое острое заболевание с лихорадкой или без нее |
| LAIV (c) | ( 43 ) | Тяжелая аллергическая реакция (например, анафилаксия) после предыдущей дозы или компонента вакцины Одновременное применение аспирина или аспиринсодержащих препаратов у детей и подростков LAIV4 не следует назначать лицам, которые принимали осельтамивир или занамивир в течение предыдущих 48 часов, перамивир в течение предыдущих 5 дней или балоксавир в течение предыдущих 17 дней. (д) Беременность Дети в возрасте от 2 до 4 лет, которым был поставлен диагноз астмы или чьи родители или опекуны сообщают, что поставщик медицинских услуг сообщил им в течение предшествующих 12 месяцев, что у их ребенка было свистящее дыхание или астма или чья медицинская карта указывает на эпизод свистящего дыхания в течение предшествующих 12 месяцев. Лица с активными цереброспинальными жидкостями / ротоглоточными связями / утечками. Тесные контакты и лица, обеспечивающие уход за людьми с тяжелой иммуносупрессией, которым требуется защищенная среда. Лица с кохлеарными имплантатами (из-за возможности утечки спинномозговой жидкости, которая может существовать в течение некоторого периода времени после имплантации. Провайдеры могут рассмотреть возможность консультации со специалистом относительно риска стойкой утечки спинномозговой жидкости, если нельзя использовать соответствующую возрасту инактивированную или рекомбинантную вакцину. ). Измененная иммунная компетентность Анатомическая или функциональная аспления (например, серповидно-клеточная анемия) | GBS <6 недель после предыдущей дозы вакцины против гриппа Астма у лиц в возрасте 5 лет и старше Заболевания, которые могут предрасполагать к более высокому риску осложнений, связанных с гриппом (d) Умеренное или тяжелое острое заболевание с лихорадкой или без нее |
| MenACWY | ( 45 ) | Тяжелая аллергическая реакция (e.g., анафилаксия) после предыдущей дозы или компонента вакцины, включая дрожжи | Умеренное или тяжелое острое заболевание с лихорадкой или без нее Преждевременные роды (MenACWY-CRM) (ж) |
| MenB | ( 46, 47 ) | Тяжелая аллергическая реакция (например, анафилаксия) после предыдущей дозы или компонента вакцины | Умеренное или тяжелое острое заболевание с лихорадкой или без нее Беременность Чувствительность к латексу (MenB-4c) |
| MMR (г), (в) | ( 1 ) | Тяжелая аллергическая реакция (e.g., анафилаксия) после предыдущей дозы или компонента вакцины Беременность Известный тяжелый иммунодефицит (например, из-за гематологических и солидных опухолей, получение химиотерапии, врожденный иммунодефицит, длительная иммуносупрессивная терапия (i) или пациенты с ВИЧ-инфекцией с тяжелым иммунодефицитом) Семейный анамнез измененной иммунокомпетентности (i) | Недавнее (≤11 месяцев) получение продукта крови, содержащего антитела (конкретный интервал зависит от продукта) История тромбоцитопении или тромбоцитопенической пурпуры Требуется туберкулиновая кожная проба или исследование высвобождения гамма-интерферона (IGRA) (k) Умеренное или тяжелое острое заболевание с лихорадкой или без нее |
| MPSV4 | ( 48 ) | Тяжелая аллергическая реакция (e.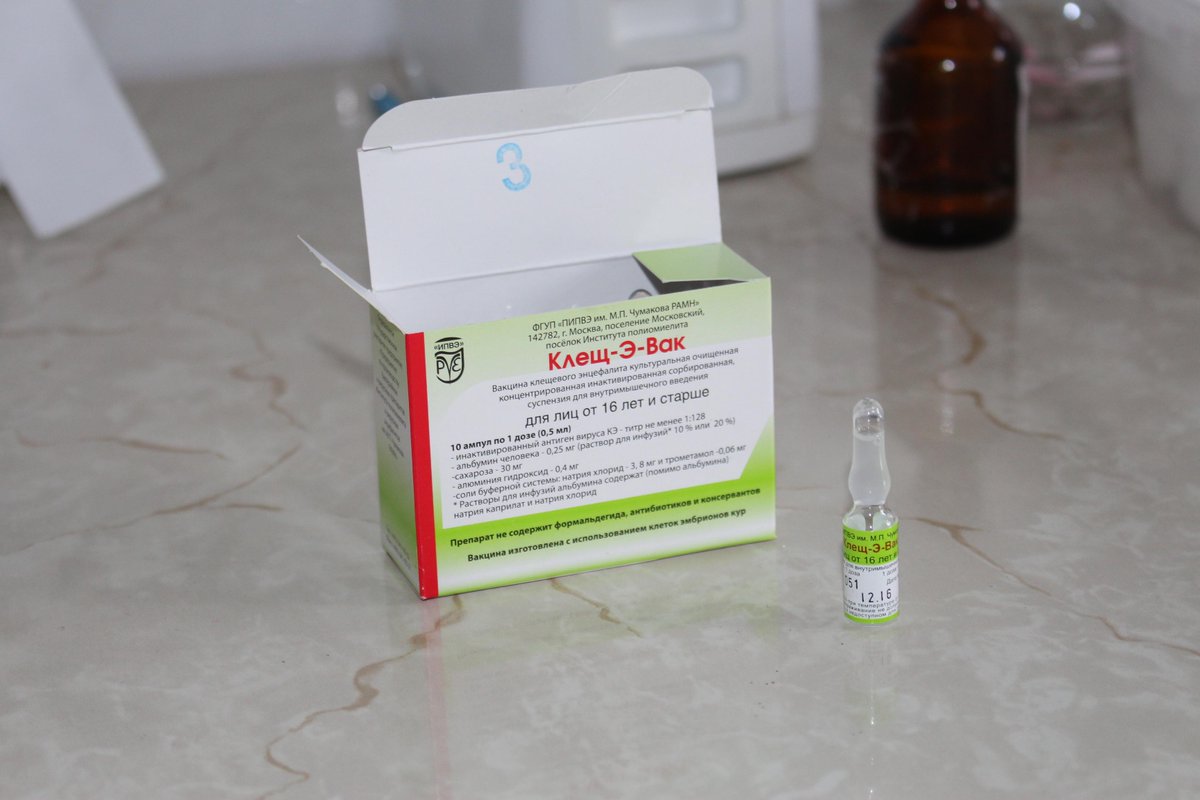 g., анафилаксия) после предыдущей дозы или компонента вакцины g., анафилаксия) после предыдущей дозы или компонента вакцины | Умеренное или тяжелое острое заболевание с лихорадкой или без нее |
| PCV13 | ( 49 ) | Тяжелая аллергическая реакция (например, анафилаксия) после предыдущей дозы PCV13 или любой вакцины, содержащей дифтерийный анатоксин, или компонента вакцины (PCV13 или любой вакцины, содержащей дифтерийный анатоксин), включая дрожжи | Умеренное или тяжелое острое заболевание с лихорадкой или без нее |
| PPSV23 | ( 50 ) | Тяжелая аллергическая реакция (e.g., анафилаксия) после предыдущей дозы или компонента вакцины | Умеренное или тяжелое острое заболевание с лихорадкой или без нее |
| RIV | ( 43 ) | Тяжелая аллергическая реакция (например, анафилаксия) на любой компонент вакцины | GBS <6 недель после предыдущей дозы вакцины против гриппа Умеренное или тяжелое острое заболевание с лихорадкой или без нее |
| Ротавирус | ( 6 ) | Тяжелая аллергическая реакция (e.g., анафилаксия) после предыдущей дозы или компонента вакцины SCID История инвагинации | Измененная иммунная компетентность, кроме ТКИД Хронические желудочно-кишечные заболевания (л) Расщелина позвоночника или экстрофия мочевого пузыря (l) Умеренное или тяжелое острое заболевание с лихорадкой или без нее |
| Tdap | ( 51 ) | Тяжелая аллергическая реакция (например, анафилаксия) после предыдущей дозы или компонента вакцины Энцефалопатия (e.g., кома, снижение уровня сознания, длительные судороги), не относящиеся к другой идентифицируемой причине, в течение 7 дней после введения предыдущей дозы АКДС, АКДС или Tdap | GBS <6 недель после введения предыдущей дозы вакцины, содержащей столбнячный анатоксин Прогрессирующее или нестабильное неврологическое расстройство, неконтролируемые судороги или прогрессирующая энцефалопатия до тех пор, пока не будет установлен режим лечения и состояние не стабилизируется История реакций гиперчувствительности типа Артюс после предыдущей дозы вакцины, содержащей дифтерийный анатоксин или столбнячный анатоксин; отложить вакцинацию до истечения как минимум 10 лет с момента последней вакцины, содержащей столбнячный анатоксин Умеренное или тяжелое острое заболевание с лихорадкой или без нее |
| Ветряная оспа (г), (в) | ( 52 ) | Тяжелая аллергическая реакция (e. g., анафилаксия) после предыдущей дозы или компонента вакцины g., анафилаксия) после предыдущей дозы или компонента вакциныИзвестный тяжелый иммунодефицит (например, из-за гематологических и солидных опухолей, получение химиотерапии, врожденный иммунодефицит, длительная иммуносупрессивная терапия (i) или пациенты с ВИЧ-инфекцией с тяжелым иммунодефицитом) (g) Беременность Семейный анамнез измененной иммунокомпетентности (j) | Недавнее (≤11 месяцев) получение продукта крови, содержащего антитела (конкретный интервал зависит от продукта) Умеренное или тяжелое острое заболевание с лихорадкой или без нее Получение определенных противовирусных препаратов (ацикловир, фамцикловир или валацикловир) за 24 часа до вакцинации (избегайте использования этих противовирусных препаратов в течение 14 дней после вакцинации) Использование аспирина или аспиринсодержащих продуктов (m) |
| Опоясывающий лишай | ( 53 ) | Тяжелая аллергическая реакция (e.g., анафилаксия) после предыдущей дозы или компонента вакцины | Умеренное или тяжелое острое заболевание с лихорадкой или без нее |
Сокращения: DT = дифтерийный и столбнячный анатоксины; DTaP = дифтерийный и столбнячный анатоксины и бесклеточный коклюш; АКДС = дифтерийный анатоксин, столбнячный анатоксин и коклюш; GBS = синдром Гийена-Барре; Hib = Haemophilus influenzae тип b; ВИЧ = вирус иммунодефицита человека; ВПЧ = вирус папилломы человека; IIV = инактивированная вакцина против гриппа; ИПВ = инактивированный полиовирус; LAIV = живая аттенуированная вакцина против гриппа; MenACWY = четырехвалентная менингококковая конъюгированная вакцина; MMR = корь, эпидемический паротит и краснуха; MPSV4 = четырехвалентная менингококковая полисахаридная вакцина; PCV13 = пневмококковая конъюгированная вакцина; PPSV23 = пневмококковая полисахаридная вакцина; ТКИД = тяжелый комбинированный иммунодефицит; RIV = рекомбинантная вакцина против гриппа; Td = столбнячный и дифтерийный анатоксины; Tdap = столбнячный анатоксин, редуцированный дифтерийный анатоксин и бесклеточный коклюш.
(a) События или условия, указанные в качестве мер предосторожности, должны быть тщательно проанализированы. Следует учитывать преимущества и риски введения конкретной вакцины человеку в этих обстоятельствах. Если считается, что риск от вакцины перевешивает пользу, вакцину не следует вводить. Если считается, что польза от вакцинации превышает риск, вакцину следует ввести. Следует ли и когда назначать DTaP детям с доказанными или предполагаемыми основными неврологическими расстройствами, следует решать в каждом конкретном случае.
(b) Вакцина против ВПЧ не рекомендуется во время беременности
(c) Кроме того, ACIP рекомендует не использовать LAIV для беременных женщин, лиц с ослабленным иммунитетом и детей в возрасте 2-4 лет, страдающих астмой или у которых был эпизод свистящего дыхания, отмеченный в медицинской карте в течение последних 12 месяцев. или родители сообщают, что поставщик медицинских услуг заявил, что у них было свистящее дыхание или астма в течение последних 12 месяцев. LAIV не следует назначать лицам, которые принимали противовирусные препараты от гриппа в течение предыдущих 48 часов.Лица, которые заботятся о лицах с тяжелым иммунодефицитом, которым требуется защитная среда, не должны получать LAIV или должны избегать контактов с такими людьми в течение 7 дней после получения.
(d) См. Ссылку: Grohskopf L, Alyanak E, Broder DR, Walter EB, Fry AM, Jernigan DB. Профилактика сезонного гриппа и борьба с ним с помощью вакцин: рекомендации Консультативного комитета по практике иммунизации — США, сезон гриппа 2019–2020 гг. MMWR Recomm Rep 2019; 68 (№РР-3): 1-26.).
(e) Эти значения основаны на клиренсе конкретного противовирусного препарата. Для получения конкретной информации, пожалуйста, обратитесь к Grohskopf LA, Alyanak, E, Broder KR, et. al. Профилактика сезонного гриппа и борьба с ним с помощью вакцин: рекомендации Консультативного комитета по практике иммунизации — США, сезон гриппа 2020–21 гг. MMWR Recomm Rep 2020; 69 (№ RR-8: 1-26. Также на https://www.cdc.gov/mmwr/volumes/69/rr/pdfs/rr6908a1-H.pdf.
MMWR Recomm Rep 2020; 69 (№ RR-8: 1-26. Также на https://www.cdc.gov/mmwr/volumes/69/rr/pdfs/rr6908a1-H.pdf.
(f) Эта мера предосторожности распространяется на детей младше 9 месяцев
(g) ВИЧ-инфицированные дети могут получить вакцину против ветряной оспы, если количество CD4 + Т-лимфоцитов ≥15%, и должны получить вакцину MMR, если они в возрасте ≥12 месяцев и не имеют доказательств тяжелой иммуносупрессии в настоящее время (т.е. люди в возрасте ≤5 лет должны иметь процентное содержание CD4 + Т-лимфоцитов [CD4] ≥15% в течение ≥6 месяцев; и люди в возрасте> 5 лет должны иметь процентное содержание CD4 + ≥15% и CD4 + ≥200 лимфоцитов / мм 3 в течение ≥6 месяцев) или другие текущие доказательства иммунитета к кори, краснухе и эпидемическому паротиту. В случаях, когда для людей старше 5 лет доступны только подсчеты CD4 + клеток или только процентные значения CD4 +, оценка тяжелой иммуносупрессии может быть основана на доступных значениях CD4 + (подсчет или процент).В случаях, когда процентное содержание CD4 + недоступно для лиц в возрасте ≤5 лет, оценка тяжелой иммуносупрессии может быть основана на повозрастном количестве CD4 + на момент измерения числа CD4 +; т.е. отсутствие тяжелой иммуносупрессии определяется как ≥6 месяцев выше возрастных критериев количества CD4 +: количество CD4 +> 750 лимфоцитов / мм 3 в возрасте ≤12 месяцев и количество CD4 + ≥500 лимфоцитов / мм 3 в то время как в возрасте от 1 года до 5 лет. Источники: ( 1, 50 ).
(h) вакцины, содержащие вакцину MMR и ветряную оспу, можно вводить в один день.Если вакцины не вводятся в тот же день, их следует разделять не менее 28 дней.
(i) По существу иммуносупрессивная доза стероидов считается ≥2 недель ежедневного приема 20 мг или 2 мг / кг массы тела преднизона или его эквивалента.
(j) семейный анамнез врожденного или наследственного иммунодефицита у родственников первой степени родства (например, родителей, братьев и сестер), если иммунная компетентность потенциального реципиента вакцины не подтверждена клинически или проверена лабораторией.
(k) Если есть подозрение на активный туберкулез, вакцинация MMR должна быть отложена. Вакцинация против кори может временно подавить реактивность туберкулина. Вакцину, содержащую корь, можно вводить в тот же день, что и туберкулиновая кожная вакцина или тестирование IGRA. Если тестирование невозможно провести до дня вакцинации MMR, его следует отложить на ≥4 недель после вакцинации. Если существует острая необходимость в кожной пробе или IGRA, делайте это с пониманием того, что вакцина может снизить реактивность.
(л) Только для RV1, на основе латекса в продукте / упаковке. Обратите внимание, что анафилактическая аллергия на латекс покрывается противопоказанием и также будет изолирована на RV 1 в случае латекса. Подробнее см. (55).
(m) Не сообщалось о побочных эффектах, связанных с использованием аспирина или аспиринсодержащих продуктов после вакцинации против ветряной оспы; однако производитель вакцины рекомендует реципиентам вакцины избегать использования аспирина или продуктов, содержащих аспирин, в течение 6 недель после вакцинации против ветряной оспы из-за связи между применением аспирина и синдромом Рея после ветряной оспы.Следует рассмотреть возможность вакцинации с последующим тщательным наблюдением для детей, страдающих ревматоидным артритом или другими состояниями, требующими терапевтического аспирина. Риск серьезных осложнений, связанных с приемом аспирина, вероятно, будет выше у детей, у которых развивается естественная ветряная оспа, чем у детей, которые получают вакцину, содержащую ослабленный VZV. Не было зарегистрировано никакой связи между синдромом Рея и анальгетиками или жаропонижающими средствами, не содержащими аспирин ».
Начало страницы
ТАБЛИЦА 4-2.Условия, которые неправильно воспринимаются как противопоказания или меры предосторожности для вакцинации (т. Е. Вакцины могут быть введены в этих условиях)
| Вакцина | Состояния, которые обычно ошибочно воспринимаются как противопоказания или меры предосторожности |
|---|---|
| Общие для всех вакцин, включая DTaP, педиатрическую DT, Td взрослых, Tdap подростков и взрослых, IPV, MMR, Hib, гепатит A, гепатит B, ветряную оспу, ротавирус, PCV13, IIV, LAIV, PPSV23, MenACWY, MPSV4, HPV и опоясывающий герпес | Легкое острое заболевание с лихорадкой или без нее Отсутствие предварительного медицинского обследования у хорошо выглядящего человека Текущая противомикробная терапия (a) Фаза выздоровления Преждевременные роды (вакцина против гепатита B является исключением в определенных обстоятельствах) (b ) Недавний контакт с инфекционным заболеванием История аллергии на пенициллин, других невакцинных аллергий, родственников с аллергией или получающих иммунотерапию экстрактом аллергена История GBS (c) |
| DTaP | Лихорадка в течение 48 часов после вакцинации предыдущей дозой АКДС или DTaP Коллапс или состояние, подобное шоку (т.е., эпизод гипотонического гипореактивного ответа) в течение 48 часов после приема предыдущей дозы АКДС / АКДС Припадок ≤3 дней после приема предыдущей дозы АКДС / АКДС Постоянный безутешный плач продолжительностью ≥3 часов в течение 48 часов после приема предыдущей дозы DTP / DTaP Семейный анамнез приступов Семейный анамнез синдрома внезапной детской смерти Семейный анамнез нежелательного явления после введения DTP или DTaP Стабильные неврологические состояния (например, церебральный паралич, хорошо контролируемые судороги или задержка развития) |
| Гепатит B | Беременность Аутоиммунное заболевание (e.g., системная красная волчанка или ревматоидный артрит) |
| ВПЧ | Иммуносупрессия Предыдущий сомнительный или ненормальный тест Папаниколау Известная инфекция ВПЧ Грудное вскармливание Остроконечные кондиломы в анамнезе |
| IIV | Нетяжелая (например, контактная) аллергия на латекс, тимеросал или яйца Одновременное введение кумадина (дженерик: варфарин) или аминофиллина |
| ИПВ | Предыдущее получение ≥1 дозы пероральной полиовакцины |
| LAIV | Поставщики медицинских услуг, которые принимают пациентов с хроническими заболеваниями или нарушенной иммунной системой (исключение составляют медицинские работники для пациентов с тяжелым иммунодефицитом, которым требуется уход в защищенной среде) Грудное вскармливание Контакты людей с хроническими заболеваниями или нарушенной иммунной компетентностью (исключение составляют контакты лиц с тяжелым иммунодефицитом пациенты, нуждающиеся в уходе в защищенной среде) |
| MMR (г), (д) | Положительный туберкулиновый кожный тест Одновременный туберкулиновый кожный тест или исследование высвобождения гамма-интерферона (IGRA) (f) Грудное вскармливание Беременность матери реципиента или другого близкого или домашнего контакта Получатель — женщина детородного возраста Член семьи с иммунодефицитом или домашний контакт Бессимптомная или слабо симптоматическая ВИЧ-инфекция Аллергия на яйца |
| PPSV23 | История инвазивного пневмококкового заболевания или пневмонии |
| Ротавирус | Недоношенность Контактные лица в семье с подавленным иммунитетом Контактные лица беременных в семье |
| Tdap | История лихорадки ≥40. 5 ° C (≥105 ° F) в течение <48 часов после вакцинации предыдущей дозой АКДС или DTaP 5 ° C (≥105 ° F) в течение <48 часов после вакцинации предыдущей дозой АКДС или DTaP История коллапса или шокового состояния (т. Е. Эпизод гипотонического гипореактивного ответа) в течение 48 часов после получения предыдущей дозы АКДС / DTaP История приступов <3 дней после приема предыдущей дозы DTP / DTaP Постоянный безутешный плач, продолжающийся> 3 часов в течение 48 часов после приема предыдущей дозы DTP / DTaP История обширного отека конечностей после DTP / DTaP / Td, который не является реакцией типа Артюса История стабильного неврологического расстройства История плечевого неврита Латексная аллергия, не являющаяся анафилактической Кормление грудью Иммуносупрессия |
| Ветряная оспа | Беременность матери реципиента или другого близкого или домашнего контакта Иммунодефицитный член семьи или домашний контакт (g) Бессимптомная или слабо симптоматическая ВИЧ-инфекция Гуморальный иммунодефицит (e.г., агаммаглобулинемия) |
| Опоясывающий лишай | Терапия низкими дозами метотрексата (≤0,4 мг / кг / неделя), азатиоприна (≤3,0 мг / кг / день) или 6-меркаптопурина (≤1,5 мг / кг / день) для лечения ревматоидного артрита, псориаза, полимиозита , саркоидоз, воспалительное заболевание кишечника или другие состояния Медицинские работники с пациентами с хроническими заболеваниями или нарушенной иммунокомпетентностью Контакты пациентов с хроническими заболеваниями или нарушенной иммунокомпетентностью Неизвестный или неопределенный анамнез ветряной оспы в U.С. рожденного человека |
Сокращения: DT = дифтерийный и столбнячный анатоксины; АКДС = дифтерийный анатоксин, столбнячный анатоксин и коклюш; DTaP = дифтерийный и столбнячный анатоксины и бесклеточный коклюш; GBS = синдром Гийена-Барре; HBsAg = поверхностный антиген гепатита В; Hib = Haemophilus influenzae тип b; ВИЧ = вирус иммунодефицита человека; ВПЧ = вирус папилломы человека; IIV = инактивированная вакцина против гриппа; ИПВ = инактивированный полиовирус; LAIV = живая аттенуированная вакцина против гриппа; MenACWY = четырехвалентная менингококковая конъюгированная вакцина; MMR = корь, эпидемический паротит и краснуха; MPSV4 = четырехвалентная менингококковая полисахаридная вакцина; PCV = пневмококковая конъюгированная вакцина; PPSV23 = пневмококковая полисахаридная вакцина; Td = столбнячный и дифтерийный анатоксины; Tdap = столбнячный анатоксин, редуцированный дифтерийный анатоксин и бесклеточный коклюш.
(a) Антибактериальные препараты могут взаимодействовать с пероральной противотифозной вакциной Ty21a, а некоторые противовирусные препараты могут влиять на вакцины, содержащие ветряную оспу, и вакцины LAIV4.
(b) Вакцинацию против гепатита В следует отложить для младенцев с массой тела <2000 г, если документально подтверждено, что мать отрицательна на HBsAg. Вакцинацию следует начинать в хронологическом возрасте 1 месяц или при выписке из больницы. Младенцам, рожденным от HBsAg-положительных женщин, следует вводить иммуноглобулин против гепатита В и вакцину против гепатита В в течение 12 часов после рождения, независимо от веса.
(c) Исключением является синдром Гийена-Барре в течение 6 недель после введения дозы вакцины против гриппа или вакцины, содержащей столбнячный анатоксин, которые являются мерами предосторожности для вакцин против гриппа и вакцин, содержащих столбнячный анатоксин, соответственно.
(d) вакцины MMR и вакцины против ветряной оспы можно вводить в один и тот же день. Если вакцины не вводятся в тот же день, их следует разделять не менее 28 дней.
(e) ВИЧ-инфицированные дети должны получать иммуноглобулин после контакта с корью.ВИЧ-инфицированные дети могут получить вакцину против ветряной оспы и кори, если количество CD4 + Т-лимфоцитов> 15%. ( 54 ).
(f) Противокоревая вакцинация может временно подавить туберкулиновую реактивность. Вакцину, содержащую корь, можно вводить в тот же день, что и туберкулиновая кожная вакцина или тестирование IGRA. Если тестирование невозможно провести до дня вакцинации MMR, его следует отложить как минимум на 4 недели после вакцинации. Если существует острая необходимость в кожной пробе или IGRA, делайте это с пониманием того, что вакцина может снизить реактивность.
(g) Если у вакцинированного наблюдается предположительно связанная с вакциной сыпь через 7-25 дней после вакцинации, этому человеку следует избегать прямого контакта с людьми с ослабленным иммунитетом на время появления сыпи.
Начало страницы
Список литературы
- Штаб-квартира Маклина, Fiebelkorn AP, Temte JL, Wallace GS. Профилактика кори, краснухи, синдрома врожденной краснухи и эпидемического паротита, 2013 г .: сводные рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 2013; 62 (RR-4): 1-34.
- Национальный консультативный комитет по вакцинам. Стандарты практики иммунизации детей и подростков. Педиатрия. 2003; 112 (4): 958-963.
- Рубин Л., Левин М., Юнгман П. и др. Руководство IDSA по клинической практике для вакцинации хозяев с ослабленным иммунитетом, 2013 г. Clin Infect Dis. 2014; 58 (3): e44-100. DOI: 10.1093 / cid / cit684
- Крогер А., Аткинсон В., Пикеринг Л. Общие методы иммунизации.В: Плоткин С., Оренштейн В., Оффит П., ред. Вакцины . 6 -е изд. Китай: Эльзевьер Сондерс; 2013: 88-111.
- CDC. Дифтерия, столбняк и коклюш: рекомендации по применению вакцины и другим профилактическим мерам. Рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 1991; 40 (RR-10): 1-28.
- CDC. Добавление истории инвагинации как противопоказания к вакцинации против ротавируса. MMWR Morb Mortal Wkly Rep. 2011; 60 (41): 1427.
- Сибер Г.Р., Вернер Б.Г., Хэлси Н.А. и др. Вмешательство иммуноглобулина при иммунизации против кори и краснухи. J Pediatr. 1993; 122 (2): 204-211. DOI: 10.1016 / S0022-3476 (06) 80114-9
- Halsey NA, Boulos R, Mode F и др. Ответ на вакцину против кори у гаитянских младенцев от 6 до 12 месяцев. Влияние материнских антител, недоедания и сопутствующих заболеваний. N Engl J Med. 1985; 313 (9): 544-549. DOI: 10.1056 / nejm1985082
904
- Ndikuyeze A, Munoz A, Stewart J, et al.Иммуногенность и безопасность вакцины против кори у больных африканских детей. Int J Epidemiol. 1988; 17 (2): 448-455.
 DOI: 10.1093 / ije / 17.2.448
DOI: 10.1093 / ije / 17.2.448 - Lindegren ML, Atkinson WL, Farizo KM, Stehr-Green PA. Вакцинация против кори в педиатрических отделениях неотложной помощи во время вспышки кори. JAMA. 1993; 270 (18): 2185-2189. DOI: 10.1001 / jama.1993.03510180055033
- Аткинсон В., Марковиц Л., Боуман А. и др. Серологический ответ на вакцинацию против кори среди больных детей [Резюме 422].32-я международная конференция по противомикробным препаратам и химиотерапии; 1992; Анахайм, Калифорния.
- Оренштейн В., Родевальд Л., Хинман А., Шухат А. Иммунизация в Соединенных Штатах. В: Плоткин С., Оренштейн В., Оффит П., ред. Вакцины . 5-е изд. Китай: Сондерс / Эльзевир; 2008: 1479-1510.
- Льюис Т., Осборн Л.М., Льюис К., Брокерт Дж., Якобсен Дж., Черри Дж. Д.. Влияние знаний и мнения родителей на показатели вакцинации против дифтерии, столбняка и коклюша в течение 12 месяцев. Am J Dis Child. 1988; 142 (3): 283-286. DOI: 10.1001 / архпеди.1988.02150030053018
- Farizo KM, Stehr-Green PA, Markowitz LE, Patriarca PA. Уровни вакцинации и упущенные возможности вакцинации против кори: аудит записи в государственной педиатрической клинике. Педиатрия. 1992; 89 (4 Pt 1): 589-592.
- Центры услуг Medicare и Medicaid. Обзор технических характеристик мер, отображаемых в больницах, сравните по состоянию на 14 декабря 2006 г. pdf icon [11 страниц] external icon. 2006. По состоянию на 9 марта 2017 г.
- Донован Р., Сотхилл Дж. Ф. Иммунологические исследования у детей, перенесших тонзиллэктомию. Clin Exp Immunol. 1973; 14 (3): 347-357.
- Пури П., Рин Ди-джей, Браун О., Блейк П., Гвини Э. Дж. Реакция лимфоцитов после операции у новорожденного. Arch Dis Child. 1979; 54 (8): 599-603. DOI: 10.1136 / adc.54.8.599
- Mollitt DL, Steele RW, Marmer DJ, Stevers Golladay E, Costas S. Хирургически индуцированные иммунологические изменения у ребенка. J Pediatr Surg. 1984; 19 (6): 818-822.
 DOI: 10.1016 / S0022-3468 (84) 80376-0
DOI: 10.1016 / S0022-3468 (84) 80376-0 - Моллитт Д.Л., Мармер Д.И., Стил Р.В. Возрастные вариации функции лимфоцитов у послеоперационного ребенка. J Pediatr Surg. 1986; 21 (7): 633-635. DOI: 10.1016 / S0022-3468 (86) 80420-1
- Курц Р., Пфайфер К.П., Зауэр Х. Иммунологический статус у младенцев и детей после операции. Инфекция. 1983; 11 (2): 104-113. DOI: 10.1007 / BF01641075
- Merry C, Puri P, Reen DJ. Влияние обширного хирургического вмешательства на хемотаксис нейтрофилов и полимеризацию актина у новорожденных и детей. J Pediatr Surg. 1997; 32 (6): 813-817. DOI: 10.1016 / S0022-3468 (97)
-6 - Platt MP, Lovat PE, Watson JG, Aynsley-Green A. Влияние анестезии и хирургического вмешательства на популяции и функцию лимфоцитов у младенцев и детей. J Pediatr Surg. 1989; 24 (9): 884-887. DOI: 10.1016 / S0022-3468 (89) 80588-3
- Mattila-Vuori A, Salo M, Iisalo E. Иммунный ответ у младенцев, перенесших гипсовую повязку: сравнение галотана и сбалансированной анестезии. Can J Anaesth. 1999; 46 (11): 1036-1042. DOI: 10.1007 / bf03013198
- Espanol T, Todd GB, Soothill JF. Влияние анестезии на ответ лимфоцитов на фитогемагглютинин. Clin Exp Immunol. 1974; 18 (1): 73-79.
- Хаузер Г.Дж., Чан М.М., Кейси В.Ф., Мидгли FM, Холбрук ПР. Иммунная дисфункция у детей после коррекционных операций по поводу врожденного порока сердца. Crit Care Med. 1991; 19 (7): 874-881.
- Пури П., Ли А., Рин Диджей. Дифференциальная восприимчивость лимфоцитов новорожденных к иммуносупрессивным эффектам анестезии и хирургического вмешательства. Pediatr Surg Int. 1992; 7 (1): 47-50. DOI: 10.1007 / bf00181002
- Hansen TG, Tonnesen E, Andersen JB, Toft P, Bendtzen K. Периоперационный цитокиновый ответ у младенцев и детей раннего возраста после обширной операции. Eur J Anaesthesiol. 1998; 15 (1): 56-60. DOI: 10.1046 / j.1365-2346.
 1998.00230.x
1998.00230.x- Mattila-Vuori A, Salo M, Iisalo E, Pajulo O, Viljanto J. Местный и системный иммунный ответ на хирургическое вмешательство у детей под сбалансированной анестезией. Paediatr Anaesth. 2000; 10 (4): 381-388. DOI: 10.1046 / j.1460-9592.2000.00505.x
- Romeo C, Cruccetti A, Turiaco A и др. Активность моноцитов и нейтрофилов после небольшого хирургического стресса. J Pediatr Surg. 2002; 37 (5): 741-744. DOI: 10.1053 / jpsu.2002.32268
- Vuori A, Salo M, Viljanto J, Pajulo O, Pulkki K, Nevalainen T. Влияние послеоперационного обезболивания с использованием нестероидных противовоспалительных анальгетиков, опиоидов или эпидуральной блокады на системные и местные иммунные реакции у детей. Acta Anaesthesiol Scand. 2004; 48 (6): 738-749. DOI: 10.1111 / j.1399-6576.2004.00404.x
- Siebert JN, Posfay-Barbe KM, Habre W, Siegrist CA. Влияние анестезии на иммунные реакции и ее влияние на вакцинацию детей: обзор доказательств. Paediatr Anaesth. 2007; 17 (5): 410-420. DOI: 10.1111 / j.1460-9592.2006.02120.x
- Карри Дж. Вакцинация: настоящая проблема для анестезии и хирургии? Paediatr Anaesth. 2006; 16 (5): 501-503. DOI: 10.1111 / j.1460-9592.2006.01898.x
- Siebert J, Posfay-Barbe KM, Habre W, Siegrist C-A. Ответ автора. Paediatr Anaesth. 2007; 17 (12): 1218-1220. DOI: 10.1111 / j.1460-9592.2007.02369.x
- Нафиу О.О., Льюис И. Вакцинация и анестезия: больше вопросов, чем ответов. Paediatr Anaesth. 2007; 17 (12): 1215-1215. DOI: 10.1111 / j.1460-9592.2007.02318.x
- Short JA, Ван дер Уолт JH, Зоанетти, округ Колумбия. Ответ автора. Paediatr Anaesth. 2007; 17 (12): 1215-1216.DOI: 10.1111 / j.1460-9592.2007.02321.x
- Марин М., Бродер К.Р., Темте Д.Л., Снайдер Д.Е., Сьюард Дж.Ф. Использование комбинированной вакцины против кори, эпидемического паротита, краснухи и ветряной оспы: рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 2010; 59 (RR-3): 1-12.
- Szilagyi PG, Rodewald LE. Упущенные возможности для иммунизации: обзор доказательств. J Public Health Manag Pract. 1996; 2 (1): 18-25. DOI: 10.1097 / 00124784-199600210-00005
- CDC.Использование вакцины против коклюша дифтерийного анатоксина, столбняка и бесклеточного коклюша в виде серии из пяти доз. Дополнительные рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 2000; 49 (RR-13): 1-8.
- Fiore AE, Wasley A, Bell BP. Профилактика гепатита А с помощью активной или пассивной иммунизации: рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 2006; 55 (RR-7): 1-23.
- Mast EE, Margolis HS, Fiore AE и др.Комплексная стратегия иммунизации для устранения передачи инфекции вируса гепатита В в Соединенных Штатах: рекомендации Консультативного комитета по практике иммунизации (ACIP), часть 1: иммунизация младенцев, детей и подростков. MMWR Recomm Rep. 2005; 54 (RR-16): 1-31.
- Briere EC, Rubin L, Moro PL, Cohn A, Clark T, Messonnier N. Профилактика и борьба с заболеванием Haemophilus influenzae типа b: рекомендации консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 2014; 63 (RR-1): 1-14.
- Марковиц Л., Данн Е., Сарайя М. и др. Вакцинация против вируса папилломы человека: рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 2014; 63 (RR-05): 1-30.
- Grohskopf LA, Sokolow LZ, Olsen SJ, et al. Профилактика сезонного гриппа и борьба с ним с помощью вакцин. Рекомендации Консультативного комитета по практике иммунизации — США, сезон гриппа 2016–17 гг. MMWR Recomm Rep 2016; 65 (No.РР-5): 1-54.
- Prevots DR, Burr RK, Sutter RW, Murphy TV. Профилактика полиомиелита в США. Обновленные рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 2000; 49 (RR-5): 1-22; викторина CE21-27.
- Cohn AC, MacNeil JR, Clark TA и др. Профилактика менингококковой инфекции и борьба с ней: рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 2013; 62 (RR-2): 1-28.
- Bexsero Package Inser: внешний значок (дата обращения: 05.04.17).
- Trumenba Package Insert pdf icon [15 страниц] внешний значок (дата обращения 05.04.17).
- Билуха О.О., Розенштейн Н. Профилактика и борьба с менингококковой инфекцией. Рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 2005; 54 (RR-7): 1-21.
- Консультативный комитет по практике иммунизации. Профилактика пневмококковой инфекции у детей грудного и раннего возраста. Рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Morb Mortal Wkly Rep. 2000; 49 (RR-9): 1-35.
- CDC. Профилактика пневмококковой инфекции: рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 1997; 46 (RR-8): 1-24.
- Бродер К.Р., Кортезе М.М., Искандер Дж.К. и др. Профилактика столбняка, дифтерии и коклюша среди подростков: использование столбнячного анатоксина, редуцированного дифтерийного анатоксина и бесклеточных коклюшных вакцин Рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 2006; 55 (RR-3): 1-34.
- Марин М., Гурис Д., Чавес СС, Шмид С., Сьюард Дж. Ф. Профилактика ветряной оспы: рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 2007; 56 (RR-4): 1-40.
- Harpaz R, Ортега-Санчес И.Р., Сьюард Дж. Ф. Профилактика опоясывающего герпеса: рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 2008; 57 (RR-5): 1-30; викторина CE32-34.
- Grohskopf LA, Olsen SJ, Sokolow LZ, et al.Профилактика сезонного гриппа и борьба с ним с помощью вакцин: рекомендации Консультативного комитета по практике иммунизации (ACIP) — США, сезон гриппа 2014-15 гг. MMWR Morb Mortal Wkly Rep. 2014; 63 (32): 691-697.
- Cortese MM, Parashar UD. Профилактика ротавирусного гастроэнтерита среди младенцев и детей: рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 2009; 58 (RR-2): 1-25.
- Американская академия педиатрии.Пассивная иммунизация. В: Пикеринг Л., Бейкер С., Кимберлин Д., Лонг С., ред. Красная книга: Отчет Комитета по инфекционным болезням 2012 . 28 изд. Деревня Элк-Гроув, Иллинойс: Американская академия педиатрии; 2012.
Начало страницы
Промежуточные клинические рекомендации по применению вакцины против COVID-19
Сводка последних изменений (последнее обновление 5 марта 2021 г.):
Ключевые моменты
Консультативный комитет по практике иммунизации (ACIP) выпустил временные рекомендации по использованию вакцин Pfizer-BioNTech, Moderna и Janssen (Johnson & Johnson) COVID-19 для профилактики коронавирусной болезни 2019 (COVID-19) в США. Состояния.Эти клинические соображения предоставляют поставщикам медицинских услуг и должностным лицам общественного здравоохранения дополнительную информацию об использовании вакцин против COVID-19.
Фон
Консультативный комитет по практике иммунизации (ACIP) выпустил временные рекомендации по использованию вакцин Pfizer-BioNTech, Moderna и Janssen (Johnson & Johnson) COVID-19 для профилактики коронавирусной болезни 2019 (COVID-19) в США. Состояния. Вакцины Pfizer-BioNTech и Moderna представляют собой липидные наночастицы и модифицированные нуклеозидами мРНК-вакцины, кодирующие гликопротеин SARS-CoV-2 перед слиянием, вызывающий COVID-19.Вакцина Янссена представляет собой рекомбинантный некомпетентный к репликации вектор аденовируса типа 26 (Ad26), кодирующий стабилизированный спайковый гликопротеин SARS-CoV-2 перед слиянием. Ни одна из разрешенных в настоящее время вакцин против COVID-19 не является живыми вирусными вакцинами.
Эти временные клинические соображения CDC основаны на данных, представленных в Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) для разрешения на экстренное использование (EUA) вакцин, из других источников данных, общих рекомендаций по передовой практике иммунизации и мнения экспертов.Эти соображения относятся только к вакцинам, разрешенным в настоящее время в США (например, вакцинам Pfizer-BioNTech, Moderna и Janssen COVID-19). Соображения будут обновлены, когда станет доступна дополнительная информация или если будут разрешены дополнительные вакцины.
В дополнение к следующим соображениям, при использовании вакцины против COVID-19 со значком Pfizer-BioNTechexternal, значком Modernaexternal и значком Janssenexternal следует учитывать условия использования, хранения, обращения и введения, описанные в инструкции по применению.
Уполномоченные возрастные группы
Согласно EUA, следующие возрастные группы имеют право на вакцинацию:
- Pfizer-BioNTech: возраст ≥16 лет
- Moderna: возраст ≥18 лет
- Янссен: возраст ≥18 лет
Дети и подростки, не входящие в эти разрешенные возрастные группы, в настоящее время не должны проходить вакцинацию от COVID-19.
Чтобы получать обновления об этой странице по электронной почте, введите свой адрес электронной почты:
Управление вакцинами
вакцины против COVID-19 вводятся внутримышечно в виде двухдозовой серии или однократной дозы.
Следует проводить однократную действительную серию вакцинации (т. Е. Серию вакцины против COVID-19 с двумя дозами мРНК или однократной дозой вакцины Janssen COVID-19). Людям не рекомендуется делать более одной полной серии вакцинации против COVID-19.
Интервал между дозами мРНК
Вторую дозу вакцин Pfizer-BioNTech и Moderna следует вводить как можно ближе к рекомендуемому интервалу, но не ранее , чем рекомендуется (т.е., 3 недели [Pfizer-BioNTech] или 1 месяц [Moderna]). Однако вторые дозы, введенные в течение льготного периода на 4 дня раньше, чем рекомендованная дата для второй дозы, по-прежнему считаются действительными. Если невозможно придерживаться рекомендованного интервала и отсрочка вакцинации неизбежна, вторая доза вакцин Pfizer-BioNTech и Moderna COVID-19 может быть введена в течение 6 недель (42 дней) после первой дозы. В настоящее время доступны лишь ограниченные данные об эффективности вакцин против мРНК COVID-19, вводимых за пределами этого окна.
Информация о предотвращении, сообщении и устранении ошибок введения вакцины COVID-19 приведена в Приложении A. Об ошибках введения вакцины следует сообщать на внешний значок Системы сообщений о побочных эффектах вакцин (VAERS).
Взаимозаменяемость вакцин против COVID-19
При наличии показаний можно использовать любую разрешенную в настоящее время вакцину против COVID-19; ACIP не указывает предпочтения продукта. Однако вакцины от COVID-19 не взаимозаменяемы.
мРНК вакцины COVID-19 (Pfizer-BioNTech и Moderna)
Безопасность и эффективность серии смешанных продуктов не оценивались.Обе дозы серии должны быть дополнены одним и тем же продуктом.
Стратегии, обеспечивающие получение пациентами второй дозы с соответствующим продуктом и интервалом между дозами, включают:
- Предоставление реципиентам вакцинации карточек вакцинации COVID-19, просьба к получателям принести свою карточку на прием для приема второй дозы и поощрение получателей сделать резервную копию (например, сфотографировав карточку на свой телефон)
- Поощрение получателей вакцины к участию в v-safe , бесплатном инструменте для смартфонов, который использует текстовые сообщения и веб-опросы для обеспечения персонализированных проверок состояния здоровья, а также напоминаний о второй дозе
- Поощрение реципиентов вакцины к регистрации в VaxText SM , бесплатной платформе на основе текстовых сообщений, которая предоставляет напоминания о второй дозе вакцинации COVID-19
- Регистрация вакцинации каждого реципиента в информационной системе иммунизации (IIS)
- Запись информации о введении вакцины в медицинскую карту пациента
- Запись на прием для второй дозы вакцины до отъезда реципиента вакцины, чтобы повысить вероятность того, что пациенты появятся в том же месте вакцинации для второй дозы
Используя вышеуказанные стратегии, необходимо приложить все усилия, чтобы определить, какой вакцинный продукт был получен в качестве первой дозы, чтобы обеспечить завершение серии вакцины с тем же продуктом.В исключительных ситуациях, когда вакцина, вводимая для первой дозы, не может быть определена или больше не доступна, любая доступная мРНК вакцина COVID-19 может быть введена с минимальным интервалом 28 дней между дозами для завершения серии вакцинации мРНК COVID-19. . В ситуациях, когда тот же самый продукт вакцины мРНК временно недоступен, предпочтительно отложить дозу 2 и (до 6 недель) для получения того же продукта, чем для получения смешанной серии с использованием другого продукта.Если две дозы различных продуктов вакцины против COVID-19 с мРНК вводятся в этих ситуациях (или случайно), никаких дополнительных доз любого продукта в настоящее время не рекомендуется.
Безопасность и эффективность вакцины Janssen COVID-19, вводимой после мРНК вакцины COVID-19, не установлены. Однако в ограниченных, исключительных ситуациях, когда пациент получил первую дозу вакцины с мРНК COVID-19, но не может завершить серию с той же или другой вакциной с мРНК COVID-19 (например,g., из-за противопоказаний), разовая доза вакцины Janssen COVID-19 может рассматриваться как минимум через 28 дней после введения дозы мРНК вакцины COVID-19. См. Раздел «Противопоказания и меры предосторожности» для получения дополнительной информации об использовании вакцины Janssen COVID-19 и дополнительных мерах предосторожности у людей с противопоказанием к вакцинации мРНК COVID-19. Следует считать, что пациенты, получившие вакцину Janssen COVID-19 после введения дозы мРНК вакцины COVID-19, получили действительную однократную вакцинацию Janssen, а не серию смешанных вакцинаций.
Совместное введение с другими вакцинами
Ни одна из разрешенных в настоящее время вакцин против COVID-19 не является живыми вирусными вакцинами. Поскольку данных о безопасности и эффективности вакцин против COVID-19, вводимых одновременно с другими вакцинами, недостаточно, серию вакцин следует обычно вводить отдельно с минимальным интервалом в 14 дней до или после введения любой другой вакцины. Однако COVID-19 и другие вакцины можно вводить в течение более короткого периода в ситуациях, когда считается, что польза от вакцинации перевешивает потенциальные неизвестные риски совместного введения вакцины (например,g., вакцинация столбнячным анатоксином как часть лечения ран, вакцинация против бешенства для постконтактной профилактики, вакцинация против кори или гепатита A во время вспышки) или во избежание препятствий или задержек в вакцинации COVID-19 (например, в долгосрочной перспективе). проживающие в учреждении временного ухода или медицинский персонал, получивший вакцинацию от гриппа или другие прививки до или при поступлении или при поступлении на работу). Если вакцины COVID-19 вводятся в течение 14 дней после другой вакцины, повторять дозы для любой вакцины не нужно.
Бустерные дозы
Необходимость и время введения бустерных доз COVID-19 не установлены. Никаких дополнительных доз в настоящее время не рекомендуется.
Вакцинация против COVID-19 и инфекция SARS-CoV-2
Люди с предыдущей или текущей инфекцией SARS-CoV-2
Данные клинических испытаний показывают, что разрешенные в настоящее время вакцины против COVID-19 можно безопасно вводить людям с признаками перенесенной ранее инфекции SARS-CoV-2. Людям следует предлагать вакцинацию независимо от предшествующей симптоматической или бессимптомной инфекции SARS-CoV-2 в анамнезе.Тестирование на вирусы для оценки острой инфекции SARS-CoV-2 или серологическое тестирование для оценки предшествующей инфекции не рекомендуется для целей принятия решения о вакцинации.
Вакцинацию людей с известной текущей инфекцией SARS-CoV-2 следует отложить до тех пор, пока человек не выздоровеет от острого заболевания (если у человека были симптомы) и они не будут соответствовать критериям для прекращения изоляции. Эта рекомендация применима к людям, которые перенесли инфекцию SARS-CoV-2 до получения какой-либо дозы вакцины, и тем, кто заражен SARS-CoV-2 после первой дозы вакцины мРНК, но до получения второй дозы.
Хотя не существует рекомендуемого минимального интервала между инфицированием и вакцинацией, имеющиеся данные свидетельствуют о том, что риск повторного инфицирования SARS-CoV-2 невелик в течение нескольких месяцев после первоначального заражения, но со временем может возрасти из-за ослабления иммунитета. Таким образом, хотя запас вакцины остается ограниченным, люди с недавно задокументированной острой инфекцией SARS-CoV-2 могут при желании временно отложить вакцинацию, осознавая, что риск повторного заражения и, следовательно, потребность в вакцинации может возрасти со временем после первоначального заражения. инфекционное заболевание.
Люди, ранее получавшие пассивную терапию антителами
В настоящее время нет данных о безопасности и эффективности вакцин против COVID-19 у людей, которые получали моноклональные антитела или выздоравливающую плазму в рамках лечения COVID-19. Основываясь на предполагаемом периоде полураспада таких методов лечения и доказательствах, свидетельствующих о том, что повторное инфицирование редко встречается в течение 90 дней после первоначального заражения, вакцинацию следует отложить как минимум на 90 дней. Это мера предосторожности до тех пор, пока не станет доступной дополнительная информация, чтобы избежать потенциального вмешательства терапии антителами в индуцированные вакцинами иммунные ответы.Эта рекомендация относится к людям, которые получают терапию пассивными антителами до получения какой-либо дозы вакцины, и к тем, кто получает терапию пассивными антителами после первой дозы мРНК-вакцины, но до второй дозы, и в этом случае вторая доза должна быть отложена как минимум на 90 лет. дни после получения терапии антителами. Получение пассивной терапии антителами в течение последних 90 дней не является противопоказанием к вакцинации от COVID-19. Дозы вакцины COVID-19, полученные в течение 90 дней после получения пассивной терапии антителами, не нужно повторять.
Для людей, получающих терапию антителами, не специфичную для лечения COVID-19 (например, внутривенный иммуноглобулин, RhoGAM), введение вакцины COVID-19 одновременно или с любым интервалом до или после получения продукта, содержащего антитела, вряд ли существенно повлияет на развитие защитного ответа антител. Таким образом, не существует рекомендуемого минимального интервала между терапией антителами, неспецифичными для лечения COVID-19, и вакцинацией против COVID-19.
Вакцинированные люди, у которых впоследствии развился COVID-19
Для вакцинированных людей, которые впоследствии переболели COVID-19, предварительное получение вакцины COVID-19 не должно влиять на решения о лечении (включая использование моноклональных антител, выздоравливающую плазму, противовирусное лечение или введение кортикостероидов) или на время проведения такого лечения.
Если человек полностью вакцинирован (т. Е. Через ≥2 недель после завершения серии двух доз мРНК или однократной дозы вакцины Янссен) и имеет положительный результат на SARS-CoV-2, медицинским работникам и местным департаментам здравоохранения рекомендуется запросить необходимо взять образец и сообщить о случившемся в государственный департамент здравоохранения. CDC будет работать с департаментом здравоохранения штата над сбором информации о данном случае. Кроме того, информацию об этих случаях следует сообщать в VAERS.
Вакцинация людей с известным контактом с COVID-19 или во время вспышек COVID-19
Вакцины
COVID-19 в настоящее время не рекомендуются для управления вспышкой или для постконтактной профилактики, чтобы предотвратить заражение SARS-CoV-2 у человека с известным контактом.Поскольку средний инкубационный период COVID-19 составляет 4–5 дней, маловероятно, что доза вакцины COVID-19 обеспечит адекватный иммунный ответ в течение инкубационного периода для эффективной постконтактной профилактики.
Люди в сообществе или амбулаторных условиях, которые подверглись воздействию COVID-19, не должны проходить вакцинацию до окончания периода карантина, чтобы избежать потенциального контакта с медицинским персоналом и другими лицами во время посещения вакцинации. Эта рекомендация также применима к людям с известным контактом с COVID-19 до получения второй дозы мРНК вакцины.
Резиденты или пациенты с известным контактом с COVID-19 в коллективных медицинских учреждениях (например, в учреждениях долгосрочного ухода) или в местах скопления вне медицинских учреждений (например, исправительных учреждениях и местах содержания под стражей, приютах для бездомных) могут быть вакцинированы. В этих условиях заражение и передача SARS-CoV-2 могут происходить неоднократно в течение длительных периодов времени, а медицинский и другой персонал уже находится в тесном контакте с жителями. Люди, проживающие в местах скопления людей (медицинские и немедицинские), которые подверглись заражению и ожидают результатов тестирования на SARS-CoV-2, могут быть вакцинированы, если у них нет симптомов, соответствующих COVID-19.Вакцинаторы должны использовать соответствующие процедуры профилактики и контроля инфекций.
Рекомендации по вакцинации людей с определенными сопутствующими заболеваниями
Любая разрешенная в настоящее время вакцина против COVID-19 может вводиться людям с сопутствующими заболеваниями, у которых нет противопоказаний к вакцинации; ACIP не указывает предпочтения продукта. Клинические испытания продемонстрировали аналогичные профили безопасности и эффективности у людей с некоторыми сопутствующими заболеваниями, в том числе с повышенным риском тяжелого COVID-19, по сравнению с людьми без сопутствующих заболеваний.Дополнительная информация для людей с конкретными заболеваниями приведена ниже.
Люди с ослабленным иммунитетом
Люди с ВИЧ-инфекцией или другими иммунодефицитными состояниями, а также люди, принимающие иммунодепрессанты или терапию, могут подвергаться повышенному риску тяжелой формы COVID-19. Нет данных для установления безопасности и эффективности вакцины COVID-19 в этих группах. Однако разрешенные в настоящее время вакцины против COVID-19 не являются живыми вакцинами и поэтому могут безопасно вводиться людям с ослабленным иммунитетом.Люди со стабильной ВИЧ-инфекцией были включены в клинические испытания вакцины COVID-19, хотя данные остаются ограниченными.
Люди с ослабленным иммунитетом могут пройти вакцинацию от COVID-19. В настоящее время данных недостаточно для определения оптимального времени вакцинации против COVID-19 среди людей, которые планируют получать иммуносупрессивную терапию. Однако, исходя из общих передовых практик вакцинации людей с ослабленным иммунитетом, в идеале вакцинацию против COVID-19 следует завершить как минимум за две недели до начала иммуносупрессивной терапии.Если невозможно заранее ввести полную серию вакцины против COVID-19 (т.е. две дозы мРНК-вакцины или одну дозу вакцины Janssen COVID-19), люди, получающие иммуносупрессивную терапию, все равно могут пройти вакцинацию против COVID-19. При принятии решения об отложении иммуносупрессивной терапии до завершения вакцинации против COVID-19 следует учитывать риски человека, связанные с его основным заболеванием.
Тестирование на антитела не рекомендуется для оценки иммунитета к SARS-CoV-2 после вакцинации против COVID-19.В настоящее время ревакцинация не рекомендуется после того, как люди, получившие вакцину против COVID-19 во время химиотерапии или лечения другими иммуносупрессивными препаратами, восстановят иммунную компетентность. Рекомендации по повторной вакцинации или дополнительным дозам вакцины COVID-19 могут быть обновлены при появлении дополнительной информации.
Людей следует проинформировать о неизвестном профиле безопасности и эффективности вакцины для популяций с ослабленным иммунитетом, о возможности снижения иммунного ответа и о необходимости продолжать следовать текущим рекомендациям по защите от COVID-19.
Люди с аутоиммунными заболеваниями
Нет данных о безопасности и эффективности вакцин против COVID-19 у людей с аутоиммунными заболеваниями, хотя эти люди имели право на участие в клинических испытаниях мРНК вакцины COVID-19. Не наблюдалось дисбаланса в возникновении симптомов, связанных с аутоиммунными состояниями или воспалительными расстройствами, у участников клинических испытаний, которые получали вакцину COVID-19, по сравнению с плацебо. Люди с аутоиммунными заболеваниями могут получить любую разрешенную вакцину против COVID-19.
Люди с синдромом Гийена-Барре в анамнезе
Не было зарегистрировано случаев синдрома Гийена-Барре (СГБ) после вакцинации среди участников клинических испытаний мРНК вакцины COVID-19. Один случай СГБ был зарегистрирован у участника группы вакцины в клиническом испытании вакцины Janssen COVID-19 по сравнению с одним случаем СГБ среди тех, кто получал плацебо. За некоторыми исключениями, общие руководящие принципы ACIP по иммунизации не включают анамнез СГБ в качестве противопоказания или меры предосторожности к вакцинации.Люди с историей СГБ могут получить вакцинацию от COVID-19. О любом возникновении GBS после вакцинации COVID-19 следует сообщать в VAERS.
Люди с параличом Белла в анамнезе
случаев паралича Белла было зарегистрировано после вакцинации участников клинических испытаний вакцины COVID-19. Однако FDA не считает, что частота таких случаев превышает ожидаемую для населения в целом, и не пришло к выводу, что эти случаи были причинно связаны с вакцинацией.Пост-авторизационный надзор за безопасностью будет важен для дальнейшей оценки любой возможной причинно-следственной связи. В отсутствие таких доказательств люди с параличом Белла в анамнезе могут получить вакцину от COVID-19. О любых случаях паралича Белла после вакцинации против COVID-19 следует сообщать в VAERS.
Люди с историей использования кожных наполнителей используют
В редких случаях люди, получившие кожные наполнители, могут испытывать отек в месте инъекции наполнителя (обычно на лице или губах) или рядом с ним после введения дозы мРНК вакцины COVID-19 (подобных случаев не наблюдалось в случае вакцины Janssen COVID-19. клинические испытания вакцины).Припухлость носит временный характер и проходит после медикаментозного лечения, включая терапию кортикостероидами. Вакцины против COVID-19 можно вводить людям, которые получали инъекционные кожные наполнители, у которых нет противопоказаний или мер предосторожности для вакцинации. Тем не менее, этим людям следует посоветовать связаться со своим врачом для оценки, если после вакцинации у них возникнет отек на участке кожного наполнителя или рядом с ним.
Вакцинация беременных и кормящих людей
Любая из разрешенных в настоящее время вакцин против COVID-19 может вводиться беременным или кормящим людям; ACIP не указывает предпочтения продукта.
Беременные
Данные наблюдений показывают, что беременные с COVID-19 имеют повышенный риск тяжелого заболевания, включая заболевание, приводящее к поступлению в реанимацию, механическую вентиляцию легких, экстракорпоральную мембранную оксигенацию или смерть, хотя абсолютный риск таких исходов невелик. Кроме того, они могут подвергаться повышенному риску неблагоприятных исходов беременности, таких как преэклампсия, коагулопатия и преждевременные роды.
Данные о безопасности вакцины против COVID-19 для беременных ограничены.У животных, получавших вакцины Pfizer-BioNTech, Moderna или Janssen COVID-19 до или во время беременности, не было продемонстрировано никаких опасений по поводу безопасности женского репродуктивного здоровья или эмбрионального, эмбрионального или постнатального развития. Кроме того, платформа аденовирусного вектора, используемая в вакцине Janssen COVID-19, также использовалась для других программ разработки вакцины Janssen, которые включали беременных людей, вакцинированных в течение любого триместра, в том числе в крупномасштабных испытаниях вакцинации против Эболы. В этих испытаниях не было установлено, что неблагоприятные исходы, связанные с беременностью, в том числе исходы для младенцев, связаны с вакциной.
На основании имеющихся данных эксперты полагают, что вакцины против COVID-19 вряд ли будут представлять опасность для беременного человека или плода, поскольку санкционированные в настоящее время вакцины против COVID-19 не реплицируются и не могут вызвать инфекцию ни у матери, ни у плода. Нет никаких доказательств риска для плода в результате вакцинации беременных женщин нереплицирующимися вакцинами в целом. Однако потенциальные риски вакцин против COVID-19 для беременных и плода неизвестны, поскольку эти вакцины не изучались на беременных.Клинические испытания для оценки безопасности и эффективности вакцин против COVID-19 у беременных продолжаются или планируются. Производители вакцин также следят за результатами клинических испытаний беременных женщин.
Беременные могут выбрать вакцину против COVID-19. Разговор между пациентом и его клинической командой может помочь в принятии решения об использовании вакцины COVID-19, хотя разговор с врачом перед вакцинацией не требуется. Принимая решение, беременные люди и их медицинские работники должны учитывать уровень передачи COVID-19 в сообществе, личный риск пациента заразиться COVID-19, риски COVID-19 для пациента и потенциальные риски для плода, эффективность вакцины, побочные эффекты вакцины и ограниченные данные о вакцине во время беременности.Беременным, которые решили получить вакцину от COVID-19, рекомендуется зарегистрироваться в v-safe . Регистр v-safe был создан для отслеживания результатов среди вакцинированных беременных. На основании информации, предоставленной самими пациентами, среди беременных реципиентов вакцины, включенных в реестр v-safe , не наблюдалось никаких конкретных сигналов безопасности. Однако для полной оценки исходов беременности и родов необходимо длительное наблюдение.
При использовании вакцины COVID-19 у беременных могут возникать побочные эффекты, аналогичные тем, которые ожидаются у небеременных людей.Ацетаминофен может быть предложен в качестве альтернативы беременным, страдающим лихорадкой (которая была связана с неблагоприятным исходом беременности) или другими поствакцинальными симптомами.
Нет рекомендаций по регулярному тестированию на беременность до вакцинации от COVID-19. Тем, кто пытается забеременеть, не нужно избегать беременности после вакцинации от COVID-19. Нет никаких доказательств того, что какие-либо вакцины от COVID-19 влияют на фертильность в будущем.
Кормящие
Нет данных о безопасности вакцин против COVID-19 для кормящих людей или о влиянии вакцин от COVID-19 на грудного ребенка, выработку или выделение молока.Поскольку неживые вакцины не представляют риска для кормящих людей или их младенцев, вакцины COVID-19 также не считаются опасными. Таким образом, кормящие люди могут выбрать вакцинацию.
Вакцинация детей и подростков
Подростки в возрасте 16–17 лет включены в число лиц, имеющих право на вакцинацию Pfizer-BioNTech COVID-19 в соответствии с EUA. Хотя данные по безопасности и эффективности вакцин в этой возрастной группе ограничены, нет никаких биологически правдоподобных причин, по которым профили безопасности и эффективности отличались бы от тех, которые наблюдаются у людей в возрасте 18 лет и старше.Подростки в возрасте 16–17 лет, входящие в группу, рекомендованную для вакцинации против COVID-19, могут быть вакцинированы вакциной Pfizer-BioNTech COVID-19 при соответствующем согласии. Детям и подросткам младше 16 лет не разрешено получать вакцину Pfizer-BioNTech COVID-19 в настоящее время.
В настоящее время детям и подросткам младше 18 лет не разрешается получать вакцины Moderna или Janssen от COVID-19.
Консультация пациента
мРНК вакцины COVID-19 (Pfizer-BioNTech и Moderna)
Предварительные данные свидетельствуют о высокой эффективности вакцины в предотвращении COVID-19 после получения двух доз вакцины с мРНК COVID-19 (Pfizer-BioNTech: 95.0% [95% ДИ: 90,3%, 97,6%]; Moderna: 94,1% [95% ДИ: 89,3%, 96,8%]). Пациенты должны быть проинформированы о важности завершения серии двух доз одной и той же вакцины для оптимизации защиты.
Перед вакцинацией медицинские работники должны проконсультировать реципиентов вакцины против мРНК COVID-19 относительно ожидаемых местных (например, боль, отек, эритема в месте инъекции, локализованная подмышечная лимфаденопатия на той же стороне, что и вакцинированная рука) и системных (например, лихорадка, усталость, головная боль, озноб, миалгия, артралгия) поствакцинальные симптомы.В зависимости от вакцины (Pfizer-BioNTech или Moderna), возрастной группы и дозы вакцины примерно 80–89% вакцинированных людей испытывают хотя бы один местный симптом, а 55–83% испытывают хотя бы один системный симптом после вакцинации.
Большинство системных поствакцинальных симптомов имеют выраженность от легкой до умеренной, возникают в течение первых трех дней после вакцинации и исчезают в течение 1–3 дней с момента появления. В целом симптомы более частые и тяжелые после второй дозы и у молодых людей по сравнению с пожилыми людьми (т.например, в возрасте> 55 или ≥65 лет [для вакцин Pfizer-BioNTech или Moderna, соответственно]). Люди с предшествующей инфекцией SARS-CoV-2 могут с большей вероятностью испытывать такие симптомы, как лихорадка, озноб и миалгия, после первой дозы вакцины мРНК COVID-19. Если у людей нет противопоказаний к вакцинации, их следует поощрять к завершению серии, чтобы оптимизировать защиту от COVID-19, даже если у них возникают местные или системные симптомы после первой дозы.
Вакцина против вирусного вектора COVID-19 (Janssen)
По предварительным данным, общая эффективность составляет 66.3% (95% ДИ: 59,9%, 71,8%) против симптоматического, лабораторно подтвержденного COVID-19 через ≥14 дней после вакцинации вакциной Janssen COVID-19. Эффективность вакцины для предотвращения госпитализации, связанной с COVID-19, была высокой; Эффективность вакцины против госпитализации ≥14 дней после вакцинации составила 93,1% (95% ДИ: 71,1%, 98,4%). В группе, получавшей вакцину, через ≥28 дней после вакцинации не было госпитализаций, связанных с COVID-19, и 16 случаев в группе плацебо (эффективность вакцины = 100%; 95% ДИ = 74.3% –100,0%). Эффективность вакцины против смерти от всех причин составила 75,0% (95% ДИ: 33,4%, 90,6%).
Перед вакцинацией поставщики должны проконсультировать реципиентов вакцины Janssen COVID-19 об ожидаемых местных (например, боль, отек, эритема в месте инъекции) и системных (например, лихорадка, усталость, головная боль, озноб, миалгия, артралгия) поствакцинальных симптомах. . Пятьдесят процентов вакцинированных людей испытывают по крайней мере один местный симптом, наиболее частым из которых является боль в месте инъекции, и примерно 55% испытывают по крайней мере один системный симптом после вакцинации.Большинство системных поствакцинальных симптомов слабо выражены и исчезают в течение 1-2 дней после вакцинации. В целом симптомы чаще встречались у молодых людей, чем у пожилых людей (в возрасте ≥60 лет).
Лечение симптомов после вакцинации против COVID-19
Для всех разрешенных в настоящее время вакцин против COVID-19, жаропонижающие или обезболивающие (например, ацетаминофен, нестероидные противовоспалительные препараты) могут приниматься для лечения местных или системных симптомов после вакцинации, если это целесообразно с медицинской точки зрения.Однако рутинное профилактическое введение этих препаратов с целью предотвращения поствакцинальных симптомов в настоящее время не рекомендуется, поскольку информация о влиянии такого применения на ответные реакции антител, вызванных вакциной COVID-19, еще не доступна.
Сообщалось об анафилактических реакциях после вакцинации против COVID-19. Не рекомендуется введение антигистаминных препаратов реципиентам вакцины COVID-19 перед вакцинацией для предотвращения аллергических реакций.Антигистаминные препараты не предотвращают анафилаксию, и их применение может маскировать кожные симптомы, что может привести к задержке диагностики и лечения анафилаксии. См. Раздел о противопоказаниях и мерах предосторожности к вакцинации и временных соображениях по ведению анафилаксии для получения дополнительной информации о лечении анафилаксии.
Рекомендации по профилактике и контролю инфекций доступны для медицинского персонала и пациентов учреждений длительного ухода с системными признаками и симптомами после вакцинации COVID-19.
Противопоказания и меры предосторожности
Противопоказания и меры предосторожности для вакцин против COVID-19 описаны ниже и кратко изложены в Приложении B. Для целей настоящего руководства немедленная аллергическая реакция на вакцину или лекарство определяется как любые связанные с гиперчувствительностью признаки или симптомы, такие как крапивница, ангионевротический отек, респираторный дистресс (например, хрипы, стридор) или анафилаксия, которые возникают в течение четырех часов после введения.
Медицинский персонал или департаменты здравоохранения в Соединенных Штатах могут запросить консультацию в рамках проекта оценки безопасности клинической иммунизации COVIDvax по поводу отдельного пациента, проживающего в Соединенных Штатах, по сложному вопросу о безопасности вакцины COVID-19, который не решается руководством CDC.
Противопоказания
CDC считает противопоказанием к вакцинации против COVID-19 наличие в анамнезе следующих заболеваний:
- Тяжелая аллергическая реакция (например, анафилаксия) после предыдущей дозы или на компонент вакцины COVID-19
- Немедленная аллергическая реакция любой степени тяжести на предыдущую дозу или известная (диагностированная) аллергия на компонент вакцины
Список ингредиентов вакцин против COVID-19 см. В Приложении C.Полиэтиленгликоль (ПЭГ) является ингредиентом обеих вакцин против COVID-19 с мРНК, а полисорбат 80 — ингредиентом вакцины Janssen COVID-19. ПЭГ и полисорбат структурно связаны, и между этими соединениями может возникать перекрестная гиперчувствительность. Людям с противопоказанием к одной из вакцин против мРНК COVID-19 не следует вводить дозы любой из вакцин против мРНК (Pfizer-BioNTech или Moderna). Однако люди с противопоказанием к вакцинации мРНК COVID-19 могут получить вакцину Janssen COVID-19, и наоборот, при условии принятия определенных мер (см. «Меры предосторожности» ниже).В отличие от предыдущих версий руководства, известная аллергия на полисорбат больше не является противопоказанием для вакцинации мРНК; однако известная аллергия на полисорбат является противопоказанием к вакцине Janssen COVID-19 и, следовательно, мерой предосторожности при вакцинации против мРНК COVID-19.
Поставщики медицинских услуг должны попытаться определить, соответствуют ли реакции, о которых сообщают после вакцинации, немедленным аллергическим реакциям по сравнению с другими типами реакций, обычно наблюдаемыми после вакцинации, такими как вазовагальная реакция или поствакцинальные побочные эффекты (Приложение D).Это поможет определить, у каких пациентов есть противопоказания к вакцинации, в том числе ко второй дозе мРНК вакцины COVID-19.
Меры предосторожности
CDC рассматривает историю немедленной аллергической реакции на любую другую вакцину или инъекционную терапию (т. Е. Внутримышечные, внутривенные или подкожные вакцины или методы лечения [за исключением подкожной иммунотерапии от аллергии, т. Е. «Уколы от аллергии»]) в качестве меры предосторожности, но не в качестве меры предосторожности. противопоказание к вакцинации.Люди с реакцией на вакцину или инъекционную терапию, которая содержит несколько компонентов, один из которых является компонентом вакцины, но у которых неизвестно, какой компонент вызвал немедленную аллергическую реакцию, должны соблюдать меры предосторожности при вакцинации.
Люди с противопоказанием к одному типу разрешенных в настоящее время вакцин против COVID-19 (например, мРНК) имеют меры предосторожности по отношению к другому (например, вирусный вектор Янссена). Однако из-за потенциальной перекрестной гиперчувствительности между ингредиентами мРНК и вакцины Janssen COVID-19 следует рассмотреть возможность консультации с аллергологом-иммунологом, чтобы определить, может ли пациент безопасно пройти вакцинацию.Поставщики медицинских услуг и отделы здравоохранения также могут запросить консультацию у проекта COVIDvax по оценке безопасности клинической иммунизации. Вакцинацию этих людей следует проводить только в соответствующих условиях под наблюдением врача, имеющего опыт лечения тяжелых аллергических реакций.
- Люди с противопоказаниями к вакцинации мРНК COVID-19 (в том числе из-за известной аллергии на ПЭГ): можно рассмотреть возможность вакцинации вакциной Janssen COVID-19.Людям, получившим одну дозу вакцины против мРНК COVID-19, но которым противопоказана вторая доза, следует подождать не менее 28 дней после введения дозы вакцины против мРНК, чтобы получить вакцину Janssen COVID-19.
- Люди с противопоказаниями к вакцине Janssen COVID-19 (в том числе из-за известной аллергии на полисорбаты): можно рассмотреть возможность вакцинации против мРНК COVID-19. Следует отметить, что аллергия на полисорбат больше не является противопоказанием к вакцинации против мРНК COVID-19, это мера предосторожности.
Следующие соображения могут быть использованы, чтобы помочь поставщику услуг провести оценку риска вакцинации у лиц с мерами предосторожности к вакцинации:
- Риск заражения SARS-CoV-2 (e.g., из-за проживания в коллективном учреждении, таком как учреждение долгосрочного ухода, род занятий)
- Риск тяжелого заболевания или смерти из-за COVID-19 (например, из-за возраста, сопутствующих заболеваний)
- Неизвестный риск анафилаксии (включая фатальную анафилаксию) после вакцинации против COVID-19 у человека с историей немедленной аллергической реакции на другие вакцины или инъекционные препараты
- Способность пациента пройти вакцинацию в условиях, когда соответствующая медицинская помощь немедленно доступна при анафилаксии.Обратите внимание, что для людей с противопоказанием к другому типу вакцины COVID-19 (например, мРНК-вакцинам) вакцинация другим типом вакцины (например, вирусной векторной вакциной Янссена) должна проводиться только в соответствующих условиях под наблюдением врача. имеет опыт лечения тяжелых аллергических реакций.
Ни противопоказаний, ни мер предосторожности при вакцинации против COVID-19
Аллергические реакции (включая тяжелые аллергические реакции), не связанные с вакцинами (COVID-19 или другими вакцинами) или инъекционными методами лечения, такие как аллергические реакции, связанные с пищевыми продуктами, домашними животными, ядом или окружающей средой, или аллергии на пероральные препараты (включая пероральные препараты). эквиваленты инъекционных препаратов), являются , а не противопоказанием или мерой предосторожности для вакцинации COVID-19.Пробки для флаконов с вакцинами COVID-19 не сделаны из натурального латекса, и нет никаких противопоказаний или мер предосторожности для вакцинации людей с аллергией на латекс. Кроме того, поскольку вакцины COVID-19 не содержат яиц или желатина, у людей с аллергией на эти вещества нет противопоказаний или мер предосторожности к вакцинации.
Сообщалось о местных реакциях с отсроченным началом после вакцинации мРНК у некоторых людей, начиная с нескольких дней до второй недели после первой дозы, и иногда они были довольно значительными.Люди с только отсроченной местной реакцией (например, эритема, уплотнение, зуд) вокруг области инъекции после первой дозы вакцины не имеют противопоказаний или мер предосторожности для второй дозы. Эти люди должны получить вторую дозу с использованием той же вакцины, что и первая доза, с рекомендованным интервалом, предпочтительно в противоположной группе.
Сроки наблюдения после вакцинации
CDC рекомендует следующие периоды наблюдения после вакцинации против COVID-19:
- 30 минут:
- В анамнезе немедленная аллергическая реакция любой степени тяжести на вакцину или инъекционную терапию
- Люди с противопоказанием к другому типу вакцины COVID-19 (например, люди с противопоказанием к вакцинации мРНК COVID-19, которые получают вакцину против вирусного вектора Янссена, должны находиться под наблюдением в течение 30 минут после вакцинации Янссен).
- Анафилаксия по любой причине в анамнезе
- 15 минут: Все остальные
Лечение анафилаксии после вакцинации против COVID-19
В случае возникновения острой анафилактической реакции после введения вакцины COVID-19 должно быть немедленно доступно соответствующее лечение, используемое для купирования немедленных аллергических реакций. Дополнительную информацию о лечении анафилаксии можно найти в разделе «Временные рекомендации по ведению анафилаксии после вакцинации против COVID-19» и лабораторной оценке людей, у которых наблюдается анафилаксия после вакцинации.
Сообщение о побочных эффектах вакцины
О нежелательных явлениях, которые происходят у реципиента после вакцинации против COVID-19, следует сообщать в VAERS. FDA требует, чтобы поставщики вакцинации сообщали о следующих событиях, происходящих после вакцинации COVID-19 в соответствии с EUA:
- Ошибки введения вакцины
- Серьезные нежелательные явления
- Случаи мультисистемного воспалительного синдрома
- Случаи COVID-19, повлекшие за собой госпитализацию или смерть
Приветствуется сообщение о любом другом клинически значимом нежелательном явлении, даже если неизвестно, вызвало ли это событие вакцина.Информацию о том, как отправить отчет в VAERS, можно получить по адресу https: //vaers.hhs.govexternal icon или по телефону 1-800-822-7967.
Кроме того, CDC разработала новый добровольный инструмент для смартфонов — v-safe . Этот инструмент использует текстовые сообщения и веб-опросы, чтобы почти в реальном времени проверять состояние здоровья после вакцинации пациентов от COVID-19. Сообщения на номер v-safe , указывающие на значимое с медицинской точки зрения воздействие на здоровье, включая беременность, отслеживаются колл-центром CDC / v-safe для сбора дополнительной информации для завершения отчета VAERS, если это необходимо.
Лабораторные испытания
Интерпретация результатов теста на SARS-CoV-2 у вакцинированных людей
Предварительное получение вакцины COVID-19 не повлияет на результаты тестов на вирус SARS-CoV-2 (амплификация нуклеиновых кислот или тесты на антиген). Доступные в настоящее время тесты на антитела к SARS-CoV-2 позволяют оценить IgM и / или IgG к одному из двух вирусных белков: спайку или нуклеокапсиду. Поскольку вакцины против COVID-19 сконструированы для кодирования белка-шипа, положительный тест на белок-шип IgM / IgG может указывать на предшествующую инфекцию и / или вакцинацию.Чтобы оценить наличие предшествующей инфекции у человека с историей вакцинации против COVID-19, следует использовать значок тестостерона, который специально оценивает IgM / IgG к белку нуклеокапсида.
Тестирование на антитела в настоящее время не рекомендуется для оценки иммунитета к SARS-CoV-2 после вакцинации COVID-19, поскольку клиническая полезность тестирования после вакцинации не установлена. Тесты на антитела, которые в настоящее время разрешены под значком EUAexternal, имеют переменную чувствительность, специфичность, а также положительную и отрицательную прогностическую ценность и не разрешены для оценки иммунного ответа у вакцинированных людей.Более того, серологические корреляты защиты не установлены, и тестирование антител не оценивает клеточный иммунный ответ, который также может играть роль в опосредованной вакциной защите. Наконец, тестирование антител против нуклеокапсида не выявит иммунных ответов, возникающих в результате вакцинации, но пациенты не всегда могут знать, какой тип теста на антитела был использован. Если тестирование на антитела проводилось после вакцинации, дополнительные дозы той же или другой вакцины COVID-19 не рекомендуются на основании результатов теста на антитела в настоящее время.Если тестирование на антитела было проведено после первой дозы мРНК-вакцины, серию вакцинации следует завершить независимо от результата теста на антитела.
Использование иммунных тестов на туберкулезную инфекцию, таких как туберкулиновая кожная проба и анализ высвобождения гамма-интерферона
Вакцины
COVID-19 не следует откладывать из-за тестирования на туберкулезную инфекцию. Тестирование на туберкулезную инфекцию с помощью одного из иммунных методов, либо туберкулиновой кожной пробы (TST), либо анализа высвобождения интерферона (IGRA), может проводиться до или во время того же контакта с вакцинацией COVID-19.Если тестирование с помощью TST или IGRA нельзя провести одновременно с вакцинацией от COVID-19, эти тесты следует отложить на ≥4 недели после завершения вакцинации COVID-19, но, как правило, их нельзя отменять.
Пациенты с активным туберкулезом или заболеванием, которое оценивается как активное туберкулезное заболевание, могут получить вакцину от COVID-19 (примечание: наличие умеренного или тяжелого острого заболевания является мерой предосторожности при введении всех вакцин). В то время как тест TST или IGRA является частью комплексной оценки заболевания туберкулезом, положительные результаты TST или IGRA не требуются для диагностики активного туберкулеза с внешним признаком.
При рассмотрении туберкулиновой кожной пробы или анализа высвобождения гамма-интерферона:- Ожидается, что TST не повлияет на безопасность или эффективность вакцины COVID-19. IGRA — это анализы крови, поэтому они не влияют на безопасность или эффективность вакцины.
- Ожидается, что надежность положительного результата TST или IGRA после вакцинации COVID-19 будет такой же, как и без вакцинации. Ожидается, что вакцинация против COVID-19 не приведет к ложноположительным результатам теста на туберкулез, который проводится во время или после вакцинации COVID-19.
- Достоверность отрицательного результата TST или IGRA после вакцинации COVID-19 не изучалась.
- TST не является вакциной. Руководство по разделению других вакцин от вакцинации против COVID-19 не менее чем на 2 недели по времени не относится к TST, поскольку TST не является вакциной.
Когда в соответствии с политикой требуется туберкулиновая кожная проба или анализ высвобождения гамма-интерферона:
- TST или IGRA для выполнения административных требований (например, для работы в сфере здравоохранения или для приема на длительный уход) могут быть выполнены до вакцинации COVID-19 или во время того же посещения.Вакцинацию против COVID-19 не следует откладывать из-за тестирования на туберкулез.
- TST или IGRA следует отложить до ≥4 недель после завершения вакцинации COVID-19. Если требования или политики тестирования не могут быть изменены для пандемии COVID-19, чтобы принять эту задержку в тестировании TST или IGRA, следует понимать, что ложноотрицательный TST или IGRA не может быть исключен, и следует рассмотреть возможность повторного отрицательного TST или IGRA. тесты по крайней мере через 4 недели после завершения вакцинации COVID-19.Если бы TST был первоначальным тестом, повышение могло бы быть фактором, если результат повторного теста положительный.
Если для оказания медицинской помощи показана туберкулиновая кожная проба или анализ высвобождения гамма-интерферона:
- Решение о том, следует ли проводить TST или IGRA для медицинской диагностики внешнего признака латентной туберкулезной инфекции (например, во время контактного расследования после контакта с контагиозным туберкулезом), следует отложить на 4 недели после завершения вакцинации COVID-19. по усмотрению ответственного поставщика медицинских услуг и местной противотуберкулезной программы, наблюдающей за расследованием контакта.Медицинские работники и местные программы борьбы с туберкулезом могут не захотеть откладывать тестирование людей с высоким риском прогрессирования туберкулеза. Однако пациентов с отрицательным результатом в этом контексте следует рассматривать для повторного тестирования > через 4 недели после завершения вакцинации против COVID-19.
- Пациенты с внешними симптомами или диагностическими находками, соответствующими активному туберкулезу, должны пройти дальнейшее медицинское обследование — например, с помощью рентгенографии грудной клетки и бактериологического исследования мокроты на предмет Mycobacterium tuberculosis — независимо от результатов TST или IGRA.
Приложение A. Ошибки и отклонения при введении вакцины
Ошибка введения вакцины — это любое предотвратимое событие, которое может вызвать или привести к ненадлежащему использованию вакцины или причинению вреда пациенту. В этом приложении представлены ресурсы для предотвращения и сообщения об ошибках при введении вакцины COVID-19, а также о действиях, которые следует предпринять после возникновения ошибки. Для полноты изложения сюда включены дополнительные сценарии, которые отклоняются от рекомендаций CDC в отношении интервалов вакцинации, но не считаются ошибками введения.Этот документ предназначен для оказания помощи поставщикам медицинских услуг в работе с исключительными ситуациями, в которых уже произошла ошибка или отклонение от вакцинации, и может быть обновлен, когда станет доступна дополнительная информация.
За все ошибки введения вакцины:
Таблица. Промежуточные рекомендации в отношении ошибок и отклонений при введении вакцины COVID-19
Таблица. Промежуточные рекомендации в отношении ошибок и отклонений введения мРНК вакцины COVID-19 Вакцины Тип Ошибка / отклонение администрирования Промежуточная рекомендация Все разрешенные в настоящее время вакцины
(вакцины Pfizer-BioNTech Moderna и Janssen COVID-19)
Участок / маршрут - Неверный сайт (т.е. участок, отличный от дельтовидной мышцы [предпочтительный участок] или переднебоковой участок бедра [альтернативный участок])
- Сделать , а не повторить дозу. * Сообщите получателю о потенциальных местных и системных побочных эффектах.
- Неправильный путь (например, подкожно)
- Сделать , а не повторить дозу. * Сообщите получателю о потенциальных местных и системных побочных эффектах.
Возраст - Если доза была получена в возрасте менее 16 лет, не вводите дополнительную дозу в это время. ∞
- Если возраст от 16 до 17 лет и была случайно введена вакцина, отличная от Pfizer-BioNTech:
- Если вакцина Moderna вводится в качестве первой дозы, можно вводить вакцину Moderna в качестве второй дозы (как использование не по назначению, поскольку вакцина Moderna не разрешена для этой возрастной группы).
- Если вводится вакцина Янссен, повторите дозу , а не с вакциной Pfizer-BioNTech.
Дозировка - Объем введенной дозы выше разрешенной
- Введенный объем дозы ниже разрешенного (например, утечка, отказ оборудования, отток реципиента)
- Если было введено более половины дозы, , а не повторяют дозу. *
- Если было введено менее половины дозы или невозможно оценить пропорцию дозы, немедленно введите разрешенную дозу (без минимального интервала) в противоположной руке. #
Хранение и обращение - Доза, введенная после неправильного хранения и обращения (например, резкое изменение температуры, более чем разрешенное время после первого прокола флакона)
- Обратитесь к производителю за инструкциями.Если производитель предоставляет информацию, подтверждающую необходимость повторения дозы, повторная доза может быть введена немедленно (без минимального интервала) в противоположной руке.
- Доза, введенная после истечения срока годности / истечения срока годности
- Обратитесь к производителю за инструкциями. Если производитель предоставляет информацию, подтверждающую необходимость повторения дозы, повторная доза может быть введена немедленно (без минимального интервала) в противоположной руке.
Совместное администрирование - Доза, вводимая в течение 14 дней до или после другой вакцины (т. Е. Не связанной с COVID-19)
- Не , а не повторная вакцина против COVID-19 * или другие дозы вакцины (ов). Это отклонение от рекомендаций CDC означает, что не требует отчетности VAERS.
- Доза, вводимая в течение 90 дней после введения моноклональных антител или плазмы выздоравливающей для лечения COVID-19
- Нужно ли , а не повторять дозу вакцины против COVID-19.Если человек уже получил одну дозу вакцины против мРНК COVID-19, отложите введение второй дозы на 90 дней после получения терапии антителами. Это отклонение от рекомендаций CDC означает, что не требует отчетности VAERS.
только мРНК вакцины
(Pfizer-BioNTech и Moderna)
Интервалы - Вторая доза вводится менее чем через 17 дней (Pfizer-BioNTech) или менее чем через 24 дня (Moderna) после первой дозы (т.е.е., администрируемый ранее, чем 4-дневный льготный период)
- Вторая доза введена более чем через 42 дня после первой дозы
- Сделать , а не повторить дозу. Это отклонение от рекомендаций CDC означает, что не требует отчетности VAERS.
Смешанная серия - Неправильная мРНК вакцинного продукта COVID-19, введенная для второй дозы в серии из 2 доз
Только Pfizer-BioNTech Разбавитель - Вводится ТОЛЬКО разбавитель (т.е.е., стерильный 0,9% хлорид натрия)
- Сообщите получателю, что вакцина не вводилась. Немедленно введите разрешенную дозу (без минимального интервала) в противоположную руку. #
- Без разбавителя, что приводит к дозе выше разрешенной (т. Е. Введено 0,3 мл неразбавленной вакцины)
- Не применять , а не повторять дозу * † Сообщите получателю о возможных местных и системных побочных эффектах.
- Неправильный тип разбавителя (например, стерильная вода, бактериостатический 0,9% NS)
- Обратитесь к производителю за инструкциями. Если производитель предоставляет информацию, подтверждающую необходимость повторения дозы, повторная доза может быть введена немедленно (без минимального интервала) в противоположной руке.
- Неправильный объем разбавителя (т. Е. Содержимое флакона было разбавлено объемом разбавителя, отличным от 1.8 мл, но все же была введена доза 0,3 мл)
- Для доз, вводимых с объемом разбавителя менее 1,8 мл, проинформируйте получателя о потенциальных местных и системных побочных эффектах. * †
- Для доз, вводимых с объемом разбавителя более 1,8 мл, не повторять , а не . * (Примечание: разведение объемом до 4,0 мл [что превышает емкость флакона] приводит к введению более половины разрешенной дозы.)
Только вакцины Pfizer-BioNTech и Moderna:
* Если ошибочно введенная доза является первой дозой, следует ввести вторую дозу с рекомендуемым интервалом (21 день [Pfizer-BioNTech] или 28 дней [Moderna]) . Если эта доза является второй дозой, серия считается полной и дополнительных доз не требуется.
∞ Не вводите вторую дозу до тех пор, пока человек не станет подходящим для вакцинации (либо по достижении разрешенного возраста, либо если разрешение будет расширено на дополнительные возрастные группы), даже если это приведет к введению второй дозы после рекомендованного интервала. между дозами.
# Если ошибочно введенная доза является первой дозой, вторую дозу следует вводить с рекомендуемым интервалом (21 день [Pfizer-BioNTech] или 28 дней [Moderna]) с даты получения действительной дозы (не дата получения ошибочной дозы).
† Если ошибка введения привела к дозе вакцины, превышающей разрешенную, в общем случае вторая доза может быть введена с рекомендованным интервалом. Однако, если местные или системные побочные эффекты после вакцинации имеют клиническое значение (за пределами ожидаемого профиля побочных эффектов), приводят к серьезным побочным реакциям или продолжаются во время приема второй дозы, решение о введении второй дозы может быть оценено. в индивидуальном порядке.
§Хотя CDC рассматривает смешанную серию в исключительных обстоятельствах, это по-прежнему считается административной ошибкой, требующей отчета VAERS (поскольку смешанная серия не разрешена под внешним значком Разрешения на использование вакцины в чрезвычайных ситуациях).Приложение B: Сортировка людей, поступающих на вакцинацию против COVID-19
† См. Список ингредиентов в Приложении C. Людям с противопоказанием к одной из вакцин против мРНК COVID-19 не следует вводить дозы любой из вакцин против мРНК (Pfizer-BioNTech или Moderna).
* Немедленная аллергическая реакция на вакцину или лекарство определяется как любые связанные с гиперчувствительностью признаки или симптомы, соответствующие крапивнице, ангионевротическому отеку, респираторному расстройству (например, свистящее дыхание, стридор) или анафилаксии, которые возникают в течение четырех часов после введения.
‡ Включает людей с реакцией на вакцину или инъекционную терапию, которая содержит несколько компонентов, один из которых является компонентом вакцины, но у которых неизвестно, какой компонент вызвал немедленную аллергическую реакцию.
# Полиэтиленгликоль (ПЭГ) является ингредиентом обеих вакцин против мРНК COVID-19, а полисорбат 80 является ингредиентом вакцины Janssen COVID-19. ПЭГ и полисорбат структурно связаны, и между этими соединениями может возникать перекрестная гиперчувствительность. Людям с противопоказаниями к вакцинации против мРНК COVID-19 (в том числе из-за известной аллергии на PEG) следует соблюдать меры предосторожности с вакциной Janssen COVID-19. Среди людей, получивших одну дозу мРНК COVID-19, но которым вторая доза противопоказана, можно рассмотреть вопрос о вакцинации вакциной Janssen COVID-19 (вводимой как минимум через 28 дней после введения дозы мРНК COVID-19).Люди с противопоказаниями к вакцине Janssen COVID-19 (в том числе из-за известной аллергии на полисорбат) должны соблюдать меры предосторожности в отношении вакцины против мРНК COVID-19. Людям, соблюдающим эти меры предосторожности, следует рассмотреть возможность обращения к аллергологу-иммунологу. Поставщики медицинских услуг и отделы здравоохранения также могут запросить консультацию у проекта COVIDvax по оценке безопасности клинической иммунизации. Пациентам, соблюдающим эти меры предосторожности, вакцинация должна проводиться только в соответствующих условиях под наблюдением врача, имеющего опыт лечения тяжелых аллергических реакций.Приложение C: Ингредиенты, входящие в состав вакцин против COVID-19
Ниже приводится список ингредиентов вакцин против COVID-19, обозначенных значком Pfizer-BioNTechexternal, значком Modernaexternal и значком Janssenexternal, которые указаны в информации о назначении каждой вакцины.
* Ни одна из вакцин не содержит яиц, желатина, латекса или консервантов.
Примечание. Вакцины Pfizer-BioNTech и Moderna COVID-19 содержат полиэтиленгликоль (ПЭГ). ПЭГ является основным ингредиентом осмотических слабительных и пероральных препаратов кишечника для процедур колоноскопии, неактивным ингредиентом или вспомогательным веществом во многих лекарствах и используется в процессе, называемом «пегилирование», для улучшения терапевтической активности некоторых лекарств (включая некоторые химиотерапевтические препараты).Кроме того, может возникать перекрестная гиперчувствительность между ПЭГ и полисорбатами (включенными в качестве вспомогательного вещества в некоторые вакцины и другие терапевтические агенты). Информацию об активных или неактивных ингредиентах вакцин и лекарств можно найти на вкладыше к упаковке. В качестве ресурса также можно использовать значок «Сводка по вспомогательным веществам вакцины» CDC и внешний значок базы данных DailyMed Национального института здравоохранения.Приложение D. Возможные характеристики аллергических реакций, вазовагальных реакций и побочных эффектов вакцины после вакцинации против COVID-19
У пациентов, у которых наблюдаются поствакцинальные симптомы, важно определить этиологию (включая аллергическую реакцию, вазовагальную реакцию или побочные эффекты вакцины), чтобы определить, может ли человек получить дополнительные дозы вакцины (включая вторую дозу мРНК COVID- 19 вакцина).Следующая таблица признаков и симптомов предназначена для использования в качестве справочного материала, но не может быть исчерпывающей, и у пациентов могут быть не все признаки или симптомы. Медицинские работники должны использовать свое клиническое суждение при оценке пациентов для определения диагноза и лечения.
TicoVac Junior 0,25 мл Суспензия для инъекций в предварительно заполненном шприце — Обзор характеристик продукта (SmPC)
Эта информация предназначена для медицинских работников
TicoVac Junior 0.25 мл Суспензия для инъекций в предварительно заполненном шприце
Вакцина против клещевого энцефалита (цельный вирус, инактивированный)
Одна доза (0,25 мл) содержит:
Вирус клещевого энцефалита 1,2 (штамм Neudörfl) 1,2 мкг
1 , адсорбированный на гидроксиде алюминия, гидратированный (0,17 миллиграмма Al 3+ )
2 продуцируются в клетках фибробластов куриного эмбриона (клетки CEF)
Наполнители с известным эффектом
Полный список вспомогательных веществ см. В разделе 6.1.
Суспензия для инъекций в предварительно заполненном шприце.
После встряхивания вакцина представляет собой беловатую опалесцирующую суспензию.
TicoVac Junior 0,25 мл показан для активной (профилактической) иммунизации детей в возрасте от 1 года до 15 лет против клещевого энцефалита (КЭ).
TicoVac Junior 0,25 мл следует вводить на основании официальных рекомендаций относительно необходимости и сроков вакцинации против клещевого энцефалита.
Позология
График первичной вакцинации
График первичной вакцинации одинаков для всех людей в возрасте от 1 года до 15 лет и состоит из трех доз TicoVac Junior 0.25 мл.
Первую и вторую дозу следует вводить с интервалом от 1 до 3 месяцев.
Если необходимо быстро добиться иммунного ответа, вторую дозу можно ввести через две недели после первой. После первых двух доз следует ожидать достаточной защиты для продолжающегося сезона клещей (см. Раздел 5.1).
Третью дозу следует ввести через 5–12 месяцев после второй вакцинации. Ожидается, что после третьей дозы защита продлится не менее 3 лет.
Для достижения иммунитета до начала сезонной активности клещей, то есть весной, первую и вторую дозу предпочтительно давать в зимние месяцы. График вакцинации в идеале должен быть дополнен третьей вакцинацией в течение того же сезона клещей или, по крайней мере, до начала следующего сезона клещей.
Базовая иммунизация
Доза
Обычный график
График быстрой иммунизации
1 st доза
0.25 мл
Дата избрания
Дата избрания
2 nd доза
0,25 мл
От 1 до 3 месяцев после вакцинации 1 st
14 дней после вакцинации 1 st
3 rd доза
0.25 мл
От 5 до 12 месяцев после вакцинации 2 nd
От 5 до 12 месяцев после вакцинации 2 nd
Бустерные дозы
Первую бустерную дозу следует ввести через 3 года после третьей дозы (см. Раздел 5.1).
Последовательные бустерные дозы следует вводить каждые 5 лет после последней бустерной дозы.
Бустерная доза
Доза
Сроки
1 st усилитель
0.25 мл
3 года после вакцинации 3 от
Последовательные бустерные дозы
0,25 мл
каждые 5 лет
Увеличение интервала между любыми дозами (график первичной вакцинации и бустерные дозы) может оставить субъектов с недостаточной защитой от инфекции (см. Раздел 5.1).
Однако в случае прерванного графика вакцинации, по крайней мере, двух предыдущих прививок, одной догоняющей дозы достаточно для продолжения графика вакцинации (см.1).
Данных о наверстывающей дозе у детей младше 6 лет нет (см. Раздел 5.1).
Дети с ослабленной иммунной системой (в том числе, получающие иммуносупрессивную терапию)
Нет конкретных клинических данных, на основе которых можно было бы основывать рекомендации по дозировке. Однако можно рассмотреть возможность определения концентрации антител через четыре недели после второй дозы и введения дополнительной дозы, если в это время нет доказательств сероконверсии.То же самое относится к любой из следующих доз.
Способ применения
Вакцину следует вводить внутримышечно в предплечье (дельтовидную мышцу).
Детям в возрасте до 18 месяцев или в зависимости от их развития и состояния питания вакцина вводится в мышцу бедра (латеральная широкая мышца бедра).
Только в исключительных случаях (пациентам с нарушением свертываемости крови или пациентам, получающим профилактическую антикоагулянтную терапию) вакцину можно вводить подкожно (см. Разделы 4.4 и 4.8).
Необходимо соблюдать осторожность, чтобы избежать случайного внутрисосудистого введения (см. Раздел 4.4).
Повышенная чувствительность к активному веществу, любому из вспомогательных веществ, перечисленных в разделе 6.1, или остаткам продукции (формальдегид, неомицин, гентамицин, сульфат протамина). Следует рассмотреть возможность перекрестной аллергии на аминогликозиды, отличные от неомицина и гентамицина.
Тяжелая гиперчувствительность к белкам яиц и цыплят (анафилактическая реакция после перорального приема яичного белка) может вызывать тяжелые аллергические реакции у сенсибилизированных лиц (см. Также раздел 4.4).
Вакцинацию против клещевого энцефалита следует отложить, если человек страдает умеренным или тяжелым острым заболеванием (с лихорадкой или без нее).
Как и в случае со всеми вакцинами, которые вводятся путем инъекции, в случае редкого анафилактического события после введения вакцины всегда должны быть доступны соответствующее неотложное лечение и наблюдение.
Нетяжелая аллергия на яичный белок обычно не является противопоказанием для вакцинации TicoVac Junior 0.25 мл. Тем не менее, таких людей следует вакцинировать только под надлежащим наблюдением, и должны быть доступны средства для экстренной помощи при реакциях гиперчувствительности.
Уровни калия и натрия составляют менее 1 ммоль на дозу, т. Е. По существу «не содержат калия и натрия».
Следует избегать внутрисосудистого введения, так как это может привести к тяжелым реакциям, включая реакции гиперчувствительности с шоком.
Рекомендуемый способ введения — внутримышечный.Однако это может не подходить для субъектов с нарушением свертываемости крови или субъектов, получающих профилактическую антикоагулянтную терапию. Ограниченные данные у здоровых взрослых предполагают сопоставимый иммунный ответ на подкожную ревакцинацию по сравнению с внутримышечной ревакцинацией. Однако подкожное введение может привести к повышенному риску местных побочных реакций. Данных о детях / подростках нет. Кроме того, отсутствуют данные о первичной иммунизации подкожным путем.
Лихорадка может возникнуть у детей после первой иммунизации, особенно у самых маленьких (см. Раздел 4.8). Обычно температура спадает в течение 24 часов. Показатели лихорадки, зарегистрированные после второй вакцинации, обычно ниже, чем показатели лихорадки после первой вакцинации. У детей, у которых в анамнезе были лихорадочные судороги или высокая температура после вакцинации, можно рассмотреть возможность применения жаропонижающих средств для профилактики или лечения.
Защитный иммунный ответ не может быть вызван у лиц, проходящих иммуносупрессивную терапию.
Если серологическое тестирование считается необходимым для определения потребности в последовательных дозах, анализы следует проводить в опытной квалифицированной лаборатории. Это связано с тем, что перекрестная реактивность с уже существующими антителами из-за естественного воздействия или предыдущей вакцинации против других флавивирусов (например, японского энцефалита, желтой лихорадки, вируса денге) может давать ложноположительные результаты.
В случае известного или предполагаемого аутоиммунного заболевания у предполагаемого реципиента риск заражения клещевым энцефалитом необходимо сопоставить с риском того, что TicoVac Junior 0.25 мл могут отрицательно повлиять на течение аутоиммунного заболевания.
Следует соблюдать осторожность при рассмотрении вопроса о необходимости вакцинации детей с ранее существовавшими церебральными нарушениями, такими как активные демиелинизирующие расстройства или плохо контролируемая эпилепсия.
Нет данных о постконтактной профилактике с помощью TicoVac Junior 0,25 мл.
Как и все вакцины, 0,25 мл TicoVac Junior не может полностью защитить всех вакцинированных от инфекции, которую он предназначен для предотвращения.Подробную информацию о применении продукта людям с ослабленной иммунной системой и лицам, проходящим иммуносупрессивную терапию, см. В разделе 4.2.
Укусы клещей могут передавать инфекции, отличные от клещевого энцефалита, включая определенные патогены, которые иногда могут вызывать клиническую картину, напоминающую клещевой энцефалит. Вакцины против клещевого энцефалита не обеспечивают защиты от инфекции Borrelia. Следовательно, появление клинических признаков и симптомов возможных инфекций клещевого энцефалита у вакцинированного должно быть тщательно исследовано на предмет возможных альтернативных причин.
Исследования взаимодействия с другими вакцинами или лекарственными средствами не проводились. Введение других вакцин одновременно с TicoVac Junior 0,25 мл следует проводить только в соответствии с официальными рекомендациями. Если одновременно вводятся другие инъекционные вакцины, введение следует проводить в отдельные участки и, предпочтительно, в отдельные конечности.
Беременность
Нет данных об использовании TicoVac Junior 0.25 мл беременным.
Кормление грудью
Неизвестно, выделяется ли TicoVac Junior 0,25 мл с грудным молоком.
Таким образом, TicoVac Junior 0,25 мл следует вводить только во время беременности и кормящим женщинам, когда это считается срочным для достижения защиты от инфекции клещевого энцефалита и после тщательного рассмотрения соотношения риска и пользы.
TicoVac Junior 0,25 мл вряд ли повлияет на моторику ребенка (т.е.g., играя на улице или катаясь на велосипеде) или способность человека водить машину и пользоваться механизмами. Однако следует учитывать, что возможно нарушение зрения или головокружение.
Вычисленные частоты основаны на объединенном анализе побочных реакций, зарегистрированных после вакцинации 1 st (3088 субъектов) из 8 клинических исследований, проведенных с использованием 0,25 мл (1,2 мкг) препарата TicoVac Junior у субъектов в возрасте 1-15 лет. Частота системных побочных реакций, наблюдаемых после вакцинации 2 -й и 3 -й , была ниже, чем после вакцинации 1 -й .Сравнимые показатели реакций в месте инъекции наблюдаются после первой, второй и третьей вакцинации.
Следующие другие нежелательные эффекты, перечисленные в этом разделе, приведены в соответствии с рекомендуемой частотой:
Побочные реакции по результатам клинических испытаний
Класс системного органа
Частота
Очень часто
(≥1 / 10)
Общий
(от ≥1 / 100 до <1/10)
Необычный
(от ≥1 / 1000 до <1/100)
Редкий
(от ≥1 / 10 000 до <1/1 000)
Нарушения со стороны крови и лимфатической системы
Лимфаденопатия
Нарушения обмена веществ и питания
Пониженный аппетит
Психиатрические расстройства
Беспокойство 1 ,
Расстройство сна
Нарушения нервной системы
Головная боль
Сенсорные аномалии,
Головокружение
Нарушения уха и лабиринта
Головокружение
Желудочно-кишечные расстройства
тошнота,
рвота
Боль в животе
Диарея,
Диспепсия
Заболевания кожи и подкожной клетчатки
Крапивница
Нарушения со стороны скелетно-мышечной и соединительной ткани
Миалгия
Артралгия
Общие расстройства и нарушения в месте введения
Реакции в месте инъекции 2 e.г.,
Боль в месте укола
Пирексия 3 ,
Усталость, недомогание 4
Реакции в месте инъекции, такие как
• Набухание
• Вступление
• Эритема
Озноб
Зуд в месте инъекции
1 Частота рассчитана на основе данных детей в возрасте 1-5 лет
2 Субъект мог испытать более одного события.
3 Лихорадка чаще возникала у детей младшего возраста, чем у детей старшего возраста (т. Е. От очень часто до общего, соответственно). Уровень лихорадки после второй и третьей прививок обычно ниже, чем после первой вакцинации.
4 Частота рассчитана на основе данных о детях в возрасте от 6 до 15 лет.
Температура измерялась ректально у детей в возрасте до 3 лет и перорально у детей в возрасте 3 лет и старше.Анализ включает любую лихорадку, временно связанную с вакцинацией, независимо от того, является ли она причинно-следственной.
Лихорадка зависит от возраста и уменьшается с количеством прививок.
В исследовании безопасности и исследованиях по подбору дозы частота лихорадки, наблюдаемая после первой вакцинации, была следующей:
дети от 1 года до 2 лет (n = 262): легкая лихорадка (38–39 ° C) у 27,9%; умеренная лихорадка (39,1-40,0 ° С) у 3,4%; нет сильной лихорадки (> 40 ° C). Дети от 3 до 15 лет (n = 2519): умеренная лихорадка у 6.8%; умеренная температура в 0,6%; нет сильной лихорадки (> 40 ° C).
Показатели лихорадки, зарегистрированные после второй вакцинации, обычно ниже, чем показатели лихорадки после первой вакцинации: 15,6% (41/263) у детей в возрасте от 1 до 2 лет и 1,9% (49/2522) у детей от 3 до 15 лет. дети.
Побочные реакции при постмаркетинговом надзоре
Следующие дополнительные побочные реакции были зарегистрированы в постмаркетинговом опыте.
Класс системного органа
Частота *
Редко (от ≥1 / 10,000 до <1/1000)
Нарушения иммунной системы
Анафилактическая реакция, гиперчувствительность
Нарушения нервной системы
Энцефалит, судороги (в том числе фебрильные), менингизм, полинейропатия, двигательная дисфункция (гемипарез / гемиплегия парез лица, паралич / парез, неврит), синдром Гийена-Барре
Заболевания глаз
Нарушение зрения, светобоязнь, боль в глазах
Нарушения уха и лабиринта
Тиннитус
Заболевания органов дыхания, грудной клетки и средостения
Одышка
Заболевания кожи и подкожной клетчатки
Сыпь (эритематозная, пятнисто-папулезная, везикулярная), эритема, кожный зуд, гипергидроз
Нарушения со стороны скелетно-мышечной и соединительной ткани
Боль в шее, костно-мышечной жесткости (включая ригидность затылочных мышц), боль в конечности
Общие расстройства и нарушения в месте введения
Нарушение походки, гриппоподобное заболевание, астения, отек
* Верхний предел 95% доверительного интервала частоты событий рассчитывается как 3 / n, где n представляет количество субъектов, включенных во все клинические испытания с TicoVac Junior 0.25 мл. Следовательно, рассчитанная частота «редко» представляет собой теоретическую максимальную частоту для этих событий
В небольшом сравнительном исследовании иммунного ответа после внутримышечного и подкожного введения TicoVac у здоровых взрослых, подкожный путь привел к более высокому профилю локальной реактогенности, особенно у женщин. Нет данных о детях.
Сообщение о предполагаемых побочных реакциях
Важно сообщать о предполагаемых побочных реакциях после получения разрешения на лекарственный препарат.Это позволяет непрерывно контролировать соотношение польза / риск лекарственного средства. Медицинских работников просят сообщать о любых предполагаемых побочных реакциях через схему желтых карточек по адресу: www.mhra.gov.uk/yellowcard или искать желтые карточки MHRA в Google Play или Apple App Store.
Есть сообщения о том, что дети получали препарат для взрослых. Вполне возможно, что в таких случаях повышается риск побочных реакций.
Фармакотерапевтическая группа: вакцины против энцефалита, код АТХ: J07 BA01
Фармакодинамический эффект продукта заключается в индукции достаточно высокой концентрации антител против TBE для обеспечения защиты от вируса TBE.
Уровень защиты вакцины против клещевого энцефалита предыдущего поколения и нынешней вакцины был определен в ходе непрерывного эпиднадзора, который проводился среди всего населения Австрии с 1984 года. В этом эпиднадзоре уровень защиты у детей выше 98% после завершения графика первичной вакцинации (3 доз) был рассчитан для периода с 1994 по 2003 год. На основании последующего эпиднадзора, проведенного среди всего населения Австрии в период с 2000 по 2006 год, был рассчитан уровень защиты 99% без статистически значимой разницы между возрастными группами у регулярно вакцинированных лиц. .
Уровень защиты по крайней мере такой же высокий после первых двух вакцинаций, после обычной и быстрой вакцинации, то есть до завершения базовой схемы вакцинации третьей вакцинацией.
У тех, у кого есть записи о нерегулярной вакцинации, уровень защиты значительно ниже.
В клинических исследованиях с TicoVac Junior 0,25 мл серопозитивность определялась как значение ELISA> 126 VIE U / мл или титры NT ≥10. Суммарные показатели серопозитивности, определенные с помощью ELISA и NT через 21 день после второй и третьей вакцинации по стандартному графику, представлены в Таблице 1 и Таблице 2.
Таблица 1.
Обычный график иммунизации, объединенные уровни серопозитивности 1 по данным ELISA и NT
Субъекты в возрасте 1-5 лет
ELISA 2
NT 2
Доза
2 nd
3 рд
2 nd
3 рд
Уровень серопозитивности 1 ,%
(нет данных)
99.4
(501/504)
100,0
(493/493)
98,5
(196/199)
99,5
(193/194)
Таблица 2.
Обычный график иммунизации, объединенные уровни серопозитивности 1 по данным ELISA и NT
Субъекты 6-15 лет
ELISA 2
NT 2
Доза
2 nd
3 рд
2 nd
3 рд
Уровень серопозитивности 1 ,%
(нет данных)
97.1
(496/511)
99,8
(505/506)
95,5
(274/287)
99,7
(289/290)
1 — оценивается через 21 день после каждой дозы
2 — отсечение серопозитивности: ELISA> 126 VIE U / мл; NT ≥ 1:10
Наивысшие показатели серопозитивности, определенные с помощью ELISA и NT, были достигнуты при введении третьей дозы.Таким образом, для достижения защитных уровней антител почти у всех реципиентов необходимо завершить схему первичной вакцинации из трех доз.
Через 5 месяцев после второй вакцинации более 97% детей в возрасте 1–5 лет и более 93% детей в возрасте 6–15 лет показали серопозитивные уровни антител против клещевого энцефалита как в ELISA, так и в NT.
Результаты последующего исследования, в котором изучалась устойчивость антител против клещевого энцефалита, подтверждают необходимость проведения первой бустерной вакцинации не позднее, чем через три года после первичной иммунизации.Анализ сероперсистентности до 58 месяцев после первой ревакцинации показал высокие показатели серопозитивности в NT для всех возрастных подгрупп: 96,6% у детей в возрасте 1-2 лет, 100% у детей в возрасте 3-6 лет и 98,1% у детей 7- летнего возраста. 15 лет, поддерживая 5-летний интервал ревакцинации с момента первой ревакцинации.
Вакцинация TicoVac индуцирует статистически эквивалентные титры нейтрализующих антител против вируса клещевого энцефалита против европейских, сибирских и дальневосточных штаммов вируса клещевого энцефалита. В опубликованном клиническом исследовании значительные перекрестно нейтрализующие антитела были также индуцированы против вируса омской геморрагической лихорадки, однако титры были ниже, чем против подтипов вируса клещевого энцефалита.
Исследование устойчивости иммунной памяти у лиц в возрасте от 6 лет и старше, интервалы вакцинации которых превышали рекомендованные (≤12 лет), показало, что однократная наверстывающая вакцинация TicoVac могла вызвать анамнестический ответ антител у 99% детей по данным ELISA. Нет данных об ответе антител, измеренном с помощью NT.
Доклинические данные, основанные на традиционных исследованиях фармакологической безопасности, не показывают особой опасности для человека.
Альбумин человека
Натрия хлорид
Дигидрат динатрийфосфата
Калия дигидрофосфат
Вода для инъекций
Сахароза
Гидроксид алюминия гидратированный.
При отсутствии исследований совместимости эту вакцину нельзя смешивать с другими лекарственными средствами.
Хранить в холодильнике (2-8 ° C). Храните шприц во внешней картонной упаковке для защиты от света.
Не замораживать.
0,25 мл суспензии в предварительно заполненном шприце (стекло типа I) с пробкой плунжера (галогенбутилкаучук), без прикрепленной иглы. Размеры упаковки 1, 10, 20 и 100. В упаковке может быть 0 игл или 1 игла. Иглы стерильные и предназначены только для одноразового использования. Не все размеры упаковки могут быть проданы.
Каждый предварительно заполненный шприц упакован в блистер. Отверстие в блистерной упаковке предназначено для уравновешивания влажности во время рекомендуемого разогрева перед введением вакцины.Откройте блистер, сняв крышку, чтобы вынуть шприц. Не продавливайте шприц через блистер.
Информацию о подкожном введении см. В разделе 6.6.
Перед введением вакцина должна достичь комнатной температуры. Хорошо встряхните перед введением, чтобы тщательно перемешать суспензию вакцины. После встряхивания TicoVac Junior 0,25 мл представляет собой не совсем белую, опалесцирующую гомогенную суспензию. Перед введением вакцину следует визуально осмотреть на предмет наличия посторонних частиц и / или изменений внешнего вида.В случае обнаружения любого из них откажитесь от вакцины.
После снятия колпачка шприца немедленно присоедините иглу и снимите колпачок с иглы перед введением. После того, как игла будет прикреплена, вакцину нужно ввести немедленно. В исключительных случаях подкожного введения следует использовать соответствующую иглу.
Любой неиспользованный продукт или отходы следует утилизировать в соответствии с местными требованиями.
Врач должен задокументировать введение вакцины и записать номер партии.К каждому предварительно загруженному шприцу прикреплена съемная этикетка с документацией.
Pfizer Limited
Ramsgate Road
Сэндвич
Кент
CT13 9NJ
Соединенное Королевство
Дата первого разрешения: 3 марта 2006 г.
Дата последнего обновления: 18 января 2007 г.
09/2018
Ссылка: TI Junior 6_0
Почему вакцинация безопасна и важна
Вакцины — самый эффективный способ профилактики инфекционных заболеваний.На этой странице объясняется, как действуют вакцины, что они содержат, а также объясняются наиболее распространенные побочные эффекты.
Видео: вакцины — безопасны ли они для моего ребенка?
В этом видео терапевт успокаивает родителей о вакцинации ее ребенка.
Последний раз просмотр СМИ: 29 июля 2019 г.
Срок сдачи обзора СМИ: 29 июля 2022 г.Важный
Имейте в виду, что истории против прививок распространяются в Интернете через социальные сети.
Они могут не основываться на научных данных и могут подвергнуть вашего ребенка риску серьезного заболевания.
Что нужно знать о вакцинах
Вакцины:
Делать
защитит вас и вашего ребенка от многих серьезных и потенциально смертельных заболеваний
защитите других людей в вашем сообществе, помогая остановить распространение болезней среди людей, которые не могут получить вакцины
- Перед внедрением
проходят тщательные испытания на безопасность — они также постоянно отслеживаются на предмет побочных эффектов после внедрения
иногда вызывает легкие побочные эффекты, которые не продлятся долго — некоторые дети могут чувствовать себя плохо и болеть рука в течение 2 или 3 дней
уменьшить или даже избавиться от некоторых болезней — если вакцинировано достаточное количество людей
Не
не вызывают аутизм — исследования не нашли доказательств связи между вакциной MMR и аутизмом
не перегружает и не ослабляет иммунную систему — детям безопасно вводить несколько вакцин за один раз, и это снижает количество необходимых им инъекций.
не вызывают аллергии или каких-либо других состояний — все текущие данные говорят нам, что вакцинация безопаснее, чем не вакцинация
не содержат ртути (тиомерсал)
не содержат ингредиентов, которые могут причинить вред в таких небольших количествах, но обратитесь к врачу, если у вас есть какие-либо известные аллергии, такие как яйца или желатин.
Почему вакцины важны
Вакцинация — это самое важное, что мы можем сделать, чтобы защитить себя и своих детей от болезней.Они предотвращают до 3 миллионов смертей во всем мире ежегодно.
С тех пор, как в Великобритании были введены вакцины, такие болезни, как оспа, полиомиелит и столбняк, которые раньше убивали или калечили миллионы людей, либо исчезли, либо наблюдаются очень редко.
Число других болезней, таких как корь и дифтерия, снизилось на 99,9% с момента внедрения их вакцин.
Однако, если люди перестанут получать вакцины, инфекционные заболевания могут быстро снова распространиться.
Информация:
Всемирная организация здравоохранения (ВОЗ) недавно включила нерешительность в отношении вакцинации как одну из 10 самых серьезных угроз глобальному здоровью.
Неуверенность в вакцинации — это когда люди, имеющие доступ к вакцинам, откладывают вакцинацию или отказываются от нее.
Корь и эпидемический паротит в Англии
Корь и эпидемический паротит снова начинают появляться в Англии, хотя вакцина MMR безопасна и защищает от обеих болезней.
Заболеваемость корью и эпидемическим паротитом за последние годы почти удвоилась:
Случаи кори и эпидемического паротита в Англии
Таблица, показывающая, сколько случаев кори и паротита было в Англии в 2016 и 2018 годах Год Корь Свинка 2016 530 573 2018 970 1061 Это серьезно, поскольку корь может привести к опасным для жизни осложнениям, таким как менингит, а свинка может вызвать потерю слуха.
Важный
Если 95% детей получат вакцину MMR, от кори можно избавиться.
Однако корь, эпидемический паротит и краснуха могут быстро снова распространиться, если вакцинировано менее 90% людей.
Как работают вакцины
Вакцины учат вашу иммунную систему создавать антитела, которые защищают вас от болезней.
Для вашей иммунной системы гораздо безопаснее научиться этому с помощью вакцинации, чем путем выявления болезней и их лечения.
Когда ваша иммунная система знает, как бороться с болезнью, она часто может защищать вас в течение многих лет.
Коллективный иммунитет
Наличие вакцины также приносит пользу всему вашему сообществу благодаря «коллективному иммунитету».
Если вакцинировано достаточное количество людей, болезнь труднее передать тем людям, которые не могут получить вакцины. Например, люди, которые болеют или имеют ослабленную иммунную систему.
Информация:
Узнайте больше о коллективном иммунитете и о том, кого он защищает, на веб-сайте Проекта знаний о вакцинах Оксфордского университета.
Почему вакцины безопасны
Все вакцины проходят тщательное тестирование, чтобы убедиться, что они не причинят вреда вам или вашему ребенку.
Часто вакцине требуется много лет, чтобы пройти испытания и тесты для утверждения.
После того, как вакцина используется в Великобритании, она также проверяется на предмет любых редких побочных эффектов Агентством по регулированию лекарственных средств и товаров медицинского назначения (MHRA).
Любой человек может сообщить в MHRA о предполагаемом побочном эффекте вакцинации через схему желтых карточек.
Информация:
Прочтите все о том, как вакцины лицензируются, тестируются и контролируются на веб-сайте Проекта знаний о вакцинах Оксфордского университета.
Побочные эффекты вакцинации
Большинство побочных эффектов вакцинации мягкие и длятся недолго.
Наиболее частые побочные эффекты вакцинации включают:
- область, в которую входит игла, выглядит красной, опухшей и ощущается легкая болезненность в течение 2–3 дней
- младенцы или маленькие дети чувствуют себя немного плохо или у них повышается температура. на 1 или 2 дня
Некоторые дети также могут плакать и расстраиваться сразу после инъекции.Это нормально, и они должны почувствовать себя лучше после объятий.
Аллергические реакции
Серьезные аллергические реакции на вакцинацию возникают редко. Если это действительно происходит, обычно это происходит в течение нескольких минут.
Человек, который вакцинирует вас или вашего ребенка, будет обучен справляться с аллергическими реакциями и немедленно лечить их. При своевременном лечении вы или ваш ребенок выздоровеете.
Прочтите советы по вакцинации для родителей, в том числе, чего ожидать после вакцинации.
Несрочный совет: поговорите со своим терапевтом или медсестрой, если:
- вы беспокоитесь о том, что вы или ваш ребенок будете вакцинированы
- вы не уверены, можете ли вы или ваш ребенок получить вакцину
Вы также можете задать патронажной сестре любые вопросы о вакцинах.
Информация:
Обновление коронавируса: как связаться с GP
По-прежнему важно получить помощь от терапевта, если она вам нужна.Чтобы связаться с вашим терапевтом:
- посетите их веб-сайт
- используйте приложение NHS
- позвоните им
Узнайте об использовании NHS во время коронавируса
Что входит в состав вакцины?
Большинство людей не беспокоятся об ингредиентах вакцины и знают, что они безопасны.
Основным ингредиентом любой вакцины является небольшое количество бактерий, вирусов или токсинов, которые сначала ослабляются или уничтожаются в лаборатории.
Это означает, что здоровые люди не заразятся болезнью от вакцины.Вот почему вы можете видеть, что вакцины называются «живыми» или «убитыми» вакцинами.
В чем разница между живой и убитой вакциной?
Сравнение живых и убитых вакцин
Таблица, показывающая различия между живыми и убитыми вакцинами Живые (ослабленные) вакцины Убитые (уничтоженные) вакцины Содержат ослабленные вирусы или бактерии Содержат уничтоженные вирусы или бактерии Нельзя давать людям с ослабленной иммунной системой Можно давать людям с ослабленной иммунной системой Обеспечивает длительную защиту Часто требуется несколько доз или бустерная вакцина для полной защиты Другие ингредиенты вакцины
Вакцины иногда содержат другие ингредиенты, которые делают вакцину более безопасной и более эффективной.
Нет никаких доказательств того, что какой-либо из этих ингредиентов причиняет вред при использовании в таких небольших количествах.
Алюминий (адъювант)
Это безопасно?
Адъюванты добавляются к вакцинам в очень малых количествах, которые оказались безопасными. Они могут вызвать незначительные реакции, такие как небольшая временная шишка или покраснение в месте инъекции.
Мы постоянно контактируем с алюминием. В естественных условиях он содержится в очень небольших количествах:
- почти во всех продуктах питания
- питьевой воде
- грудном молоке
- детском молоке
Он также используется в лекарствах, таких как антациды, и в упаковке пищевых продуктов.
Хотя небольшие количества алюминия из этих повседневных источников могут накапливаться в организме, они не считаются вредными для нашего здоровья. Наши тела не используют алюминий, и он постепенно удаляется с нашей мочой.
Нет никаких доказательств того, что уровни алюминия, с которыми мы сталкиваемся каждый день, увеличивают риск таких состояний, как деменция или аутизм.
Количество алюминия, используемого в убитых вакцинах, очень и очень мало. Вакцины, содержащие адъювант на основе алюминия, не имели вредных эффектов.
Что это?
Алюминий — очень распространенный металл, который безопасно используется в вакцинах более 70 лет.
Большинство убитых вакцин содержат очень небольшое количество адъюванта на основе алюминия, чтобы:
- помочь повысить наш иммунный ответ
- сделать вакцину более эффективной и долговечной
- уменьшить количество антигена, необходимого в вакцине
- иногда уменьшают количество доз, которые необходимо ввести
Скваленовое масло (адъювант)
Это безопасно?
Адъюванты добавляются к вакцинам в очень малых количествах, которые оказались безопасными.
Они могут вызвать незначительные реакции, такие как небольшая временная опухоль или покраснение в месте инъекции.
Что это?
Скваленовое масло — это адъювант, добавляемый к трехвалентной вакцине против гриппа для взрослых в возрасте 65 лет и старше.
Он производится из рыбьего жира и подвергается высокой очистке перед использованием в вакцине против гриппа.
Адъюванты добавляются к некоторым вакцинам, чтобы:
- помочь повысить наш иммунный ответ
- сделать вакцину более эффективной и долговечной
- уменьшить количество антигена, необходимого в вакцине
- иногда уменьшить количество доз, которые нужно отдать
Желатин свиной
Это безопасно?
Было небольшое количество аллергических реакций на вакцины, содержащие желатин.Если у вас аллергия на желатин, сначала обратитесь к врачу.
Некоторые религиозные группы, такие как мусульмане и евреи, могут быть обеспокоены использованием вакцин, содержащих желатин, от свиней. Но многие лидеры религиозных групп заявили, что использование желатина в вакцинах приемлемо и не нарушает никаких религиозных правил.
Прочтите эту брошюру NHS о вакцинах и свином желатине
Что это?
Желатин, полученный от свиней, используется в качестве стабилизатора в некоторых вакцинах для:
- защиты вакцин от воздействия тепла или сублимационной сушки
- помогает поддерживать срок годности вакцины
Единственные вакцины, содержащие желатин в календаре плановой вакцинации Великобритании:
- вакцина против опоясывающего лишая
- детская назальная вакцина против гриппа
- 1 из 2 типов вакцины MMR
Сывороточный альбумин человека и рекомбинантный альбумин
Они в безопасности?
Да, они считаются безопасными.Сывороточный альбумин человека, используемый в вакцинах, поступает от проверенных доноров крови. Производственный процесс гарантирует отсутствие риска передачи каких-либо заболеваний.
Рекомбинантный альбумин не содержит продуктов человеческого или животного происхождения.
Какие они?
Сывороточный альбумин человека — это вещество из крови человека. Он используется для стабилизации вакцины против ветряной оспы под названием Varilix и поддержания ее качества во время хранения.
Рекомбинантный альбумин продуцируется клетками, такими как дрожжевые клетки, в которые встроен ген человеческого альбумина.
После этого клетки могут вырабатывать большие количества сывороточного альбумина человека без необходимости извлекать его из крови человека.
Рекомбинантный альбумин можно использовать в очень малых количествах в качестве стабилизатора в одной из вакцин MMR, используемых в Великобритании (MMRVaxPro).
Яичный белок
Это безопасно?
Дети и взрослые с тяжелой аллергией на яйца могут безопасно получить вакцину MMR.
Детям и взрослым с аллергией на яйца рекомендуется иметь:
- инактивированную вакцину против гриппа без яиц
- вакцину с очень низким содержанием яичного белка (овальбумина)
Живую назальную вакцину против гриппа в виде спрея у детей очень низкое содержание яичного белка.Его смело можно давать детям с аллергией на яйца.
Детям и взрослым, у которых ранее была очень тяжелая аллергическая реакция на яйца, можно посоветовать сделать прививку от гриппа в больнице.
Что это?
В стандартном календаре Великобритании есть 2 вакцины, которые содержат небольшое количество яичного белка:
- вакцина против гриппа, выращиваемая на куриных яйцах. Она потенциально может вызвать аллергическую реакцию у людей с аллергией на яйца.
- вакцина MMR, выращиваемая на клетках куриных эмбрионов, что отличается от куриных яиц.Это означает, что он не вызывает аллергической реакции
Формальдегид
Это безопасно?
Формальдегид может быть обнаружен в нашем кровотоке в естественных условиях в количествах, намного превышающих уровни, которым мы подвергаемся в вакцинах.
Хотя формальдегид в высоких концентрациях может быть вредным, небольшие количества, содержащиеся в вакцинах, не вызывают опасений для здоровья.
Что это?
Формальдегид — это химическое вещество, которое также используется в производстве убитых вакцин.Он используется очень рано в производственном процессе, чтобы убить или инактивировать токсины от бактерий или вирусов.
После того, как антигены инактивированы, формальдегид разводится. Возможно, что в окончательной вакцине останутся следовые количества.
Антибиотики
Они в безопасности?
Если вы знаете, что у вас аллергия на неомицин или любой другой антибиотик, поговорите со своим врачом или медсестрой перед вакцинацией.
Антибиотики, вызывающие аллергические реакции, такие как пенициллин, обычно не используются в вакцинах.
Но крошечные количества антибиотика под названием неомицин, который способен вызывать аллергическую реакцию, находятся в:
- вакцине MMR
- вакцине 6-в-1
- четырехвалентной инактивированной вакцине против гриппа
- 4-в- 1 ревакцинация для дошкольников Repevax
- вакцина против опоясывающего лишая
Что это такое?
К некоторым вакцинам добавляют антибиотики, чтобы предотвратить рост бактерий во время производства и хранения вакцины.
 Разовая доза составляет 0,25 мл.
Разовая доза составляет 0,25 мл.

 Е. Вакцины могут быть введены в этих условиях)
Е. Вакцины могут быть введены в этих условиях)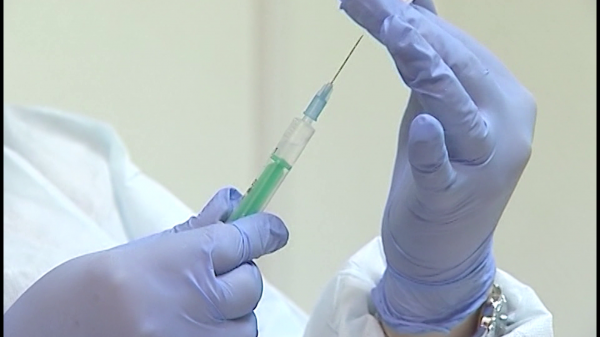 DOI: 10.1093 / ije / 17.2.448
DOI: 10.1093 / ije / 17.2.448 DOI: 10.1016 / S0022-3468 (84) 80376-0
DOI: 10.1016 / S0022-3468 (84) 80376-0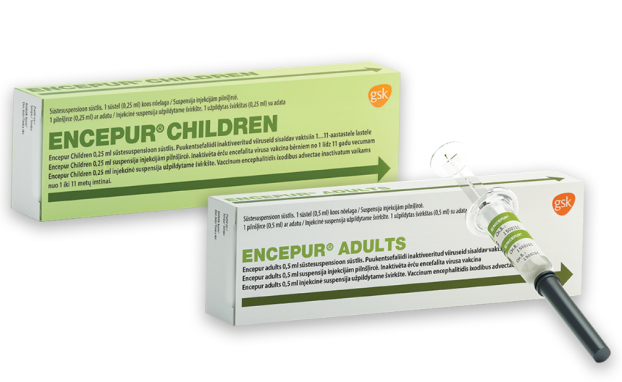 1998.00230.x
1998.00230.x